 Für einen individuellen Ausdruck passen Sie bitte die
Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk; BGI / DGUV-I

 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk; BGI / DGUV-I |  |
BGI 505-7 / DGUV-I 213-507 - Verfahren zur Bestimmung von Dimethylsulfat
Von den Unfallversicherungsträgern anerkannte Analysenverfahren zur Feststellung der Konzentrationen krebserzeugender Arbeitsstoffe in der Luft in Arbeitsbereichen
Berufsgenossenschaftliche Informationen für Sicherheit und Gesundheit bei der Arbeit (BGI/GUV-I)
(Ausgabe 10/2006)
Erprobte und von den Berufsgenossenschaften anerkannte, diskontinuierliche Verfahren zur Bestimmung von Dimethylsulfat (DMS) in Arbeitsbereichen.
Es sind personenbezogene oder ortsfeste Probenahmen für Messungen zur Beurteilung von Arbeitsbereichen möglich:
| 01 | Probenahme mit Pumpe und Adsorption an Kieselgel, Derivatisierung, Dünnschichtchromatographie "Dimethylsulfat - 01 - DC" (erstellt: Dezember 1983; zurückgezogen: Dezember 2005) |
| 02 | Probenahme mit Pumpe und Adsorption an Kieselgel, Gaschromatographie nach Elution "Dimethylsulfat - 02 - GC" (erstellt: Dezember 1983; zurückgezogen: Dezember 2005) |
| 03 | Probenahme mit Pumpe und Adsorption an Tenax-TA, Gaschromatographie nach Elution "Dimethylsulfat - 03 - GC" (erstellt: Januar 1987) |
| 04 | Probenahme mit Pumpe und Adsorption an Tenax-TA, Desorption, Gaschromatographie mit massenselektivem Detektor "Dimethylsulfat - 04 - GC" (erstellt: April 1997) |
| 05 | Probenahme mit Pumpe und Adsorption an Tenax, Gaschromatographie nach Thermodesorption "Dimethylsulfat - 05 - GC (Thermodesorption)" (erstellt: Oktober 2006) |
Die Verfahren sind auch geeignet zur Messung anderer Dialkylsulfate.
| IUPAC-Name: | Dimethylsulfat |
| Cas-Nr.: | 77-78-1 |
| Summenformel: | C2H6O4S |
| Molmasse: | 126,13 g/mol |
03 Probenahme mit Pumpe und Adsorption an Tenax-TA, Gaschromatographie nach Elution
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch Tenax-TA gesaugt. Das aus der Probeluft an Tenax-TA adsorbierte DMS wird nach Elution mit Methylacetat gaschromatographisch mit einem schwefelspezifischen Flammenphotometer-Detektor (FPD) bestimmt. |
| Technische Daten | |
| Nachweisgrenze: | absolut: 3 ng DMS, relativ: 0,003 ml/m3 (ppm)  0,015 mg/m3 an DMS für 10 l Probeluft. 0,015 mg/m3 an DMS für 10 l Probeluft. |
| Spezifität: | Die Kombination von gaschromatographischer Trennung und schwefelspezifischem Detektor bewirkt hohe Spezifität der Methode. |
| Vorteile: | Spezifisches Verfahren zur Bestimmung von DMS; praktisch keine Störempfindlichkeit gegenüber Feuchtigkeit und Ammoniak; längere Lagerfähigkeit der beladenen Röhrchen und Eluat; Messungen kurzzeitiger Expositionen möglich. |
| Nachteile | Keine Anzeige von Konzentrationsspitzen innerhalb der Probenahme, hoher Zeitaufwand. |
| Apparativer Aufwand: | Pumpe mit Gasmengenzähler oder Volumenstromanzeiger, Sammelröhrchen mit Tenax-TA, Gaschromatograph mit FPD. |
Ausführliche Verfahrensbeschreibung
1 Zusammenfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration von DMS im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
Mit Hilfe einer Pumpe, die von einer Person mitgeführt wird oder die ortsfest angebracht ist, wird ein definiertes Luftvolumen durch ein mit Tenax-TA gefülltes Glasröhrchen gesaugt. Das DMS wird an Tenax-TA adsorbiert und anschließend mit Methylacetat eluiert. Die Bestimmung erfolgt mit Hilfe eines mit einem FPD ausgerüsteten Gaschromatographen.
Die absolute Nachweisgrenze beträgt 3 ng DMS.
Die relative Nachweisgrenze beträgt
0,003 ml/m3 (ppm)  0,015 mg/m3 an DMS Für 10 l Probeluft.
0,015 mg/m3 an DMS Für 10 l Probeluft.
Das Verfahren ist erprobt für Dimethylsulfat und Diethylsulfat.
2 Geräte, Chemikalien und Lösungen
2.1 Geräte
Für die Probenahme und Probenaufbereitung:
Pumpe mit Gasmengenzähler oder Volumenstromanzeiger.
| Sammelröhrchen: | Ein mit Kunststoffkappen verschließbares Glasröhrchen wird mit ca. 50 mg Tenax-TA gefüllt. Das Tenax-TA wird mit kleinen Pfropfen silanisierter Glaswolle Fixiert.
Die Abmessungen der Sammelröhrchen müssen den Abmessungen des Sammelkopfes der Pumpe angepasst sein.
Bewährt haben sich Sammelröhrchen mit 50 mm Länge, 6 mm Außen- und 4 mm Innendurchmesser. 50 mg Tenax-TA ergeben in diesem Röhrchen eine Füllhöhe von 35 mm. |
| Probengefäß: | Volumen ca. 2 ml, mit PTFE 1 -kaschiertem Septum und Aluminium-Verschlusskappe.
Vorrichtung zum Verschließen der Probengefäße. Für die analytische Bestimmung: |
| Gaschromatograph: | Mit Flammenphotometer-Detektor, gepackter Trennsäule und Dreiwege-Ventil. |
2.2 Chemikalien und Lösungen
Methylacetat p.a.:
Auf Abwesenheit störender Schwefelverbindungen prüfen.
Dimethylsulfat, destilliert,
Tenax-TA, 60-80 mesh,
Dimethylsulfat-Stammlösung
Lösung von 200 µg DMS in 1 ml Methylacetat.
Mit Hilfe einer Injektionsspritze werden 7,5 µl  10 mg Dimethylsulfat in 50 ml Methylacetat gelöst.
10 mg Dimethylsulfat in 50 ml Methylacetat gelöst.
Kalibrierlösungen:
Von der Stammlösung werden durch Verdünnen z.B. Lösungen mit 2 µg, 5 µg, 10 µg. 20 µg und 50 µg Dimethylsulfat in jeweils 50 ml Methylacetat hergestellt.
Gase zum Betrieb des Gaschromatographen:
Helium, synthetische Luft, Sauerstoff und Wasserstoff.
3 Probenahme und Probenaufbereitung
Ein mit Tenax-TA gefülltes Glasröhrchen wird geöffnet und mit der Pumpe verbunden. Pumpe und Röhrchen werden von einer Person während der Arbeitszeit getragen oder ortsfest verwendet. Der Volumenstrom beträgt ca. 4 l/h.
Nach Beendigung der Probenahme wird der Inhalt des Sammelröhrchens in ein Probengefäß (siehe Abschnitt 2.1) entleert. Nach Zugabe von 1 ml Methylacetat wird das Probengefäß mit Septum und Kappe verschlossen und 1 Minute geschüttelt. Nach dem Absetzen des Tenax-TA wird die überstehende Lösung (Eluat) zur gaschromatographischen Untersuchung verwendet.
4 Gaschromatographische Arbeitsbedingungen
Die in Abschnitt 8 angegebenen Verfahrenskenngrößen wurden unter folgenden Gerätebedingungen erarbeitet:
| Gerät: | Gaschromatograph Carlo Erba, Modell 2150, mit Flammenphotometer-Detektor, Modell 250.
Zwischen Trennsäule und Detektor befand sich ein Dreiwege-Ventil. Dieses ist erforderlich zum Ausschleusen des Methylacetats, das erhebliche Störungen hervorrufen kann. |
| Trennsäule: | Edelstahl, Länge 120 cm, Innendurchmesser 3 mm, gefüllt mit 10 % OS 138 (Polyphenylether) auf Gaschrom Q, Korngröße 80-100 mesh. |
| Temperaturen: | Einspritzblock: 200 °C, Säule: 160 °C, isotherm, Detektor: 200 °C. |
| Trägergas: | Helium (Volumenstrom 150 ml/min). |
| Brenngase: | Synth.
Luft (Volumenstrom 30 ml/min), Sauerstoff (Volumenstrom 30 ml/min), Wasserstoff (Volumenstrom 85 ml/min). |
Photomultiplier-Spannung: 710 V.
5 Analytische Bestimmung
Nach Konditionieren des gaschromatographischen Systems (siehe Abschnitt 9) werden zur analytischen Bestimmung 20 µl des Eluates in den Gaschromatographen injiziert und die Höhe oder Fläche des Dimethylsulfat-Peaks ermittelt. Die Retentionszeit von Dimethylsulfat beträgt für die Bedingungen des Abschnitts 4 etwa 1 Minute.
6 Kalibrierung
Da sich die Empfindlichkeit des gaschromatographischen Systems ändern kann, stellt man keine Kalibrierkurve auf.
Die Kalibrierung geschieht nach der Methode des äußeren Standards. Dazu werden jeweils 20 µl der Kalibrierlösungen (siehe Abschnitt 2.2) in den Gaschromatographen injiziert.
Nach der gaschromatographischen Analyse der Probelösung (Eluat, siehe Abschnitt 5) wird zum Berechnen des Analysenergebnisses diejenige Kalibrierlösung verwendet, deren DMS-Peak hinsichtlich Fläche oder Höhe dem DMS-Peak der Probelösung am nächsten liegt.
Die analytische Bestimmung und Kalibrierung werden unter derselben Geräteeinstellung und mit derselben Spritze durchgeführt.
Um sicherzustellen, dass Tenax-TA und Methylacetat keine störenden Verunreinigungen enthalten, wird 1 ml Methylacetat mit ca. 50 mg des verwendeten Tenax-TA versetzt und analysiert.
7 Berechnen des Analysenergebnisses
Die Berechnung der Dimethylsulfat-Konzentration der Probeluft in mg/m3 erfolgt nach der Formel (1):
| (1) | 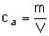 |
Für die Errechnung der Volumenkonzentration cv in ml/m3 aus ca gilt, wenn ca bezogen ist auf 20 °C und 1013 mbar:
| (2) | cv = 0,19 * ca |
Es bedeuten:
| ca | = Massenkonzentration von Dimethylsulfat in der Probeluft in mg/m3, |
| cv | = Volumenkonzentration von Dimethylsulfat in der Probeluft in ml/m3 (ppm), |
| m | = Masse Dimethylsulfat in der Probelösung (Eluat) in µg, |
| V | = Probeluftvolumen in l. |
8 Beurteilung des Verfahrens
8.1 Präzision
Für das vollständige Messverfahren ergab sich eine relative Standardabweichung von ± 12 % (n = 10, P = 95 %).
8.2 Nachweisgrenze
Die absolute Nachweisgrenze beträgt 3 ng DMS.
Die relative Nachweisgrenze beträgt
0,003 ml/m3 (ppm)  0,015 mg/m3 an DMS für 10 l Probeluft,
0,015 mg/m3 an DMS für 10 l Probeluft,
1 ml Eluatvolumen und 20 µl Injektionsvolumen.
8.3 Spezifität
Durch die Kombination von gaschromatographischer Trennung mit schwefelspezifischem Detektor ist das beschriebene Verfahren weitgehend spezifisch.
8.4 Oberführungsrate
Zur Bestimmung der Überführungsrate wurden 50 µl Toluol, in denen 1 µg DMS gelöst war, in das Sammelröhrchen gespritzt und anschließend 16 l Luft mit einem Volumenstrom von 2 l/h durchgesaugt. Aus 19 Messungen ergab sich eine Überführungsrate > 93 %.
8.5 Haltbarkeit
Beladene Sammelröhrchen und Kalibrierlösungen können bei Raumtemperatur mindestens 10 Tage ohne Veränderung aufbewahrt werden.
9 Besondere Hinweise
Vor jeder Messreihe ist das gaschromatographische System mit Dimethylsulfat zu konditionieren. Dazu werden zweimal jeweils 5 µl einer Lösung aufgegeben, die in 50 ml Methylacetat ca. 1 mg Dimethylsulfat enthält. Danach wird durch Aufgeben von 20 µl Methylacetat sichergestellt, dass keine "Memory-Effekte" auftreten. Gegebenenfalls ist Methylacetat nochmals zu injizieren.
Es hat sich als zweckmäßig erwiesen, die Trennsäule nur für Dimethylsulfat-Analysen zu verwenden.
10 Hersteller
| Pumpe: | z.B. Modell 4903, Compur Electronic, München; |
| Tenax-TA: | z.B. Chrompack Deutschland, Müllheim/Baden, Macherey-Nagel GmbH & Co KG, Düren; |
| Gaschromatographen: | z.B. Carlo Erba, Vertrieb in Deutschland: Erba Science, Hofheim/Ts., Siemens AG, Karlsruhe. |
04 Probenahme mit Pumpe und Adsorption an Tenax-TA, Desorption, Gaschromatographie mit massenselektivem Detektor
Kurzfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration von Dimethylsulfat (DMS) im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein Tenax-Röhrchen gesaugt. Das adsorbierte Dimethylsulfat wird mit Toluol desorbiert und gaschromatographisch mittels massenselektiver Detektion bestimmt |
| Technische Daten | |
| Bestimmungsgrenze: | absolut: 0,4 ng Dimethylsulfat relativ: 0,01 mg/m3 an Dimethylsulfat für 20 l Probeluft, 1 ml Desorptionslösung und 2 µl Injektionsvolumen |
| Selektivität: | Durch die Kombination von gaschromatographischer Trennung und massenselektiver Detektion ist das Verfahren selektiv. |
| Vorteile: | Personenbezogene und selektive Messungen möglich. |
| Nachteile: | Keine Anzeige von Konzentrationsspitzen. |
| Apparativer Aufwand: | Pumpe, Gasmengenzähler oder Volumenstromanzeiger, Tenax-Röhrchen, Gaschromatograph mit massenselektivem Detektor. |
Ausführliche Verfahrensbeschreibung
1 Geräte, Chemikalien und Lösungen
1.1 Geräte
Für die Probenahme:
Ein mit Kunststoffkappen verschließbares Glasröhrchen wird mit ca. 50 mg Tenax-TA gefüllt. Das Tenax-TA wird mit kleinen Pfropfen silanisierter Glaswolle fixiert. Die Abmessungen der Sammelröhrchen müssen den Abmessungen des Sammelkopfes der Pumpe angepasst sein. Bewährt haben sich Sammelröhrchen mit 50 mm Länge, 6 mm Außen- und 4 mm Innendurchmesser. 50 mg Tenax-TA ergeben in diesem Röhrchen eine Füllhöhe von 35 mm.
Für die Probenaufbereitung und Analyse:
1.2 Chemikalien und Lösungen
| Dimesthylulfat: | Reinheit mind. 99 %, z.B. Firma Fluka, 89231 Neu-Ulm. |
| Desorptionsmittel: | Toluol, getrocknet über Molekularsieb. |
| DMS-Stammlösung: | Lösung von 0,2 mg DMS in 1 ml Toluol.
In einen 50-ml-Messkolben werden einige Milliliter Desorptionsmittel vorgelegt und 7,5 µl, (10 mg) DMS mit einer 10-µl-Spritze hinzugegeben. Anschließend wird der Messkolben mit Toluol bis zur Marke aufgefüllt. |
| Kalibrierlösungen: | Lösungen von je 0,2 µg, 2 µg, 4 µg DMS pro ml Toluol.
In einen 50-ml-Messkolben werden einige Milliliter Desorptionsmittel vorgelegt und jeweils 50 µl, 0,5 ml und 1 ml Stammlösung hinzugefügt. |
| Gase zum Betrieb des Gaschromatographen: | Helium, geeignet zum Betrieb eines massenselektiven Detektors. |
2 Probenahme
Ein Tenax-Röhrchen wird geöffnet und mit der Pumpe verbunden. Der Volumenstrom wird auf ca. 3,3 l/h eingestellt. Bei einer Probenahmedauer von ca. 6 Stunden entspricht dies einem Probeluftvolumen von ca. 20 l. Pumpe und Röhrchen werden von einer Person während der Arbeitszeit getragen oder ortsfest verwendet. Nach Beendigung der Probenahme wird das Röhrchen dicht verschlossen. Das Verfahren wurde bis zu einem Probeluftvolumen von 40 l bei einem max. Volumenstrom von 4 l/h überprüft.
3 Analytische Bestimmung
3.1 Probenaufbereitung und Analyse
Der gesamte Inhalt des beladenen Tenax-Röhrchens wird in ein 5-ml-Probengefäß überführt. Nach dem Zusatz von 1 ml Desorptionsmittel wird das Gefäß verschlossen, 30 Minuten lang vorsichtig geschüttelt und unmittelbar danach analysiert. Um sicherzustellen, dass das verwendete Toluol und Tenax-TA keine störenden Verunreinigungen enthalten, wird die Füllung eines unbeladenen Röhrchens wie zuvor beschrieben behandelt (Leerwertlösung).
Jeweils 2 µl der Desorptionslösung und der Leerwertlösung werden in den Gaschromatographen eingespritzt. Die quantitative Auswertung der Chromatogramme erfolgt nach der Methode des externen Standards.
3.2 Gaschromatographische Arbeitsbedingungen
Die in Abschnitt 5 angegebenen Verfahrenskenngrößen wurden unter folgenden Gerätebedingungen erarbeitet:
| Gerät: | Gaschromatograph Hewlett-Packard 5890 mit MSD HP 5970, Split-/Splitless-Injektor und automatischem Probengeber HP 7673. |
| Trennsäule: | Quarzkapillare, stationäre Phase 95 % Methylsilikon +5 % Methylphenylsilikon (HP-5 von Hewlett-Packard), Länge 50 m, Innendurchmesser 0,20 mm, Filmdicke 0,33 µm. |
| Temperaturen: | Injektor: 200 °C, Ofen: Anfangstemperatur: 50 °C, 2 min isotherm, Heizrate 1: 10 °C/min bis 220 °C, Heizrate 2: 30 °C/min, Endtemperatur: 250 °C, 15 min isotherm, Transferleitung: 250 °C. |
| Injektionsart: | splitlos, 1 min. |
| Trägergas: | Helium, 180 Pa Vordruck. |
| Injektionsvolumen: | 2 gl. |
| Ionisierungsart: | Elektronenstoßionisation (70 eV) |
| Messmodus: | selected ion monitoring (SIM-MODE). Registriermassen (m/z): 66; 95; 96. |
| Dwelltime: | 200 ms/Registriermasse. |
4 Auswertung
4.1 Kalibrierung
Von den unter Abschnitt 1.2 beschriebenen Kalibrierlösungen werden jeweils 2 µl in den Gaschromatographen eingespritzt. Durch Auftragen der ermittelten Peakflächen über die in den jeweiligen Kalibrierlösungen enthaltenen Konzentrationen in µg/ml wird die Kalibrierkurve erstellt.
Die Linearität der Kalibrierkurven ist nicht über den gesamten geprüften Konzentrationsbereich gegeben. Innerhalb enger Konzentrationsbereiche sind die Kalibrierkurven jedoch hinreichend linear. Somit lässt sich die nichtlineare Kalibrierkurve durch einen Polygonzug darstellen.
4.2 Berechnen des Analysenergebnisses
Die Berechnung der Massenkonzentration an DMS in der Probeluft in mg/m3 erfolgt nach der Formel (1):
| (1) | 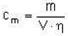 |
Für die Berechnung der Volumenkonzentration cv in ml/m3 aus cm gilt, bezogen auf 20 °C und 1013 hPa:
(2) cv = 0,19 * cm
Es bedeuten:
| cm | = Massenkonzentration von DMS in der Probeluft in mg/m3, |
| cv | = Volumenkonzentration von DMS in der Probeluft in ml/m3 (ppm), |
| m | = die aus der entsprechenden Kalibrierkurve ermittelte Masse von DMS in der Desorptionslösung in µg |
| V | = Probeluftvolumen in l, |
| η | = Wiederfindungsrate. |
5 Beurteilung des Verfahrens
5.1 Genauigkeit und Wiederfindungsrate
Jeweils 5 Sammelröhrchen wurden mit je 0,4 µg 4 µg und 8 µg, Dimethylsulfat beaufschlagt (jeweils 100 µl Kalibrierlösung der Konzentration 4 µg/ml bzw. 20 µl und 40 µl Stammlösung). Anschließend wurde ca. 6 Stunden lang Laborluft (15 - 25 % relative Luftfeuchte) mit einem Volumenstrom von 3,3 l/h durch das jeweilige Röhrchen gesaugt.
Die dotierten Massen entsprechen bei 20 l Luftvolumen Konzentrationen von 0,02 mg/m3 bis 0,4 mg/m3. Es ergaben sich relative Standardabweichungen wie in der Tabelle 1 ersichtlich:
| Konzentration mg/m3 | relative Standardabweichung % |
| 0,02 | 4,1 |
| 0,2 | 1,6 |
| 0,4 | 3,2 |
Bei einem Luftvolumen von 20 l und einem Volumenstrom von ca. 3,3 l/Stunde lag die Wiederfindungsrate bei 0,8.
5.2 Bestimmungsgrenze
Die absolute Bestimmungsgrenze beträgt 0,4 ng. Das entspricht 0,2 µg pro Tenax-Röhrchen bzw. Probe.
Die Bestimmungsgrenze wurde nach DIN 32645 als ein Vielfaches der Verfahrensstandardabweichung ermittelt.
Die relative Bestimmungsgrenze beträgt 0,01 mg/m3 an DMS für 20 l Probeluft, 1 ml Desorptionslösung und 2 µl Injektionsvolumen.
5.3 Selektivität
Durch die Kombination von gaschromatographischer Trennung und massenselektiver Detektion ist das Verfahren selektiv.
6 Bemerkungen
Die Lagerfähigkeit (Kühlschrank) des Dimethylsulfats im adsorbierten Zustand beträgt mindestens 14 Tage. Die Kalibrierlösungen und die Stammlösung müssen nach spätestens 48 Stunden neu angesetzt werden, da im Toluol vorhandenes Restwasser das Dimethylsulfat zerstört.
Vor jeder Messreihe ist das gaschromatographische System mit Dimethylsulfat zu konditionieren. Dazu werden zweimal jeweils 2 µl einer Lösung, die in 1 ml Toluol ca. 0,2 mg Dimethylsulfat enthält, in den Gaschromatographen eingespritzt. Danach wird durch Injizieren von 2 µl Toluol sichergestellt, dass keine "Memory-Effekte" auftreten. Gegebenenfalls ist Toluol nochmals zu injizieren.
Es hat sich als zweckmäßig erwiesen, die Trennsäule nur für Dialkylsulfat-Analysen zu verwenden.
05 Probenahme mit Pumpe und Adsorption an Tenax, Gaschromarographie nach Thermodesorption
Kurzfassung:
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration an Dimethylsulfat (DMS) im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein mit Tenax gefülltes Metallröhrchen gesaugt. Danach wird das adsorbierte DMS thermisch desorbiert und anschließend gaschromatographisch bestimmt. |
| Technische Daten | |
| Bestimmungsgrenze: | absolut: 23 ng DMS
relativ: 0,9 µg/m3 an DMS bei 25 l Probeluft. |
| Selektivität: | Durch die Kombination von gaschromatographischer Trennung und massenselektiver Detektion ist das Verfahren selektiv. |
| Vorteile: | Personenbezogene und selektive Messungen möglich. |
| Nachteile: | Keine Anzeige von Konzentrationsspitzen. |
| Apparativer Aufwand: | Pumpe mit Gasmengenzähler oder Volumenstromanzeiger, Adsorptionsröhrchen gefüllt mit Tenax, Gaschromatograph mit Thermodesorber und massenselektivem Detektor. |
Ausführliche Verfahrensbeschreibung
1 Geräte, Chemikalien und Lösungen
1.1 Geräte
Für die Probenahme:
Für die Probenaufbereitung und analytische Bestimmung:
1.2 Chemikalien und Lösungen
Tenax TA 60 - 80 mesh, z.B. Fa. Supelco, 82024 Taufkirchen
Naphthalin > 99 %, , z.B. Fa. Aldrich, 82024 Taufkirchen
Dimethylsulfat 99 %, z.B. Fa. Aldrich
Methyltert.-butylether (MTBE), Reinheit 99,8 %, wasserfrei, z.B. Fa. Aldrich
Naphthalin-Stammlösung:
Lösung von ca. 5,32 mg Naphthalin/ml Methyltert.-butylether (MTBE)
In einen 5-ml-Messkolben werden ca. 26,6 mg Naphthalin auf 0,1 mg genau eingewogen, mit MTBE bis zur Marke aufgefüllt und umgeschüttelt.
Lösung interner Standard (IStd):
Lösung von ca. 266 µg Naphthalin (IStd)/ml MTBE.
In einen 10-ml-Messkolben, der einige ml MTBE enthält, werden 500 µl der Naphthalin-Stammlösung einpipettiert, mit MTBE bis zur Marke aufgefüllt und umgeschüttelt.
Kalibrierstammlösung:
Lösung von ca. 20 mg DMS/ml MTBE.
In einen 10-ml-Messkolben, der einige ml MTBE enthält, werden ca. 150 µl DMS einpipettiert und auf 0,1 mg genau gewogen, mit MTBE bis zur Marke aufgefüllt und umgeschüttelt.
Kalibrierlösungen:
Lösungen von 50 bis 1000 µg DMS/ml MTBE
In sechs 10-ml-Messkolben werden jeweils einige Milliliter MTBE vorgelegt. Anschließend werden je 25 µl, 100 µl, 200 µl, 300 µl, 400 µl und 500 µl der Kalibrierstammlösung zugegeben, mit MTBE bis zur Marke aufgefüllt und umgeschüttelt.
Jeweils 5 µl der Lösungen werden auf sechs Tenaxröhrchen aufgegeben. Mit diesen Adsorptionsröhrchen wird für ein Probeluftvolumen von 25 l ein Konzentrationsbereich an DMS von 0,01 mg/m3 bis 0,198 mg/m3 erfasst. Die entsprechenden Konzentrationen sind in Tabelle 1 aufgeführt.
Tabelle 1: Konzentrationen der Kalibrierlösungen
| Zugabe Stammlösung [µl] | Konzentration [mg/l] | Konzentration [mg/m3] 3 |
| 25 | 50 | 0,010 |
| 100 | 200 | 0,040 |
| 200 | 400 | 0,079 |
| 300 | 600 | 0,119 |
| 400 | 800 | 0,158 |
| 500 | 1000 | 0,198 |
2 Probenahme
Kurz vor der Verwendung wird das vorgereinigte Adsorptionsröhrchen erneut ca. 15 Minuten im Thermodesorber bei 250 °C im Heliumstrom ausgeheizt. Anschließend werden 5 µl der Lösung des internen Standards aufgegeben und das Röhrchen mit Hilfe von Swagelok®-Verschraubungen mit Teflon-Dichtungen verschlossen.
Zur Probenahme wird das Adsorptionsröhrchen geöffnet und mit der Pumpe verbunden. Pumpe und Röhrchen werden von einer Person während der Probenahmezeit getragen oder ortsfest verwendet. Der Volumenstrom wird auf 100 ml/min eingestellt. Bei einer Probenahmedauer von 4 Stunden entspricht dies einem Volumen von ca. 25 l. Nach Beendigung der Probenahme wird das Röhrchen dicht verschlossen.
3 Analytische Bestimmung
3.1 Probenaufbereitung und Analyse
Das beladene Adsorptionsröhrchen wird geöffnet und in den Thermodesorber gegeben. Durch Erhitzen wird das adsorbierte DMS mittels Helium desorbiert, in einer mit Tenax TA gepackten Kühlfalle aufgefangen und von dort durch schlagartiges Aufheizen (gerätespezifische Aufheizrate ca. 40 °C/sec) in die Trennsäule des Gaschromatographen überführt und ein Chromatogramm angefertigt. Die quantitative Auswertung erfolgt nach der Methode des internen Standards über die Flächen oder Höhen des DMS und des Naphthalins als internem Standard.
3.2 Gaschromatographische Arbeitsbedingungen
Die in Abschnitt 5 angegebenen Verfahrenskenngrößen wurden unter folgenden Gerätebedingungen erarbeitet:
| Gerät: | Thermodesorber ATD 400 der Firma Perkin Elmer, 63110 Rodgau-Jügesheim Gaschromatograph HP 6890 mit massenselektivem Detektor MSD HP 5872 |
| Temperaturen: | Desorptionsofen: 250 °C Überführungsleitung: 200 °C Kühlfalle (Füllung Tenax TA) Adsorption: -30 °C Injektion: 280 °C Desorptionsfluss: 11,4 ml/min Desorptionszeit: 5 min Outlet-Split: 20,0 ml/min Inlet-Split: geschlossen |
| GC-Bedingungen: | |
| Trennsäule: | Quarzkapillare, stationäre Phase DB-1 quervernetzt (Dimethylpolysiloxan), Innendurchmesser 0,25 mm, Filmdicke 1 µm, Länge 30 m |
| Temperaturen: | Transferline MS: 280 °C, Detektor: 250 °C Ofen: Anfangstemperatur: 50 °C, Heizrate 20 °C/min auf Endtemperatur 240 °C |
| Trägergas: | Helium 24 psi Vordruck |
| MSD-Parameter: | |
| Ionisierungsart: | Elektronenstoßionisation (70 eV) |
| MS Quad | 150 °C |
| MS Source | 230 °C |
| Scan Parameters | Low Mass: 50 |
| High Mass: | 550 |
| Solvent Delay | 3.00 min |
| Messmodus: | SIM-Mode Registriermassen (m/z in amu) Quantifizierung / Qualifizierung Naphthalin 128.127 DMS 95 96 |
4 Auswertung
4.1 Kalibrierung
Zur Kalibrierung werden jeweils 5 µl, der unter Abschnitt 1.2 exemplarisch beschriebenen Kalibrierlösungen mit einer Mikroliterspritze auf Adsorptionsröhrchen aufgegeben und anschließend 10 Minuten Luft mit einem Volumenstrom von ca. 50 ml/min zur Verdampfung des MTBEs durch die Röhrchen gesaugt. Die auf den Adsorptionsröhrchen dotierten Mengen an DMS sowie die auf ein Probeluftvolumen von 25 l umgerechneten Luftkonzentrationen sind in Tabelle 1 angegeben. Die Röhrchen werden anschließend wie unter 3.2 beschrieben analysiert.
Durch Auftragen der Quotienten der Peakflächen des DMS und des internen Standards gegen die Quotienten der Massen des DMS und des internen Standards auf dem Adsorptionsröhrchen ermittelt man durch Regressionsrechnung die Kalibrierfunktion.
4.2 Berechnen des Analysenergebnisses
Aus der Kalibrierkurve wird die zur Peakfläche (-höhe) zugehörige Masse des DMS auf dem Adsorptionsröhrchen entnommen.
Die Berechnung der DMS-Konzentration in der Probeluft in mg/m3 erfolgt nach Formel (1):
| (1) | 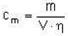 |
Es bedeuten:
| cm | = Massenkonzentration des DMS in der Probeluft in mg/m3 |
| m | = Adsorbierte Masse des DMS in µg, auf dem Röhrchen |
| V | = Probeluftvolumen in l |
| η | = Wiederfindung (siehe Tabellen 2 und 3) |
5 Beurteilung des Verfahrens
5.1 Präzision und Wiederfindung
Die Präzision im Mindestmessbereich nach DIN EN 482 [1] sowie die Wiederfindung wurden für drei Konzentrationen (siehe Tabellen 2 und 3) bestimmt.
Für die Einstellung der Luftkonzentrationen wurden folgende Validierlösungen hergestellt:
| Validierstammlösung: | Lösung von 22,5 mg DMS/ml MTBE.
In einen 10-ml-Messkolben, der einige ml MTBE enthält, werden 170 µl DMS einpipettiert und auf 0,1 mg genau gewogen, mit MTBE bis zur Marke aufgefüllt und umgeschüttelt. |
| Validierlösungen: | Drei Lösungen von 56, 562 und 1124 µg DMS/ml MTBE
In drei 10-ml-Messkolben wurden jeweils einige Milliliter MTBE vorgelegt. Anschließend wurden je 25 µl, 250 µl und 500 µl der Kalibrierstammlösung zugegeben und mit der MTBE bis zur Marke aufgefüllt und umgeschüttelt. |
Zur Ermittlung der Präzision des Verfahrens wurden pro zu untersuchender Konzentration 6 Adsorptionsröhrchen über einen Sechsfachröhrchenhalter, bei dem für jedes Röhrchen der Volumenstrom separat eingestellt werden konnte, mit der Pumpe verbunden. Vor jedem Probenahmesystem (siehe Abschnitt 2) wurde mit einem kurzen Stück Teflonschlauch ein mit einem Quarzwollepfropf gefülltes Glasröhrchen angebracht. Für die Einstellung der Validierkonzentrationen bei 0,23 mg/m3, 0,11 mg/m3 und 0,01 mg/m3 wurden jeweils 5 µl, der drei Validierlösungen auf die Quarzwolle dosiert. Anschließend wurde über jedes Röhrchen bei Raumtemperatur (23 - 25 °C) 25 l Luft mit einem Volumenstrom von 200 ml/min gesaugt.
Die beschriebenen Versuche wurden bei Luftfeuchten von ca. 55 % und 85 % durchgeführt. Die injizierten Substanzmassen entsprachen bei 25 l Gasvolumen den in den Tabellen 2 und 3 angegebenen Konzentrationen. Für eine relative Luftfeuchte von 55 % sind die ermittelten Kenndaten in der Tabelle 2 aufgeführt. Es ergab sich eine mittlere Standardabweichung von 5,9 %, die mittlere Wiederfindung lag bei 0,98.
Tabelle 2: Kenndaten des Messverfahrens (Feuchte ca. 55 %)
| Konzentration DMS [mg/m3] | rel. Standard- abweichung [%] | Wiederfindung η |
| 0,01 | 7,9 | 1,02 |
| 0,11 | 5,4 | 0,99 |
| 0,23 | 4,3 | 0,92 |
Für eine relative Luftfeuchte von 85 % sind die ermittelten Kenndaten in der Tabelle 3 aufgeführt. Es ergab sich eine mittlere Standardabweichung von 4,3 %, die mittlere Wiederfindung lag bei 0,88.
Tabelle 3: Kenndaten des Messverfahrens (Feuchte ca. 85 %)
| Konzentration DMS [mg/m3] | rel. Standard- abweichung [%] | Wiederfindung · |
| 0,01 | 5,3 | 0,84 |
| 0,11 | 4,4 | 0,89 |
| 0,23 | 3,1 | 0,92 |
Die relative Luftfeuchte beeinflusst die relativen Standardabweichungen nur wenig.
Bei einer höheren Luftfeuchte sank die Wiederfindung für die niedrigeren Konzentrationen merklich.
Die Lagerstabilität des DMS auf den Adsorptionsröhrchen wird von der Luftfeuchte zum Zeitpunkt der Probenahme nicht merklich verändert.
5.2 Bestimmungsgrenzen
Die Bestimmungsgrenze wurde in Anlehnung an die in der DIN EN 32645 [2] beschriebene Schnellschätzung der Bestimmungsgrenze ermittelt. Die für die Berechnung benötigte Standardabweichung wurde durch sechsmalige Injektion einer DMS-Lösung mit einer Konzentration von 0,025 mg/ml (entsprechend 0,005 µg/m3 für 25 l Probeluftvolumen) ermittelt.
Die absolute Bestimmungsgrenze beträgt 23 ng DMS. Die relative Bestimmungsgrenze liegt bei 0,9 µg/m3 für 25 l Probeluft.
5.3 Selektivität
Durch die Kombination von gaschromatographischer Trennung und massenselektiver Detektion ist das Verfahren selektiv.
6 Bemerkungen
Die Lagerfähigkeit des DMS im adsorbierten Zustand beträgt bei Raumtemperatur mindestens 7 Tage.
Die Kalibrierlösungen und die Stammlösung müssen nach spätestens 48 Stunden neu angesetzt werden, da im MTBE enthaltenes Restwasser das DMS hydrolysiert.
7 Literatur
| [1] | DIN EN 482 Arbeitsplatzatmosphäre - Allgemeine Anforderungen an Verfahren für die Messung von chemischen Arbeitsstoffen, Beuth Verlag, Berlin 1994 |
| [2] | DIN EN 32645 Chemische Analytik - Nachweis-, Erfassungs- und Bestimmungsgrenze, Beuth Verlag, Berlin 1994 |
________
| 1 | Polytetrafluorethylen. |
| 2 | Polytetrafluorethylen. |
| 3 | bzgl. 25 l Probeluftvolumen |
 | ENDE |  |