 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. ▢ Regelwerk; BGI / DGUV-I |
BGI 505-19 / DGUV Information 213-519 - Von den Berufsgenossenschaften anerkannte Analysenverfahren zur Feststellung der Konzentrationen krebserzeugender Arbeitsstoffe in der Luft in Arbeitsbereichen - Verfahren zur Bestimmung von Ethylenimin
Berufsgenossenschaftliche Informationen für Sicherheit und Gesundheit bei der Arbeit (BGI)
(bisherige ZH 1/120.19)
(Ausgabe 12/1983)
Erprobte und von den Berufsgenossenschaften anerkannte Verfahren zur Bestimmung von Ethylenimin in Arbeitsbereichen.
Diskontinuierliche VerfahrenEs sind personenbezogene oder ortsfeste Probenahmen für Messungen zur Beurteilung von Arbeitsbereichen möglich:
Probenahme mit Absorption in Folins Reagenz, Flüssigkeits-Chromatographie (HPLC) 1.Kontinuierliche Verfahren
Zur Konzentrationsüberwachung in Arbeitsbereichen können Geräte mit stickstoffspezifischem (thermoionischem) Detektor (PND, TID) eingesetzt werden.
Kontinuierliche Verfahren
Gerät mit stickstoffspezifischem (thermoionischem) Detektor zur ortsfesten Messung
| Messprinzip: | Ein definiertes Probeluftvolumen wird mit Wasserstoff gemischt und über eine auf 600 °C erhitzte Rubidiumbromidpastille, die Rubidiumbromiddampf in den Gasstrom abgibt, einem elektrischen Spannungsfeld zugeführt.
Enthält die Probeluft Ethylenimin oder andere organische Stickstoffverbindungen, so steigt der im Spannungsfeld fließende Ionenstrom proportional zur Konzentration dieser Verbindungen an. Die Änderung des Ionenstromes wird gemessen. |
| Technische Daten | |
| Kleinster Messbereich: | 0 ... 2 ml/m3 (ppm). |
| Nachweisgrenze: | 0, 2 ml/m3 (ppm)  0,4 mg/m3 an Ethylenimin. 0,4 mg/m3 an Ethylenimin. |
| Spezifität: | Nicht gegeben
(nur stickstoffspezifische Messung möglich; Propylenimin, Amine, Nitrile und Blausäure werden mit angezeigt). |
| Anzeigeverzögerung: | T90 ~ 2 sec. |
| Vorteile: | Angabe örtlicher und zeitlicher Änderungen der Konzentration möglich rasche und unmittelbare Anzeige.
Günstiges Signal-Rausch-Verhältnis sowie geringe Nulliniendrift. |
| Betriebsmittel: | Reinstwasserstoff , Rubidiumbromidpastillen. |
| Hersteller: | z.B. Siemens AG, Karlsruhe. |
Diskontinuierliche Verfahren
Probenahme mit Absorption in Folins Reagenz und flüssigkeitschromatographische Bestimmung (HPLC)
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch eine mit einer Lösung von Folins-Reagenz (1,2-Naphthochinon-4-sulfonat) beschickte Waschflasche gesaugt.
Das absorbierte Ethylenimin reagiert in dieser Lösung zu 4-(1-Aziridinyl)-1,2-Naphthochinon.
Das Reaktionsprodukt wird nach beendeter Probenahme mit Chloroform extrahiert.
Die Bestimmung erfolgt mittels Flüssigkeits-Chromatographie. |
| Technische Daten
Nachweisgrenze: | Unter den Bedingungen in der Praxis beträgt die relative Nachweisgrenze 0,1 ml/m3 (ppm)  0,2 mg/m3 an Ethylenimin. 0,2 mg/m3 an Ethylenimin. |
| Spezifität: | Die Spezifität ist in jedem Einzelfall zu prüfen.
Störungen ergeben sich nur durch Substanzen, die unter den chromatographischen Arbeitsbedingungen die gleiche Retentionszeit wie das Ethylenimin-Derivat aufweisen. |
| Vorteile: | Personenbezogene Messungen;
spezifische Messungen möglich. |
| Nachteile: | Kein Erkennen von Konzentrationsspitzen;
hoher zeitlicher Aufwand. |
| Apparativer Aufwand: | Probenahmeeinrichtung, bestehend aus auslaufsicherer Kleinwaschflasche zur personenbezogenen Probenahme oder Frittenwaschflasche Pumpe, Gasmengenzähler oder Volumenstromanzeiger; HPLC-Gerät mit Photometer-Detektor für die Wellenlänge 254 nm. |
Ausführliche Verfahrensbeschreibung
1 Zusammenfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration von Ethylenimin im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch eine mit einer Lösung von Folins Reagenz (1,2-Naphthochinon-4-sulfonat) beschickte Waschflasche gesaugt. Ethylenimin reagiert in der Lösung zu 4-(1-Aziridinyl)-1,2-naphthochinon. Das Reaktionsprodukt wird nach beendeter Probenahme mit Chloroform extrahiert.
Die Bestimmung erfolgt mittels HPLC.
Unter den Bedingungen in der Praxis beträgt die absolute Nachweisgrenze 10 ng Ethylenimin.
Die relative Nachweisgrenze beträgt 0,1 ml/m3 (ppm)  0,2 mg/m3 an Ethylenimin für 50 l Probeluft.
0,2 mg/m3 an Ethylenimin für 50 l Probeluft.
2 Geräte, Chemikalien und Lösungen
2.1 Geräte
Für die Probenahme:
Pumpe,
Volumenstromanzeiger oder Gasmengenzähler,
Auslaufsichere Kleinwaschflasche oder Frittenwaschflasche, Aluminiumfolie.
Für die Probenaufbereitung und analytische Bestimmung:
Messkolben der Volumina 10 ml, 50 ml, 500 ml,
| Scheidetrichter: | 50 ml, 1 l, |
| HPLC-Gerät: | Geeignet für isokratische Arbeitsweise, |
| Trennsäule: | HIBAR (Merck) LiChrosorb Diol (10 µm),
Länge 25 cm, Innendurchmesser 4 mm, |
| Detektor: | Photometer-Detektor, geeignet für die Messung
bei der Wellenlänge 254 nm, |
| Probenaufgabe: | z.B. Injektionsschleife 10 µl, |
Registrier- und/oder Auswerteeinheit: Kompensationsschreiber oder Rechnerintegrator.
2.2 Chemikalien und Lösungen
Chloroform p.a., mit 1 % Ethanol stabilisiert,
n-Hexan, UV rein,
2-Propanol, UV rein,
Methanol,
Ethylenimin,
Natriumsalz der 1,2-Naphthochinon-4-sulfonsäure (Folins Reagenz).
| Natriumhydroxid-Lösung: | Stoffmengenkonzentration 0,1 mol/l. |
| Kaliumdihydrogenphosphat- Lösung: | Stoffmengenkonzentration 0,1 mol/l. |
| Trinatriumphosphat-Lösung: | Stoffmengenkonzentration 0,5 mol/l. |
| Pufferlösung, pH 7,7: | 100 ml der Kaliumdihydrogenphosphat-Lösung werden mit 93,4 ml der Natriumhydroxid-Lösung gemischt. |
| Reagenzlösung: | In einem 500 ml-Messkolben werden 0,40 g Natriumsalz der 1,2-Naphthochinon-4-sulfonsäure in 100 ml der Pufferlösung gelöst, dann wird mit destilliertem Wasser zur Marke aufgefüllt.
Zur Verringerung des Leerwertes wird die Lösung dreimal mit je 100 ml Chloroform extrahiert. Messkolben und Vorratsgefäße für die Lösung werden mit Aluminiumfolie umhüllt. Die Lösung wird im Kühlschrank aufbewahrt und ist 5 Tage verwendbar. |
| 4-(1-Aziridinyl)-1,2- naphthochinon: | In einen mit Aluminiumfolie umhüllten 1 l-Scheidetrichter wird eine Lösung von 2 g Natriumsalz der 1,2-Naphthochinon-4-sulfonsäure in destilliertem Wasser gegeben.
Man fügt 25 ml der Trinatriumphosphat-Lösung hinzu, schüttelt und prüft, ob der pH-Wert zwischen 10,5 und 11,5 liegt.
Nach Zugabe von 0,3 ml Ethylenimin wird 10 Minuten mit Unterbrechungen geschüttelt. Das gebildete 4-(1-Aziridinyl)-1,2-naphthochinon wird sechsmal mit je 200 ml Chloroform extrahiert. Man vereinigt die Extrakte in einem 2 l-Kolben, der mit Aluminiumfolie umhüllt ist, und treibt das Chloroform mit Hilfe eines Stickstoffstromes unter Ausschluß von Licht ab. Der trockene, orangefarbene Rückstand wird in ein mit Aluminiumfolie umgebenes 50 ml-Becherglas überführt. Nach Zugabe von 35 ml Methanol und 1 ml Chloroform wird kurz gerührt. Man setzt das Becherglas für 10 Minuten in ein Eiswasserbad und filtriert danach den Niederschlag durch ein Papierfilter ab. Der Rückstand auf dem Filter wird mit 4 ml gekühltem Methanol ausgewaschen, mit Stickstoff getrocknet, in eine Braunglas-Flasche gegeben und über Nacht im Exsikkator getrocknet. Der Schmelzpunkt der Verbindung liegt bei 173-175 °C. Sie wird bei Temperaturen unter 0 °C aufbewahrt. |
| Stammlösung: | Eine genau abgewogene Menge zwischen 5 und 10 mg des Ethylenimin-Derivats (4-(1-Aziridinyl)-1,2-naphthochinon wird in 50 ml Chloroform gelöst. |
| Kalibrierlösungen: | Durch Verdünnen der Stammlösung mit Chloroform werden Kalibrierlösungen angesetzt, die - bezogen auf die Ethyleniminäquivalente des Derivats - zwischen 1 und 40 µg/10 ml enthalten (Faktor des Ethyleniminanteils im Derivat 0,216). Die Lösungen sind in mit Aluminiumfolie umhüllten Gefäßen anzusetzen und aufzubewahren. |
| Eluent: | Es werden gemischt 59,5 Vol.-Teile n-Hexan, 40 Vol.-Teile Chloroform mit 1 % Ethanol, 0,5 Vol.-Teile 2-Propanol. |
3 Probenahme
3.1 Probenahme mit Kleinwaschflaschen
Durch eine mit Aluminiumfolie umhüllte Kleinwaschflasche, die etwa 4 ml Absorptionslösung enthält, werden mit Hilfe einer Pumpe ca. 5 l Luft pro Stunde gesaugt. Pumpe und Waschflasche können von einer Person getragen oder ortsfest verwendet werden.
3.2 Probenahme mit Frittenwaschflaschen
Durch eine mit ca. 20 ml Absorptionslösung gefüllte und mit Aluminiumfolie umgebene Frittenwaschflasche wird Luft mit einem Volumenstrom von ca. 50 l/h gesaugt.
4 Probenaufbereitung
Die Waschflaschen werden in einen 10 ml- bzw. 25 ml-Messkolben entleert und mit Reagenzlösung nachgespült. Der Messkolben wird mit Reagenzlösung zur Marke aufgefüllt. Der Messkolbeninhalt wird im Scheidetrichter zweimal mit je 4 ml Chloroform extrahiert. Das Chloroform aus dem Scheidetrichter wird durch ein Papierfilter in einen 10 ml-Messkolben gegeben. Das Papierfilter wird mit dem zum Auffüllen dieses Messkolbens erforderlichen Chloroform ausgewaschen. Diese Probelösung wird der chromatographischen Bestimmung zugeführt.
5 Analytische Bestimmung
Das HPLC-Gerät wird gemäß Abschnitt 2.1 eingestellt (Eluentenfluss 1,3 ml/min). Dann werden jeweils 10 µl Probelösung und Kalibrierlösung injiziert. Das Retentionsvolumen des Ethylenimin-Derivats beträgt unter diesen Bedingungen 4,8 ml. Es werden die Peakhöhen oder Peakflächen ermittelt.
6 Berechnen des Analysenergebnisses
Es wird gegen einen externen Standard ausgewertet
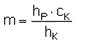
Es bedeuten:
| m | = Masse Ethylenimin in der Probelösung in µg, |
| hP | = Höhe oder Fläche des Ethylenimin-Derivat-Peaks der Probelösung, |
| hK | = Höhe oder Fläche des Ethylenimin-Derivat-Peaks derjenigen Kalibrierlösung, die der Höhe oder Fläche des Peaks der Probelösung am nächsten kommt, |
| cK | = Massenkonzentration der Kalibrierlösung an Ethyleniminäquivalenten in µg/10 ml. |
Die Ethylenimin-Konzentration der Probeluft ca in mg/m3 errechnet sich aus:
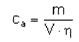
Für die Errechnung der Volumenkonzentration cV in ml/m3 aus ca gilt, wenn ca bezogen ist auf 20 °C und 1013 mbar:
cV = 0,56 * ca
Es bedeuten:
| Ca | = Massenkonzentration von Ethylenimin in der Probeluft in mg/m3 |
| cV | = Volumenkonzentration von Ethylenimin in der Probeluft in ml/m3 (ppm), |
| m | = Masse an Ethylenimin in der Probelösung in µg, |
| V | = Probeluftvolumen in l, |
| η | = Wiederfindungsrate (siehe Abschnitt 7.5). |
7 Beurteilung des Verfahrens
7.1 Reproduzierbarkeit
Chromatographische Parameter, z.B. Retentionszeiten und Responsefaktoren, sind u.a. abhängig vom Typ der Trennsäule, d.h. Charge, Alter, Verwendungsdauer. Somit ist es erforderlich, vor neuen Analysen das System zu überprüfen und ggf. den Erfordernissen der Messaufgabe anzupassen.
7.2 Präzision
Die relative Standardabweichung für das Gesamtverfahren wurde bei einer Konzentration von 2 mg/m3 an Ethylenimin unter Laborbedingungen zu 10 % gefunden.
7.3 Nachweisgrenze
Unter den Bedingungen in der Praxis beträgt die absolute Nachweisgrenze für das Gesamtverfahren 10 ng Ethylenimin und die relative Nachweisgrenze 0,1 ml/m3 (ppm) 0,2 mg/m3 an Ethylenimin für 50 l Probeluft, 10 ml Extraktionslösung, 10 µl Injektionslösung.
7.4 Spezifität
Die Spezifität ist in jedem Einzelfall zu prüfen. Störungen ergeben sich nur durch Substanzen, die unter den chromatographischen Arbeitsbedingungen die gleiche Retentionszeit wie das Ethylenimin-Derivat sowie eine Extinktion bei der Messwellenlänge 254 nm aufweisen.
7.5 Wiederfindungsrate
Die Absorption des Ethylenimins in einer Waschflasche ist größer als 96 %. Es ist deshalb im allgemeinen nicht erforderlich, bei der Probenahme zwei Waschflaschen hintereinander zu schalten. Zur Reagenzlösung direkt zugegebenes Ethylenimin wurde zu ca. 90 % wiedergefunden. Bei dynamisch hergestellten Prüfgasen mit Konzentrationen zwischen 1 und 4 mg/m3 an Ethylenimin wurden ca. 80 % wiedergefunden. Soweit die eigene Überprüfung des Benutzers der Methode nicht anderes ergibt, sollte daher mit einer Wiederfindungsrate ηvon 0,8 gerechnet werden.
8 Hersteller
| Pumpe: | z.B. Compur Electronic GmbH, München, Du Pont Instruments, Vertrieb in Deutschland: DEHA-Haan & Wittmer GmbH, Friolzheim; |
| Kleinwaschflasche: | z.B. Compur Electronic GmbH, München; |
| HPLC-Gerät: | z.B. Hewlett Packard, Böblingen, Spectra Physics GmbH, Darmstadt, Varian GmbH, Darmstadt, Waters GmbH, Königstein. |
9 Literatur
Morales, R., Stampfer, J.F., Hermes, R.E.: Air Sampling and Liquid Chromatographic Determination of Ethylenimine. Anal. Chem. 54 (1982), S. 1340-1344.
________________
1 HPLC, engl.: High performance liquid chromatography.
 | ENDE | |
...
X
⍂
↑
↓
