 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. ▢ Regelwerk; BGI / DGUV-I |  |
BGI 505-39 / DGUV Information 213-539 - Verfahren zur Bestimmung von 4,4'-Diaminodiphenylmethan (4,4'-Methylendianilin, MDA)
Von den Berufsgenossenschaften anerkannte Analysenverfahren zur Feststellung der Konzentrationen krebserzeugender Arbeitsstoffe in der Luft in Arbeitsbereichen
Berufsgenossenschaftliche Informationen für Sicherheit und Gesundheit bei der Arbeit (BGI)
(bisherige ZH 1/120.39)
(Ausgabe 11/1994)
Erprobte und von den Berufsgenossenschaften anerkannte, diskontinuierliche Verfahren zur Bestimmung von 4,4'-Diaminodiphenylmethan in Arbeitsbereichen.
Es sind personenbezogene oder ortsfeste Probenahmen für Messungen zur Beurteilung von Arbeitsbereichen möglich:
1. Probenahme mit Pumpe und Abscheidung an imprägniertem Kieselgel, Photometrie nach Derivatisierung
"4,4'-Diaminodiphenylmethan - 1 - PHOT"
(Ausgabe:
Januar 1989, überarbeitet November 1994);
2. Probenahme mit Pumpe und Abscheidung auf einem imprägnierten Filter,
Arbeitsweise A:
Photometrie nach Derivatisierung
"4,4'-Diaminodiphenylmethan - 2 - PHOT"
(Ausgabe:
November 1994);
Arbeitsweise B:
Flüssigchromatographie (HPLC) 1 nach Elution
"4,4'-Diaminodiphenylmethan - 2 - HPLC"
(Ausgabe November 1994).
| IUPAC-Name: | 4,4'-Diaminodiphenylmethan |
| CAS-Nr.: | 101-77-9 |
1. Probenahme mit Pumpe und Abscheidung an imprägniertem Kieselgel, Photometrie nach Derivatisierung
Kurzfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration von 4,4'-Diaminodiphenylmethan im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
| Meßprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein Sammelröhrchen gesaugt, das mit Schwefelsäure imprägniertes Kieselgel enthält. Hierdurch wird 4,4'-Diaminodiphenylmethan als Sulfat gebunden. Das abgeschiedene 4,4'-Diaminodiphenylmethan wird eluiert und nach Diazotieren durch Zugabe eines Kupplungsreagenzes zu einem blauvioletten Azofarbstoff umgesetzt. Die analytische Bestimmung geschieht photometrisch. |
| Technische Daten | |
| Bestimmungsgrenze: | absolut: 2 µg 4,4'-Diaminodiphenylmethan bei 25 ml Meßlösung und 1 cm Küvetten Schichtdicke,
relativ: 0,025 mg/m3 an 4,4'-Diaminodiphenylmethan für 320 l Probeluft, 25 ml Meßlösung und 1 cm Küvettenschichtdicke. |
| Selektivität: | Die Selektivität ist in jedem Einzelfall zu prüfen. Primäre Arylamine und Arylisocyanate werden miterfaßt. Phenole können stören. |
| Vorteile: | Geringer apparativer Aufwand. |
| Nachteile: | Querempfindlichkeiten gegenüber anderen Arylaminen. |
| Apparativer Aufwand: | Pumpe, Gasmengenzähler oder Volumenstromanzeiger, Sammelröhrchen mit imprägniertem Kieselgel, Ausrüstung für die Photometrie. |
Ausführliche Verfahrensbeschreibung
1 Geräte, Chemikalien und Lösungen
1.1 Geräte
Für die Probenahme:
Probenahmegerät:
Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein Sammelröhrchen gesaugt, das mit Schwefelsäure imprägniertes Kieselgel enthält. Geeignet sind Probenahmegeräte, die Stäube gemäß Gesamtstaubdefinition mit einer Ansauggeschwindigkeit von 1,25 m/s ±10 % erfassen.
Es sind Pumpen einzusetzen, deren Förderleistung hinreichend unabhängig vom Druckabfall im Glasröhrchen ist.
Sammelröhrchen:
z.B. Glasröhrchen von 8 cm Länge, ca. 3,5 mm Innendurchmesser, ca. 6 mm Außendurchmesser.
Diese Röhrchen werden mit etwa 500 mg imprägniertem Kieselgel gefüllt (Herstellung siehe Abschnitt 1.2).
Für die Probenaufbereitung und analytische Bestimmung:
Glasgeräte: Vollpipetten oder Meßpipetten der Volumina 0,5 ml, 1 ml, 2 ml, 5 ml, 10 ml, 50 ml.
Meßkolben der Volumina 20 ml, 25 ml, 100 ml, 1000 ml.
Spektralphotometer oder Filterphotometer:
zur Extinktionsmessung bei 590 nm.Zur Messung mit einem Filterphotometer ist ein Absorptionsfilter oder Interferenzfilter anzuwenden, das eine ausreichend hohe Durchlässigkeit bei 590 nm hat.
Küvetten: Vierkantküvetten, z.B. 10 mm Schichtdicke.
1.2 Chemikalien und Lösungen
Schwefelsäure p.a., 96 %,
Kieselgel 60, Porendurchmesser 6 nm, Korngröße 0,2-0,5 mm,
Natriumnitrit p.a.,
Amidoschwefelsäure p.a.,
N-(1-Naphthyl)-ethylendiamindihydrochlorid p.a.,
Salzsäure, 25 %, p.a.,
Salzsäure c (HCl) = 1 mol/l, p.a.,
Ethanol, absolut p.a.,
4,4'-Diaminodiphenylmethan, Reinheit > 97 %.
Imprägniertes Kieselgel:
In einem Erlenmeyerkolben mit Schliffstopfen werden 50 g Kieselgel mit 10 g Schwefelsäure 96 % versetzt. Man schwenkt gelegentlich um und läßt über Nacht stehen.
Nitritlösung:
0,5 g Natriumnitrit in 100 ml Wasser gelöst. Frisch bereiten!
Amidoschwefelsäure-Lösung:
2 g Amidoschwefelsäure in 100 ml Wasser gelöst.
Kupplungsreagenz-Lösung:
500 mg N-(1-Naphthyl)-ethylendiamindihydrochlorid in 100 ml Wasser gelöst.Die Lösung muß lichtgeschützt aufbewahrt werden. Sie ist etwa 24 Stunden haltbar.
Kalibrierlösung:
Lösung von 5 µg 4,4'-Diaminodiphenylmethan/ml Wasser.In einem 1-l-Meßkolben werden 100 mg 4,4'-Diaminodiphenylmethan, auf 0,1 mg genau gewogen, mit 5 ml Salzsäure 25 % versetzt und nach vollständigem Lösen mit Wasser bis zur Marke aufgefüllt. Von dieser Lösung werden 50 ml entnommen und im Meßkolben mit Wasser auf 1000 ml aufgefüllt.
2 Probenahme
Ein Sammelröhrchen wird mit der Pumpe verbunden. Pumpe und Röhrchen werden von einer Person während der Arbeitszeit getragen oder ortsfest verwendet. Der Volumenstrom wird unter Beachtung der erforderlichen Ansauggeschwindigkeit und der Dimension des Sammelröhrchens (vgl. Abschnitt 1.1) auf ca. 40 l/h eingestellt. Die Probenahmezeit kann bis zu 8 Stunden entsprechend 320 L Probeluft betragen.
3 Probenaufbereitung und analytische Bestimmung
Das Sammelröhrchen wird mit 5 ml Salzsäure c (HCl) = 1 mol/l eluiert und das Fluat in einen 20-ml-Meßkolben überführt; der Kolben wird anschließend mit Wasser zur Marke aufgefüllt (Probelösung). 5 ml dieser Lösung werden in einem 25-ml-Meßkolben mit 2 ml Salzsäure c (HCl) = 1 mol/l und 0,5 ml Nitritlösung versetzt. Nach 10 Minuten gibt man zur Zerstörung des überschüssigen Nitrits 1 ml Amidoschwefelsäure-Lösung zu und schüttelt kräftig, um den freigesetzten Stickstoff aus der Lösung zu entfernen. Noch weiteren zwei Minuten gibt man 1 ml Kupplungsreagenz-Lösung hinzu. Man läßt die Lösung 10 Minuten bei Raumtemperatur stehen, fügt dann 1 ml Salzsäure 25 % hinzu und füllt den Meßkolben mit Ethanol zur Marke auf (Meßlösung).
Nach frühestens 15 Minuten und spätestens zwei Stunden wird die Lösung in eine 1-cm-Küvette gegeben und die Extinktion bei einer Wellenlänge von 590 nm gegen Wasser gemessen [1].
Bei Lösungen mit einer Extinktion über 0,5 besteht die Gefahr, daß der gebildete Farbstoff ausfällt. Solche Lösungen müssen vor der analytischen Bestimmung mit Ethanol weiter verdünnt werden.
Zur Ermittlung des Leerwertes wird ein nicht beaufschlagtes Sammelröhrchen wie oben beschrieben aufgearbeitet. Es werden drei Leerwerte bestimmt und hieraus der mittlere Leerwert errechnet.
4 Auswertung
4.1 Kalibrierung
In 25-ml-Meßkolben werden z.B. 0,5, 1, 2, 3, 4 und 5 ml der Kalibrierlösung (siehe Abschnitt 1.2) pipettiert, mit Wasser zu 5 ml ergänzt und jeweils 2 ml Salzsäure c (HCl) = 1 mol/l und 0,5 ml Nitritlösung hinzugegeben. Der weitere Gang der analytischen Bestimmung entspricht den Angaben in Abschnitt 3.
Zur Bestimmung des Kalibrierfaktors stellt man eine Kalibrierkurve für den Arbeitsbereich 2,5 bis 25 µg 4,4'-Diaminodiphenylmethan auf. Hierzu trägt man die mit der Kalibrierreihe ermittelten Extinktionen gegen die zugehörigen Massen auf. Man erhält eine lineare Kalibrierfunktion. Sie ist geprüft bis 0,5 Extinktionseinheiten.
Aus der Steigung der Kalibrierfunktion erhält man den methodenspezifischen Extinktionskoeffizienten, im weiteren Kalibrierfaktor (F) genannt (Extinktion für 1 mg Substanz, 1 ml Meßlösung und 1 cm Schichtdicke), nach der Formel
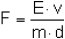 | (1) |
Es bedeuten:
| F | = Kalibrierfaktor (unter den genannten Arbeitsbedingungen F ca. 480), |
| E | = Extinktionen der Lösungen der Kalibrierreihe, vermindert um die mittlere Extinktion des Leerwertes, |
| v | = Volumen der Meßlösung in ml, |
| m | = Entsprechende Masse des 4,4'-Diaminodiphenylmethans in mg, |
| d | = Schichtdicke in cm. |
4.2 Berechnen des Analysenergebnisses
Die Berechnung der 4,4'-Diaminodiphenylmethan-Konzentration der Probeluft in mg/m3 erfolgt nach der Formel:
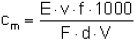 | (2) |
Es bedeuten:
| cm | = Massenkonzentration in mg/m3 an 4,4'-Diaminodiphenylmethan in der Probeluft, |
| E | = Extinktion der Meßlösung, vermindert um die mittlere Extinktion des Leerwertes, |
| v | = Volumen der Meßlösung in ml, |
| f | = Aliquotierungsfaktor nach Abschnitt 3 (f = 4), |
| F | = Kalibrierfaktor, |
| d | = Schichtdicke in cm, |
| V | = Probeluftvolumen in l. |
5 Beurteilung des Verfahrens
5.1 Genauigkeit
Zur Bestimmung der Standardabweichung wurden in 8 Sammelröhrchen mit Hilfe einer Mikropipette je 20 µl einer Lösung gegeben, die 3 mg 4,4'-Diaminodiphenylmethan in 1 ml Methanol enthielt. Anschließend wurden durch die Sammelröhrchen je 140 l Luft geleitet.
Die relative Standardabweichung des Analysenverfahrens ergab sich zu 2,5 %, ermittelt aus 8 Einzelmessungen für die Konzentration 0,4 mg/m3 an 4,4'-Diaminodiphenylmethan ( 60 µg je Sammelröhrchen) bei 140 l Luft.
60 µg je Sammelröhrchen) bei 140 l Luft.
5.2 Bestimmungsgrenze
Die absolute Bestimmungsgrenze beträgt 2 µg 4,4'-Diaminodiphenylmethan (5 ml von 20 ml Probelösung in 25 ml Meßlösung, 1 cm Küvettenschichtdicke).
Die relative Bestimmungsgrenze beträgt bei einem Volumenstrom von 40 l/h 0,025 mg/m3 an 4,4'-Diaminodiphenylmethan für 320 l Probeluft, 25 ml Meßlösung, 1 cm Küvettenschichtdicke.
Eine Senkung der Bestimmungsgrenze ist möglich bei Verwendung von Küvetten mit größerer Schichtdicke, z.B. 4 cm, oder Änderung der Aliquotierung.
5.3 Selektivität
Primäre Arylamine werden miterfaßt. Phenole und aromatische Isocyanate können stören.
Alkylamine sowie sekundäre und tertiäre Arylamine bilden keine Azofarbstoffe.
5.4 Wiederfindungsrate
Zur Bestimmung der Wiederfindungsrate wurden Sammelröhrchen mit 180 µg 4,4'-Diaminodiphenylmethan durch Verdampfen im Luftstrom beaufschlagt und insgesamt 140 l Luft durch die Röhrchen gesaugt. Aufarbeitung und analytische Bestimmung erfolgten entsprechend den Angaben in Abschnitt 3.
Bei diesen Versuchen ergab sich eine Wiederfindung über 95 %.
6 Literatur
[1] Kakác, B., Vejdelek, Z. J.: Handbuch der photometrischen Analyse organischer Verbindungen, Verlag Chemie GmbH, Weinheim (1974).
2. Probenahme mit Pumpe und Abscheidung auf einem imprägnierten Filter
Arbeitsweise A: Photometrie nach Derivatisierung
Arbeitsweise B: Flüssigchromatographie (HPLC) nach Elution
Kurzfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration von 4,4'-Diaminodiphenylmethan im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
| Meßprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein mit Schwefelsäure imprägniertes Glasfaserfilter gesaugt. Arbeitsweise A: Das abgeschiedene 4,4'-Diaminodiphenylmethan wird mit Salzsäure eluiert und nach Diazotieren durch Zugabe eines Kupplungsreagenzes zu einem blauvioletten Azofarbstoff umgesetzt. Die analytische Bestimmung geschieht photometrisch. Arbeitsweise B: Das abgeschiedene 4,4'-Diaminodiphenylmethan wird mit Wasser eluiert und flüssigchromatographisch bestimmt. | |
| Technische Daten | ||
| Bestimmungsgrenze: | ||
| Arbeitsweise A: | ||
| absolut: | 2 µg 4,4'-Diaminodiphenylmethan bei 25 ml Meßlösung und 1 cm Küvetten-Schichtdicke. | |
| relativ: | 0,008 mg/m3 an 4,4'-Diaminodiphenylmethan für 500 l Probeluft, 25 ml Meßlösung und 1 cm Küvetten-Schichtdicke. | |
| Arbeitsweise B: | ||
| absolut: | 0,05 µg 4,4'-Diaminodiphenylmethan. | |
| relativ: | 0,008 mg/m3 an 4,4'-Diaminodiphenylmethan bei 500 l Probeluft, 4 ml Elutionslösung und 50 µl Injektionsvolumen. | |
| Selektivität | Bei Arbeitsweise A werden andere primäre Aryl amine und Arylisocyanate miterfaßt. Phenole können stören. Bei Arbeitsweise B ist die Selektivität in jedem Einzelfall zu prüfen. | |
| Vorteile: | Personenbezogene Messung möglich, Arbeitsweise A: geringer apparativer Aufwand, Arbeitsweise B: selektive Messungen möglich. | |
| Nachteile: | Keine Anzeige von Konzentrationsspitzen. Bei Arbeitsweise A Querempfindlichkeiten gegenüber anderen Arylaminen und Arylisocyanaten. | |
| Apparativer Aufwand: | ||
| Pumpe mit Gasmengenzähler oder Volumenstromanzeiger, sauer imprägniertes Glasfaserfilter mit Filterhalter, Arbeitsweise A: Arbeitsweise B: | ||
Ausführliche Verfahrensbeschreibung
Arbeitsweise A: Photometrie
A 1 Geräte, Chemikalien und Lösungen
A 1.1 Geräte
Für die Probenahme:
- Pumpe mit Volumenstromanzeiger oder Gasmengenzähler, geeignet für einen Volumenstrom von 3,5 l/min,
- Probenahmekopf GSP, z.B. Firma Ströhlein GmbH, Kaarst, oder Firma DEHA-Haan & Wittmer GmbH, Friolzheim,
- Glasfaserfilter, z.B. No. 6, Firma Schleicher und Schüll.
Für die Probenaufbereitung und analytische Bestimmung:
- Meßpipetten oder Vollpipetten: 0,5 ml, 1 ml, 2 ml, 5 ml und 50 ml,
- Meßkolben: 25 ml, 100 ml und 1000 ml,
- Erlenmeyerkolben mit Schliff: 50 ml,
- Ultraschallbad,
- Trockenschrank,
- Exsikkator,
- Spektralphotometer oder Filterphotometer:
Zur Extinktionsmessung bei 590 nm.
Zur Messung mit einem Filterphotometer ist ein Absorptionsfilter oder Interferenzfilter anzuwenden, das eine ausreichend hohe Durchlässigkeit bei 590 nm hat. - Küvetten: Vierkantküvetten, 10 mm Schichtdicke.
A 1.2 Chemikalien und Lösungen
Schwefelsäure c (H2SO4) = 0,5 mol/l, p.a.,
Natriumnitrit p.a.,
Amidoschwefelsäure p.a.,
N-(1-Naphthyl)-ethylendiamindihydrochlorid p.a.,
Salzsäure 25 %, p.a.,
Salzsäure c (HCl) = 1 mol/l, p.a.,
Ethanol, absolut, p.a.,
4,4'-Diaminodiphenylmethan, Reinheit > 97 %.
Nitritlösung:
0,5 g Natriumnitrit in 100 ml Wasser gelöst. Frisch bereiten!
Amidoschwefelsäure-Lösung:
2 g Amidoschwefelsäure in 100 ml Wasser gelöst.
Kupplungsreagenz-Lösung:
500 mg N-(1-Naphthyl)-ethylendiamindihydrochlorid in 100 ml Wasser gelöst.Die Lösung muß lichtgeschützt aufbewahrt werden. Sie ist etwa 24 Stunden haltbar.
Kalibrierlösung:
Lösung von 5 µg 4,4'-Diaminodiphenylmethan/ml Wasser.In einem 1-l-Meßkolben werden 100 mg 4,4'-Diaminodiphenylmethan, auf 0,1 mg genau gewogen, mit 5 ml Salzsäure 25 % versetzt und nach vollständigem Lösen mit Wasser bis zur Marke aufgefüllt. Von dieser Lösung werden 50 ml entnommen und mit Wasser auf 1000 ml aufgefüllt.
A 1.3 Imprägnierung der Filter
Die Glasfaserfilter werden in die Schwefelsäure eingetaucht, danach 30 Minuten an der Luft vorgetrocknet und anschließend im Trockenschrank bei 40 °C vollständig getrocknet. Die imprägnierten Filter werden im Exsikkator gelagert und sind etwa acht Wochen haltbar.
A 2 Probenahme
Zur Probenahme wird der Probenahmekopf mit einem sauer imprägnierten Glasfaserfilter bestückt und mit der Pumpe verbunden. Pumpe und Filterhalter werden von einer Person während der Arbeitszeit getragen oder ortsfest aufgestellt. Der Volumenstrom wird auf 3,5 l/min eingestellt, damit an der Eintrittsöffnung gemäß Gesamtstaubdefinition eine Strömungsgeschwindigkeit von 1,25 m/s gewährleistet ist. Das Meßverfahren wurde bis zu einem Probeluftvolumen von 525 L geprüft. Das entspricht einer Probenahmedauer von zweieinhalb Stunden.
A 3 Probenaufbereitung und analytische Bestimmung
Zur Aufbereitung wird das Filter in einen 50-ml-Erlenmeyerkolben mit Schliff gegeben, mit 4,0 ml Salzsäure c (HCl) = 1 mol/l versetzt und 15 Minuten im Ultraschallbad behandelt. Anschließend werden 2,0 ml der Lösung in einen 25-ml-Meßkolben pipettiert und nacheinander 5 ml Wasser und 0,5 ml Nitritlösung zugegeben. Nach 10 Minuten gibt man zur Zerstörung des überschüssigen Nitrits 1 ml Amidoschwefelsäure-Lösung zu und schwenkt um, damit der freigesetzte Stickstoff aus der Lösung entweichen kann. Nach weiteren 2 Minuten gibt man 1 ml Kupplungsreagenz-Lösung hinzu. Man läßt die Lösung 10 Minuten bei Raumtemperatur stehen, fügt dann 1 ml Salzsäure 25 % hinzu und füllt den Meßkolben mit Ethanol bis zur Marke auf (Meßlösung).
Nach frühestens 15 Minuten und spätestens 2 Stunden wird die Lösung in eine 1-cm-Küvette gegeben und die Extinktion bei einer Wellenlänge von 590 nm gegen Wasser gemessen [1].
Bei Lösungen mit einer Extinktion über 0,5 besteht die Gefahr, daß der gebildete Farbstoff ausfällt. Solche Lösungen müssen vor der Herstellung der Meßlösung mit Ethanol weiter verdünnt werden.
Zur Bestimmung des Leerwertes wird ein unbeladenes, imprägniertes Filter wie oben beschrieben aufgearbeitet. Es werden 3 Leerwerte bestimmt und hieraus der mittlere Leerwert errechnet.
A 4 Auswertung
A 4.1 Kalibrierung
In 25-ml-Meßkolben werden z.B. 0,5, 1, 2, 3, 4 und 5 ml der Kalibrierlösung (siehe Abschnitt A 1.2) pipettiert, mit Wasser zu 5 ml ergänzt und jeweils 2 ml Salzsäure c (HCl) = 1 mol/l und 0,5 ml Nitritlösung hinzugegeben. Es wird weiter verfahren wie in Abschnitt A 3 beschrieben.
Zur Bestimmung des Kalibrierfaktors stellt man eine Kalibrierkurve für den Arbeitsbereich 2,5 bis 25 µg 4,4'-Diaminodiphenylmethan auf. Hierzu trägt man die mit der Kalibrierreihe ermittelten Extinktionen gegen die zugehörigen Massen auf. Man erhält eine lineare Kalibrierfunktion. Sie ist geprüft bis 0,5 Extinktionseinheiten.
Aus der Steigung der Kalibrierfunktion erhält man den methodenspezifischen Extinktionskoeffizienten, im weiteren Kalibrierfaktor (F) genannt (Extinktion für 1 mg Substanz, 1 ml Meßlösung und 1 cm Schichtdicke), nach der Formel:
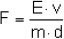 | (1) |
Es bedeuten:
| F | = Kalibrierfaktor (unter unseren Arbeitsbedingungen F ca. 480), |
| E | = Extinktionen der Lösungen der Kalibrierreihe, vermindert um die mittlere Extinktion des Leerwertes, |
| v | = Volumen der Meßlösung in ml, |
| m | = Entsprechende Masse des 4,4'-Diaminodiphenylmethans in mg, |
| d | = Schichtdicke in cm. |
A 4.2 Berechnen des Analysenergebnisses
Die Berechnung der Konzentration an 4,4'-Diaminodiphenylmethan in der Probeluft in mg/m3 erfolgt nach der Formel:
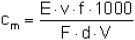 | (2) |
Es bedeuten:
| cm | = Massenkonzentration in mg/m3 von 4,4'-Diaminodiphenylmethan in der Probeluft, |
| E | = Extinktion der Meßlösung, vermindert um die mittlere Extinktion des Leerwertes, |
| v | = Volumen der Meßlösung in ml, |
| f | = Aliquotierungsfaktor nach Abschnitt 3 (f = 2), |
| F | = Kalibrierfaktor, |
| d | = Schichtdicke in cm, |
| V | = Probeluftvolumen in l. |
A 5 Beurteilung des Verfahrens
A 5.1 Genauigkeit
Mit Hilfe einer Mikropipette wurden jeweils 5 µg, 25 µg und 50 µg 4,4'-Diaminodiphenylmethan auf je ein imprägniertes Glasfaserfilter aufgebracht. Anschließend wurden 500 l Laborluft wie unter Abschnitt A 2 beschrieben durch die Filter gesaugt. Die dotierten Mengen an 4,4'-Diaminodiphenylmethan entsprechen Konzentrationen von 10, 50 und 100 µg/m3. Die Filter wurden anschließend wie unter Abschnitt 3 beschrieben analysiert. Für jede Konzentration wurden sechs Filter eingesetzt. Es ergaben sich relative Standardabweichungen von 3,2 %, 1,1 % und 1,7 %. Die Wiederfindung lag über 95 %.
A 5.2 Bestimmungsgrenze
Die absolute Bestimmungsgrenze beträgt 2 µg 4,4'-Diaminodiphenylmethan bei 25 ml Meßlösung und 1 cm Küvetten-Schichtdicke.
Die relative Bestimmungsgrenze beträgt 0,008 mg/m3 für ein Probeluftvolumen von 500 l, 25 ml Meßlösung und 1 cm Küvetten-Schichtdicke.
A 5.3 Selektivität
Primäre Arylamine und aromatische Isocyanate werden miterfaßt. Phenole können stören.
Alkylamine sowie sekundäre und tertiäre Arylamine bilden keine Azofarbstoffe.
A 6 Bemerkungen
Aufgrund des Miterfassens von aromatischen Aminen und aromatischen Isocyanaten muß dieses Verfahren als Summenverfahren betrachtet werden. Zur Erhöhung der Selektivität kann das Verfahren "4,4'-Diaminodiphenylmethan-2-HPLC" herangezogen werden.
Die Lagerfähigkeit der beaufschlagten Filter beträgt bei Raumtemperatur mindestens drei Wochen.
A 7 Literatur
[1] Kakác, B., Vejdelek, Z. J.: Handbuch der photometrischen Analyse organischer Verbindungen, Verlag Chemie GmbH, Weinheim (1974).
Arbeitsweise B: Flüssigchromatographie
B 1 Geräte, Chemikalien und Lösungen
B 1.1 Geräte
- Pumpe mit Volumenstromanzeiger oder Gasmengenzähler, geeignet für einen Volumenstrom von 3,5 l/min,
- Probenahmekopf GSP, z.B. Firma Ströhlein GmbH, Kaarst, oder Firma DEHA-Haan & Wittmer GmbH, Friolzheim,
- Glasfaserfilter, z.B. No. 6, Firma Schleicher und Schüll,
- Meßkolben: 10 ml, 100 ml und 1000 ml,
- Variable Dosierpipetten: 5 µl bis 1 ml,
- Probengläschen,
- PTFE 2 -Spritzenvorsatzfilter, z.B. Firma Millipore Millex FG 13, 0,2 µm,
- Einmalspritzen: 2,5 ml,
- HPLC-Gerät mit Gradientenpumpensteuerung und UV-Detektor,
- Registrier- und Auswerteeinheit,
- Wasseraufbereitungsgerät, z.B. Elgastat, Firma Elga, Vertrieb in Deutschland: Firma Labotec, Wiesbaden,
- Schnappdeckelgläschen,
- Ultraschallbad.
B 1.2 Chemikalien und Lösungen
- 4,4'-Diaminodiphenylmethan, Reinheit > 97 %,
- Wasser für die HPLC, z.B. mit dem Elgastat aufbereitet (UHQ-Wasser),
- Methanol, z.B. LiChrosolv, Firma Merck,
- Kaliumbihydrogenphosphat, p.a.,
- Schwefelsäure c (H2SO4) = 0,5 mol/l, p.a.,
- Pufferlösung:
Kaliumdihydrogenphosphatlösung
c (KH2PO4) = 30 mmol/l.
4,1 g Kaliumdihydrogenphosphat werden in 1 l UHQ-Wasser gelöst. - Stammlösung:
Lösung von 2 mg 4,4'-Diaminodiphenylmethan/ml Methanol.
In einen 50-ml-Meßkolben werden 100 mg 4,4'-Diaminodiphenylmethan auf 0,1 mg genau eingewogen und mit Methanol bis zur Marke aufgefüllt. - Kalibrierlösungen:
Lösungen von 1,0; 2,0; 4,0; 12; 24 und 40 µg 4,4'-Diaminodiphenylmethan/ml Wasser-Methanol-Gemisch.
Es werden 5; 10; 20; 60; 120 und 200 µl der Stammlösung in jeweils einem 10 ml-Meßkolben vorgelegt und mit einem Gemisch aus gleichen Teilen UHQ Wasser und Methanol (v/v) bis zur Marke aufgefüllt. Mit diesen Lösungen wird bei einem Probeluftvolumen von 500 L ein Konzentrationsbereich von 0,008 bis 0,32 mg/m3 abgedeckt.
B 1.3 Imprägnierung des Filters
Die Glasfaserfilter werden in die Schwefelsäure eingetaucht, danach 30 Minuten an der Luft vorgetrocknet und anschließend im Trockenschrank bei 40 °C vollständig getrocknet. Die imprägnierten Filter werden im Exsikkator gelagert und sind etwa acht Wochen haltbar.
B 2 Probenahme
Zur Probenahme wird der Probenahmekopf mit einem sauer imprägnierten Glasfaserfilter bestückt und mit der Pumpe verbunden. Pumpe und Filterhalter werden von einer Person während der Arbeitszeit getragen oder ortsfest aufgestellt. Die Volumenstrom wird auf 3,5 l/min eingestellt, damit an der Eintrittsöffnung gemäß Gesamtstaubdefinition eine Strömungsgeschwindigkeit von 1,25 m/s gewährleistet ist.
Das Meßverfahren wurde bis zu einem Probeluftvolumen von 525 L geprüft. Das entspricht einer Probenahmedauer von zweieinhalb Stunden.
B 3 Analytische Bestimmung
B 3.1 Probenaufbereitung und Analyse
Zur Aufbereitung wird das Filter in ein Schnappdeckelgläschen gegeben und mit 4 ml UHQ-Wasser versetzt. Nach der anschließenden 15-minütigen Behandlung im Ultraschallbad werden die festen Bestandteile mit einem PTFE-Spritzenvorsatzfilter von der Flüssigkeit abgetrennt (Elutionslösung).
Um sicherzustellen, daß das zur Elution verwendete Wasser und das Glasfaserfilter keine störenden Verunreinigungen enthalten, wird ein unbeladenes, imprägniertes Filter mit 4 ml Wasser desorbiert (Leerwertlösung).
Aus der Elutionslösung werden 50 µl in den Flüssigchromatographen eingespritzt und ein Chromatogramm wie unter Abschnitt B 3.2 beschrieben, angefertigt. Das 4,4'-Diaminodiphenylmethan wird bei einer Wellenlänge von 240 nm detektiert.
B 3.2 Instrumentelle Arbeitsbedingungen
Die in Abschnitt B 5 angegebenen Verfahrenskenngrößen wurden unter folgenden Gerätebedingungen erarbeitet.
| Gerät: | Hewlett Packard 1090 mit Diodenarray Detektor (DAD) und Autosampler. |
| Trennsäule: | LiChroCART-Kartusche (Länge 250 mm, Innendurchmesser 4 mm) mit LiChros-pher 100 RP-18 (5 µm) und mit einer Vorsäule (Länge 4 mm, Innendurchmesser 4 mm) mit dem gleichen Packungsmaterial, Firma Merck, Darmstadt. |
| Mobile Phase: | Gradientenelution. Zu Beginn Mischung aus 50 Volumenteilen Pufferlösung und 50 Volumenteilen Methanol; der Anteil an Methanol wird in 20 Minuten kontinuierlich auf 100 % gesteigert. |
| Flußrate: | 0,5 ml/min. |
| Einspritzvolumen: | 50 µl. |
| Meßwellenlänge: | 240 nm. |
| Ofentemperatur: | 40 °C. |
B 4 Auswertung
B 4.1 Kalibrierung
Von den unter Abschnitt B 1.2 beschriebenen Kalibrierlösungen werden je 50 µl in das Analysengerät injiziert. Durch Auftragen der ermittelten Flächen über den in den jeweiligen Kalibrierlösungen enthaltenen Konzentrationen an 4,4'-Diaminodiphenylmethan wird die Kalibrierkurve erstellt und die Linearität überprüft. Im angegebenen Konzentrationsbereich ist die Kalibrierkurve eine Gerade.
Der Kalibrierfaktor f wird mit Hilfe der erhaltenen Peakflächen von 4,4'-Diaminodiphenylmethan aus den unterschiedlichen Kalibrierlösungen nach Formel (1) ermittelt:
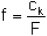 | (1) |
Es bedeuten:
| f | = Kalibrierfaktor, |
| cK | = Konzentration von 4,4'-Diaminodiphenylmethan in µg/ml in der Kalibrierlösung, |
| F | = Peakfläche des 4,4'-Diaminodiphenylmethans. |
Der Kalibrierfaktor ist für alle Verdünnungen ungefähr gleich. Der Mittelwert̄f ist für die Berechnung des Analysenergebnisses zu verwenden.
B 4.2 Berechnen des Analysenergebnisses
Die Berechnung der 4,4'-Diaminodiphenlymethankonzentration in der Probeluft in mg/m3 erfolgt nach der Formel (2)
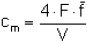 | (2) |
Es bedeuten:
| cm | = Massenkonzentration in mg/m3 an 4,4'-Diaminodiphenylmethan in der Probeluft, |
| F | = Peakfläche des 4,4'-Diaminodiphenylmethans aus der Elutionslösung, |
| ̄f | = mittlerer Kalibrierfaktor für 4,4'-Diaminodiphenylmethan, |
| V | = Probeluftvolumen in l. |
B 5 Beurteilung des Verfahrens
B 5.1 Genauigkeit
Mit Hilfe einer Mikropipette wurden jeweils 2,5 µl, 25 µl und 50 µl der unter Abschnitt B 1.2 beschriebenen Stammlösung auf je ein imprägniertes Glasfaserfilter aufgebracht. Anschließend wurden 500 l Laborluft wie unter Abschnitt B 2 beschrieben durch die Filter gesaugt. Die dotierten Mengen an 4,4'-Diaminodiphenylmethan entsprechen beim untersuchten Probeluftvolumen Konzentrationen von 0,01; 0,1 und 0,2 mg/m3. Nach 24-stündiger Lagerung wurden die Filter wie unter Abschnitt B 3 beschrieben analysiert. Für jede Konzentration wurden sechs Filter eingesetzt. Für die untersuchten Konzentrationen ergaben sich relative Standardabweichungen von 4,9; 0,9 und 1,3 %.
Bei einem Probeluftvolumen von 525 l lag die Wiederfindung bei 87 %.
B 5.2 Bestimmungsgrenze
Die absolute Bestimmungsgrenze beträgt 0,05 µg 4,4'-Diaminodiphenylmethan.
Die relative Bestimmungsgrenze beträgt 0,008 mg/m3 für ein Probeluftvolumen von 525 l, 4 ml Desorptionslösung und 50 µl Injektionsvolumen.
B 5.3 Selektivität
Die Selektivität ist in jedem Einzelfall zu prüfen.
B 6 Bemerkungen
Die Lagerfähigkeit der beaufschlagten Filter beträgt bei Raumtemperatur mindestens drei Wochen.
Mit dem beschriebenen Verfahren können neben 4,4'-Diaminodiphenylmethan auch 3,3,-Dimethyl-4,4'-diaminodiphenylmethan, o-Toluidin und Anilin in der Luft am Arbeitsplatz bestimmt werden. Bei Probeluftvolumina bis zu 500 l beträgt die Wiederfindung bis zu 80 %.
___________
1 HPLC, engl.: High Performance Liquid Chromatography.
2 Polytetrafluorethylen
 | ENDE |  |
...
X
⍂
↑
↓
