 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. ▢ Regelwerk; BGI / DGUV-I |
BGI 505-60 / DGUV Information 213-560 - Verfahren zur Bestimmung von Dinitrotoluolen
Von den Berufsgenossenschaften anerkannte Analysenverfahren zur Feststellung der Konzentrationen krebserzeugender Arbeitsstoffe in der Luft in Arbeitsbereichen
Berufsgenossenschaftliche Informationen für Sicherheit und Gesundheit bei der Arbeit (BGI)
(bisherige ZH 1/120.60)
(Ausgabe 02/1996)
Erprobtes und von den Berufsgenossenschaften anerkanntes, diskontinuierliches Verfahren zur Bestimmung von Dinitrotoluolen in Arbeitsbereichen.
Es sind personenbezogene oder ortsfeste Probenahmen für Messungen zur Beurteilung von Arbeitsbereichen möglich:
| 1. | Probenahme mit Pumpe und Adsorption an Tenax, Gaschromatographie nach Desorption. "Dinitrotoluole - 1 - GC" (Ausgabe: Februar 1996). |
| IUPAC-Name: | CAS-Nr.: |
| 1-Methyl-2,3-dinitrobenzol | 602-01-7 |
| 1-Methyl-2,4-dinitrobenzol | 121-14-2 |
| 1-Methyl-2,6-dinitrobenzol | 606-20-2 |
| 1-Methyl-3,4-dinitrobenzol | 610-39-9 |
| 1-Methyl-3,5-dinitrobenzol | 618-85-9 |
1. Probenahme mit Pumpe und Adsorption an Tenax, Gaschromatographie nach Desorption
Kurzfassung
Mit diesem Verfahren wird die über die Probenahmedauer gemittelte Konzentration der isomeren Dinitrotoluole (DNT) im Arbeitsbereich personenbezogen oder ortsfest bestimmt.
| Messprinzip: | Mit Hilfe einer Pumpe wird ein definiertes Luftvolumen durch ein Tenax-Röhrchen gesaugt. Die Dinitrotoluole sind bei Raumtemperatur Feststoffe. Daher ist bei der Probenahme die Gesamtstaubdefinition zu beachten. Die adsorbierten Dinitrotoluole werden mit Aceton desorbiert und gaschromatographisch bestimmt. |
| Technische Daten | |
| Bestimmungsgrenze: | absolut: 12 pg für jedes DNT-Isomer,
relativ: 1 µg/m3 an dem jeweiligen DNT-Isomer für 60 l Probeluft, 5 ml Desorptionslösung und 1 µl Injektionsvolumen. |
| Selektivität: | Infolge Störkomponenten zu hohe Werte möglich. Störeinflüsse sind im allgemeinen durch Wahl einer anderen Trennsäule eliminierbar. |
| Vorteile: | Personenbezogene und selektive Messungen möglich. |
| Nachteile: | Keine Anzeige von Konzentrationsspitzen. |
| Apparativer Aufwand: | Pumpe mit Gasmengenzähler oder Volumenstromanzeiger, Tenax-Röhrchen, Gaschromatograph mit Elektroneneinfangdetektor (ECD). |
Ausführliche Verfahrensbeschreibung
1 Geräte, Chemikalien und Lösungen
1.1 Geräte
Für die Probenahme:
- Pumpe, geeignet für einen Volumenstrom von 1 ml/min,
z.B. S 2500 der Firma DuPont Instruments (Vertrieb in Deutschland: DEHA-Haan & Wittmer GmbH, Friolzheim), - Gasmengenzähler oder Volumenstromanzeiger,
- Adsorptionsröhrchen mit Tenax (standardisiert, bestehend aus zwei durch Glaswolle getrennte Tenaxfüllungen von ca. 50 mg und 100 mg),
z.B. der Firma SKC (Vertrieb in Deutschland: MTC-GmbH, Müllheim; Katalog-Nr. 226-35-03), - Verschlusskappen für die geöffneten Tenax-Röhrchen.
Für die Probenaufbereitung und Analyse: - Probengefäße, braun, mit Verschlusskappe aus Aluminium mit PTFE 1 -kaschiertem Septum 2 ml, 5 ml,
- Verschlusszange,
- Schüttelmaschine,
- Messkolben, 5 ml, 10 ml,
- Mikroliterspritzen 5 µl, 10 µl, 25 µl, 50 µl, 100 µl,
- Gaschromatograph mit ECD,
- Auswerteeinheit.
1.2 Chemikalien und Lösungen
1-Methyl-2,3-dinitrobenzol (2,3-DNT):
Reinheit mind. 99 %, z.B. Riedel-de Haen AG, Seelze,
1-Methyl-2,4-dinitrobenzol (2,4-DNT):
Reinheit mind. 99 %, z.B. Merck KGaA, Darmstadt,
1-Methyl-2,6-dinitrobenzol (2,6-DNT):
Reinheit mind. 99 %, z.B. Riedel-de Haen AG, Seelze,
1-Methyl-3,4-dinitrobenzol (3,4-DNT):
Reinheit mind. 99 %, z.B. Aldrich-Chemie, Stuttgart,
1-Methyl-3,5-dinitrobenzol (3,5-DNT):
Reinheit mind. 99 %, z.B. Promochem GmbH, Wesel,
1,2-Dinitrobenzol:
Reinheit mind. 99 % (interner Standard),
z.B. Riedel-de Haen AG, Seelze.
Desorptionsmittel: Aceton.
DNT-Stammlösung I:
Lösung von 50 mg der jeweiligen DNT-Isomeren in 10 ml Aceton.
In einen 10-ml-Messkolben werden ca. 50 mg der jeweiligen DNT-Isomeren auf 0,01 mg genau eingewogen.
Anschließend wird der Messkolben mit Aceton bis zur Marke aufgefüllt.
DNT-Stammlösung II:
Lösung von 1,25 mg der jeweiligen DNT-Isomeren in 10 ml Aceton.
250 µl der Stammlösung I werden in einen 10-ml-Messkolben, in dem Aceton vorgelegt wurde, überführt. Anschließend wird der Messkolben mit Aceton bis zur Marke aufgefüllt.
Interne Standardlösung I:
Lösung von 200 mg 1,2-Dinitrobenzol in 10 ml Aceton.
In einen 10-ml-Messkolben werden ca. 200 mg 1,2-Dinitrobenzol auf 0,01 mg genau eingewogen und mit Aceton bis zur Marke aufgefüllt.
Interne Standardlösung II:
Lösung von 2 mg 1,2-Dinitrobenzol in 10 ml Aceton.
In einen 10-ml-Messkolben werden einige Milliliter Aceton vorgelegt und 100 µl der internen Standardlösung I hinzugefügt. Anschließend wird mit Aceton bis zur Marke aufgefüllt.
DNT-Kalibrierlösungen:
Lösungen von 0,25 µg, 0,63 µg, 1,25 µg, 2,5 µg, 5,0 µg, und 7,5 µg eines jeden DNT-Isomeren und jeweils 1 µg 1,2-Dinitrobenzol in 5 ml Aceton.
In einen 5-ml-Messkolben werden einige Milliliter Aceton vorgelegt und jeweils 2 µl, 5 µl, 10 µl, 20 µl, 40 µl und 60 µl der DNT-Stammlösung II hinzugefügt. Anschließend werden jeweils 5 µl der internen Standardlösung II zugegeben und der Messkolben bis zur Marke aufgefüllt. Mit diesen Lösungen wird bei einem Probeluftvolumen von 60 l ein Konzentrationsbereich von 4 µg/m3 bis 125 µg/m3 an den jeweiligen DNT-Isomeren abgedeckt.
Gase zum Betrieb des Gaschromatographen:
Helium, Reinheit geeignet zum Betrieb eines ECD,
Stickstoff, Reinheit geeignet zum Betrieb eines ECD.
2 Probenahme
Die Schmelzpunkte der Dinitrotoluole liegen in dem Bereich von 50 bis 70 °C. Sie können als partikelförmig in dem zu untersuchenden Arbeitsbereich auftreten. Bei der Probenahme ist daher die Gesamtstaubdefinition zu berücksichtigen. Dies geschieht mit Probenahmesystemen, bei denen die geforderte Ansauggeschwindigkeit 1,25 m/s +10 % eingestellt werden kann. Die Ansauggeschwindigkeit kann bei der Probenahme der Dinitrotoluole beispielsweise durch Vorschalten einer Glassonde (Länge 3-4 cm, Glas auf Glas) von definiertem Innendurchmesser (z.B. 3 mm) und entsprechend eingestelltem Volumenstrom (z.B. 0,5 l/min) erreicht werden.
Ein Tenax-Röhrchen wird geöffnet und mit der Pumpe verbunden. Pumpe und Röhrchen werden von einer Person während der Arbeitszeit getragen oder ortsfest verwendet. Nach Beendigung der Probenahme wird das Röhrchen mit den Verschlusskappen dicht verschlossen. Das Verfahren wurde bei einem Probeluftvolumen von 60 l und einem Volumenstrom von 0,5 l/min überprüft.
3 Analytische Bestimmung
3.1 Probenaufbereitung und Analyse
Der gesamte Inhalt des beladenen Tenax-Röhrchens wird in ein 5-ml-Probengefäß gegeben. Nach dem Zusatz von 5 ml Aceton und 5 µl der internen Standardlösung II wird das Gefäß verschlossen und 1 h vorsichtig geschüttelt. Danach wird die überstehende Lösung in ein 2-ml-Probengefäß überführt und dieses ebenfalls verschlossen. Um sicherzustellen, dass das verwendete Aceton und Tenax keine störenden Verunreinigungen enthalten, wird die Füllung eines unbeladenen Röhrchens - wie zuvor beschrieben - behandelt (Leerwertlösung).
Jeweils 1 µl der Desorptionslösung und der Leerwertlösung werden in den Gaschromatographen eingespritzt und ein Gaschromatogramm, wie unter Abschnitt 3.2 beschrieben, angefertigt.
Die quantitative Auswertung erfolgt nach der Methode des internen Standards.
3.2 Gaschromatographische Arbeitsbedingungen
Die in Abschnitt 5 angegebenen Verfahrenskenngrößen wurden unter folgenden Gerätebedingungen erarbeitet:
| Gerät: | Gaschromatograph Hewlett-Packard 5890 mit ECD, Split/Splitless-Injektor und automatischem Probengeber HP 7673. |
| Trennsäule: | Quarzkapillare, stationäre Phase Rtx-200 der Firma Restek, Länge 30 m, Innendurchmesser 0,25 mm, Filmdicke 0,25 µm. |
| Temperaturen: | Injektor: 250 °C, Ofen: Anfangstemperatur: 80 °C, 2 min isotherm, Heizrate 1: 3 °C/min bis 120 °C, 10 min isotherm, Heizrate 2: 3 °C/min bis 260 °C, Endtemperatur: 260 °C, 5 min isotherm. Detektor: 300 °C. |
| Injektionsart: | split, |
| Split: | 20 ml/min, |
| Trägergas: | Helium, 2 ml/min, |
| Make-up-Gas: | Stickstoff, 60 ml/min, |
| Injektionsvolumen: 1 µl. | |
4 Auswertung
4.1 Kalibrierung
In den Gaschromatographen wird 1 µl der jeweiligen Kalibrierlösung eingespritzt. Durch Auftragen der ermittelten Peakflächenverhältnisse über die in 5 ml der jeweiligen Kalibrierlösung bestehenden Massenverhältnisse der einzelnen DNT-Isomeren zu 1,2-Dinitrobenzol werden die Kalibrierkurven erstellt.
4.2 Berechnen des Analysenergebnisses
Die Linearität der Kalibrierkurven ist nicht über den gesamten geprüften Konzentrationsbereich gegeben. Innerhalb enger Konzentrationsbereiche sind die Kalibrierkurven jedoch hinreichend linear. Somit lässt sich die nichtlineare Kalibrierkurve durch einen Polygonzug darstellen.
Die Berechnung der Massenkonzentration der einzelnen DNT-Isomeren in der Probeluft in mg/m3 erfolgt nach der Formel (1):
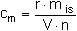 (1)
(1)
Für die Berechnung der Volumenkonzentration cV in ml/m3 aus cm gilt, bezogen auf 20 °C und 1013 hPa, Formel (2):
cv = 0,13 * cm (2)
Es bedeuten:
| cm = | Massenkonzentration des jeweiligen DNT-Isomeren in der Probeluft in mg/m3, |
| cV = | Volumenkonzentration des jeweiligen DNT-Isomeren in der Probeluft in ml/m3 (ppm), |
| miS = | Masse des 1,2-Dinitrobenzols (interner Standard) in der Desorptionslösung in µg, |
| r = | aus der Kalibrierkurve ermitteltes Massenverhältnis des jeweiligen DNT-Isomeren zu 1,2-Dinitrobenzol (interner Standard) in der Desorptionslösung, |
| V = | Probeluftvolumen in l, |
| n = | Wiederfindungsrate. |
5 Beurteilung des Verfahrens
5.1 Genauigkeit und Wiederfindungsrate
Jeweils 6 Sammelröhrchen wurden mit je 0,25 µg, 2,5 µg und 7,5 µg eines jeden DNT-Isomeren beaufschlagt (Injektion mit Kalibrierlösungen). Anschließend wurde zwei Stunden lang Laborluft (30-40 % rel. Luftfeuchte) mit einem Volumenstrom von 0,5 l/min durch das jeweilige Röhrchen gesaugt. Die angegebenen Dinitrotoluolmassen entsprechen bei 60 l Luftvolumen Konzentrationen von 4,2 µg/m3 bis 125 µg/m3. Bei Durchführung der beschriebenen Probenaufbereitung und Analyse ergaben sich relative Standardabweichungen, wie in der Tabelle 1 ersichtlich:
Tabelle 1
| Konzentration µg/m3 | relative Standardabweichung % | ||||
| 2,3-DNT | 2,4-DNT | 2,6-DNT | 3,4-DNT | 3,5-DNT | |
| 4,2 | 8,4 | 7,8 | 7,7 | 8,0 | 7,8 |
| 42 | 2,3 | 3,0 | 2,4 | 2,6 | 2,5 |
| 125 | 2,1 | 1,5 | 3,2 | 2,8 | 3,3 |
Bei einem Luftvolumen von 60 l und einem Volumenstrom von 0,5 l/min lag die Wiederfindungsrate unter den beschriebenen Bedingungen über 0,9.
5.2 Bestimmungsgrenze
Die absolute Bestimmungsgrenze beträgt 12 pg DNT-Isomer. Das entspricht 0,06 µg DNT-Isomer/Tenax-Röhrchen bzw. Probe.
Die relative Bestimmungsgrenze beträgt 1 µg/m3 für 60 l Probeluft, 5 ml Desorptionslösung und 1 µl Injektionsvolumen.
5.3 Selektivität
Unter den angegebenen GC-Bedingungen werden alle DNT-Isomeren getrennt. Beim Vorliegen von Störkomponenten muss ggf. eine Säule mit anderer Trenncharakteristik verwendet werden.
6 Bemerkungen
Die verlustfreie Lagerfähigkeit der beaufschlagten Röhrchen beträgt im Dunkeln und bei Raumtemperatur mindestens 14 Tage.
_________
1 Polytetrafluorethylen.
 | ENDE |
...
X
⍂
↑
↓
