 Für einen individuellen Ausdruck passen Sie bitte die
Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Bund

 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Bund |  |
Empfehlung 2005/175/EG der Kommission vom 1. März 2005 für ein koordiniertes Programm zur amtlichen Lebensmittelüberwachung für 2005
(ABl. Nr. L 59 vom 05.03.2005 S. 27)
Die Kommission der Europäischen Gemeinschaften -
gestützt auf den Vertrag zur Gründung der Europäischen Gemeinschaft,
gestützt auf die Richtlinie 89/397/EWG des Rates vom 14. Juni 1989 über die amtliche Lebensmittelüberwachung 1, insbesondere auf Artikel 14 Absatz 3,
nach Anhörung des Ständigen Ausschusses für die Lebensmittelkette und Tiergesundheit,
in Erwägung nachstehender Gründe:
(1) Koordinierte Lebensmittelüberwachungsprogramme auf Gemeinschaftsebene, mit denen die einheitliche Durchführung der amtlichen Lebensmittelüberwachung durch die Mitgliedstaaten zweckmäßiger gestaltet werden soll, sind erforderlich, um das ordnungsgemäße Funktionieren des Binnenmarktes zu gewährleisten.
(2) Diese Programme sollten den Nachdruck auf Übereinstimmung mit den gemeinschaftlichen Rechtsvorschriften für Lebensmittel legen, die insbesondere den Schutz der öffentlichen Gesundheit und der Verbraucherinteressen sowie die Gewährleistung loyaler Handelspraktiken zum Ziel haben.
(3) Mit der Richtlinie 89/397/EWG werden die allgemeinen Grundsätze für die Durchführung amtlicher Lebensmittelkontrollen, einschließlich der von den zuständigen Behörden der Mitgliedstaten durchzuführenden Inspektionen, festgelegt. Außerdem sieht sie vor, dass die Kommission den Mitgliedstaaten alljährlich eine Empfehlung über ein koordiniertes Überwachungsprogramm für das folgende Jahr übermittelt.
(4) Die Empfehlung der Kommission vom 19. Dezember 2003 über ein koordiniertes Programm zur amtlichen Lebensmittelüberwachung für 2004 2 enthält Empfehlungen für ein koordiniertes Programm amtlicher Kontrollen, einschließlich der Bewertung der bakteriologischen Sicherheit von aus roher oder thermisierter Milch hergestelltem Käse. Diese Untersuchung sollte auf andere, aus pasteurisierter Milch hergestellte Käsekategorien ausgedehnt werden, damit zweckmäßige Schlussfolgerungen hinsichtlich der Sicherheit dieser Erzeugnisse gezogen werden können.
(5) Mit der Richtlinie 93/99/EWG des Rates vom 29. Oktober 1993 über zusätzliche Maßnahmen im Bereich der amtlichen Lebensmittelüberwachung 3 werden die Bestimmungen der Richtlinie 89/397/EWG ergänzt. Sie sieht vor, dass die amtlichen Laboratorien in den Mitgliedstaaten gemäß Artikel 7 der Richtlinie 89/397/EWG die Kriterien der europäischen Normenreihe EN 45000, mittlerweile ersetzt durch EN ISO 17025:2000, erfüllen müssen.
(6) Die Durchführung der koordinierten Programme lässt alle übrigen von den Mitgliedstaaten im Rahmen ihrer nationalen Überwachungsprogramme durchgeführten amtlichen Kontrollen unbeschadet.
(7) Die gleichzeitige Durchführung einzelstaatlicher und koordinierter Programme kann Informationen liefern und zu Erfahrungen führen, auf die sich die künftige Überwachung und Rechtsetzung stützen kann
- Empfiehlt:
1. Im Jahr 2005 sollten die Mitgliedstaaten Inspektionen und Kontrollen durchführen und, wo erforderlich, Proben nehmen und diese in Laboratorien analysieren mit folgendem Ziel:
2. Zwar wird in dieser Empfehlung die Häufigkeit der Probenahmen und/oder Inspektionen nicht festgelegt, die Mitgliedstaaten sollten jedoch sicherstellen, dass sie so häufig durchgeführt werden, dass sie einen Überblick über den entsprechenden Bereich in den einzelnen Mitgliedstaaten ermöglichen.
3. Die Mitgliedstaaten sollten Informationen entsprechend dem Format der Berichtsblätter in den Anhängen I - IV liefern und damit zur Vergleichbarkeit der Ergebnisse beitragen. Diese Auskünfte sollten der Kommission zusammen mit einem erläuternden Bericht, der Hinweise zu den Ergebnissen und den getroffenen Durchführungsmaßnahmen enthalten sollte, bis zum 1. Mai 2006 zugeleitet werden.
4. Die im Rahmen dieses Programms für 2005 zu analysierenden Lebensmittel sollten Laboratorien übergeben werden, die die Anforderungen von Artikel 3 der Richtlinie 93/99/EWG erfüllen. Sollten jedoch solche Laboratorien für bestimmte in dieser Empfehlung vorgesehene Analysen in Mitgliedstaaten nicht vorhanden sein, so können diese Mitgliedstaaten auch andere Laboratorien benennen, die zur Durchführung dieser Analysen befähigt sind.
5. Bakteriologische Sicherheit von Käse aus pasteurisierter Milch
5.1 Anwendungsbereich des koordinierten Programms für 2005
Ziel dieses Programmelements ist es, die im Jahr 2004 im Rahmen des koordinierten Programms für 2004 begonnenen mikrobiologischen Untersuchungen, die sich nur auf aus roher oder thermisierter Milch hergestellten Käse konzentrierten, fortzuführen, um auch andere Käse einzubeziehen, für deren Herstellung Milch aus einer stärkeren Wärmebehandlung als der Thermisierung (d. h. Pasteurisierung) verwendet wird. Diese Erweiterung des koordinierten Programms wird empfohlen, damit über die Sicherheit von Käse zweckmäßige Schlussfolgerungen gezogen werden können. Die Ergebnisse dieser Untersuchung werden ausgewertet und mit den Ergebnissen der Erhebung von 2004 vorgelegt, damit in diesem Sektor ein allgemeiner Überblick vorhanden ist.
5.2 Probenahme und Analysemethode
Untersucht werden sollten Frischkäse, Weichkäse und halbfester Käse aus pasteurisierter Milch. Hierzu sollten die zuständigen Behörden der Mitgliedstaaten repräsentative Proben dieser Erzeugnisse bei der Herstellung und im Einzelhandel entnehmen - einschließlich eingeführter Erzeugnisse - und auf Salmonella und Listeria monocytogenes testen bzw. Staphylococcus aureus und Escherichia coli auszählen. Bei Nachweis von Listeria monocytogenes sollten diese Bakterien ebenfalls ausgezählt werden. Werden Proben auf der Einzelhandelsstufe entnommen, können die Tests auf den Nachweis von Salmonella und die Auszählung von Listeria monocytogenes beschränkt werden. Die Proben von jeweils mindestens 100 g bzw. 1 Käse bei weniger als 100 g sollten nach den Grundsätzen der Hygiene gehandhabt, in Kühlbehältern aufbewahrt und unverzüglich zur Auswertung an das Labor gesandt werden.
Den Laboratorien sollte es freigestellt sein, Methoden ihrer Wahl zu verwenden, sofern der entsprechende Leistungsumfang dem verfolgten Zweck gerecht wird. Empfohlen werden allerdings die neueste Fassung der ISO-Norm 6785 oder EN/ISO-Norm 6579 zum Nachweis von Salmonella, die neueste Fassung von EN/ISO 11290-1 und 2 zum Nachweis von Listeria monocytogens, die neueste Fassung der EN/ISO 6888-1 oder 2 zum Nachweis von Staphylococcus aureus und die neueste Fassung der ISO-Norm 11866-2, 3 oder ISO 16649-1, 2 zum Nachweis von Escherichia coli. Angewandt werden können auch weitere gleichwertige von den zuständigen Behörden anerkannte Analysemethoden.
Der Gesamtprobenumfang sollte im Ermessen der zuständigen Behörden der Mitgliedstaaten liegen.
Die Ergebnisse dieser Kontrollen sind in den Musterbogen in Anhang I einzutragen.
6. Bakteriologische Sicherheit gemischter Salate hinsichtlich Listeria monocytogenes
6.1 Anwendungsbereich des koordinierten Programms für 2005
In den letzten Jahren ist der Verbrauch an verzehrfertigen Lebensmitteln, wie z.B. gemischten Salaten, die rohes Gemüse und andere Zutaten (wie etwa Fleisch oder Meeresfrüchte) enthalten, angestiegen. Aufgrund des Vorhandenseins krankheitserregender Bakterien, wie z.B. Listeria monocytogenes, kann diese Produktart möglicherweise ein Risiko für die Gesundheit der Bevölkerung darstellen. Zur Verhinderung des Wachstums pathogener Bakterien, die möglicherweise in den Erzeugnissen vorhanden sind, und zum Schutz der Gesundheit der Bevölkerung ist die Durchführung spezifischer Hygienemaßnahmen, einschließlich angemessener Haltbarkeit und Temperaturüberwachung von entscheidender Bedeutung.
Dieses Programmelement verfolgt das Ziel, die mikrobiologische Sicherheit von vorgemischten Salaten, die rohes Gemüse und andere Zutaten (wie z.B. Fleisch oder Meeresfrüchte) enthalten, in Bezug auf Listeria monocytogenes zu untersuchen, um einen hohen Grad des Verbraucherschutzes zu fördern und Informationen zum Vorkommen dieser Bakterien in solchen Erzeugnissen zu erhalten.
6.2. Probenahme und Analysemethode
Untersucht werden sollten vorverpackte gemischte rohe Gemüsesalate, die Fleisch oder Meeresfrüchte oder sonstige Zutaten enthalten, die
Die zuständigen Behörden der Mitgliedstaaten sollten auf Einzelhandelsebene, vorzugsweise in Supermärkten, Proben dieser Erzeugnisse entnehmen und diese auf das Vorhandensein von Listeria monocytogenes untersuchen sowie eine Auszählung des Bakteriums vornehmen. Eine Probe besteht aus einer Probeneinheit (eine nicht geöffnete Verpackung). Die Proben, die nach Möglichkeit nahe am Verfallsdatum entnommen werden sollten, sind in Kühlbehältern unmittelbar dem Labor zur Untersuchung zuzusenden. Die Lagertemperatur und die Haltbarkeit der Erzeugnisse sollten bei der Probenahme aufgezeichnet und die Daten in den Erläuterungsbericht zu den Untersuchungsergebnissen aufgenommen werden.
Im Labor sollten die Proben so behandelt werden, dass alle Zutaten gründlich gemischt werden.
Für die Ermittlung und Auszählung von Listeria monocytogenes wird die aktuellste Fassung der Norm EN/ISO 11290-1 und 2 empfohlen. Den Laboratorien sollte es freigestellt sein, Methoden ihrer Wahl zu verwenden, sofern der entsprechende Leistungsumfang dem verfolgten Zweck gerecht wird.
Der Gesamtprobenumfang sollte im Ermessen der zuständigen Behörden der Mitgliedstaaten liegen.
Die Ergebnisse dieser Kontrollen sind in den Musterbogen in Anhang II einzutragen.
7. Sicherheit, Qualität und Etikettierung von Geflügelfleisch hinsichtlich der Verwendung von Wasserbindern
7.1 Anwendungsbereich des koordinierten Programms für 2005
Bei vor kurzem durchgeführten Probenahmen in bestimmten Mitgliedstaaten hat sich gezeigt, dass eine beachtliche Anzahl von Erzeugnissen im Handel sind, denen zu viel Wasser und hydrolysierte Proteine als Wasserbinder in Geflügelfleisch und Geflügelfleischzubereitungen zugesetzt sind.
Artikel 5 Absatz 1 der Richtlinie 71/118/EWG des Rates vom 15. Februar 1971 zur Regelung gesundheitlicher Fragen beim Handelsverkehr mit frischem Geflügelfleisch 4 verbietet das Inverkehrbringen von frischem Geflügelfleisch, bei dem Wirkstoffe verwendet wurden, die speziell die Wasserbindung fördern.
In einem vor kurzem veröffentlichten Arbeitspapier der Kommissionsdienststellen (SEC(2004) 1130) wurden die Mitgliedstaaten außerdem darauf aufmerksam gemacht, dass die Verwendung von Wasserbindern, die in Geflügelzubereitungen und Erzeugnissen verwendet werden dürfen, gemäß den von den Mitgliedstaaten gebilligten Verhaltenskodizes oder der guten Herstellungspraxis sowie unter Einhaltung der Vorschriften zum Verbraucherschutz und über die Etikettierung von Lebensmitteln erfolgen muss, wie in der Richtlinie 2000/13/EG des Europäischen Parlaments und des Rates vom 20. März 2000 zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über die Etikettierung und Aufmachung von Lebensmitteln sowie die Werbung hierfür 5 vorgesehen.
Ziel dieses Programmelements ist es, auf Gemeinschaftsebene die ordnungsgemäße Durchführung der Richtlinie 71/118/EWG hinsichtlich der Verwendung von Wasserbindern in gekühltem und tiefgefrorenem Geflügelfleisch (Hähnchenbrust) und deren Verwendung in tiefgefrorenen Geflügelzubereitungen (Hähnchenbrust) zu überprüfen, um den Verbraucherschutz zu fördern und die ordnungsgemäße Etikettierung zu kontrollieren.
7.2 Probenahme und Analysemethode
Bei der Probenahme, Untersuchung und Auswertung der Ergebnisse sollten die zuständigen Behörden der Mitgliedstaaten nach dem in Anhang V beschriebenen Analyseprotokoll vorgehen.
Es wird empfohlen, die Probenahme auf Großhandelslieferungen gefrorener Hähnchenbrust sowie auf gekühlte und gefrorene Hähnchenbrust im Einzelhandel zu konzentrieren. Der Gesamtprobenumfang sollte im Ermessen der zuständigen Behörden der Mitgliedstaaten liegen.
Die Ergebnisse dieser Kontrollen sind in den Musterbogen in Anhang III einzutragen.
8. Sicherheit bestimmter Lebensmittel für Säuglinge und Kleinkinder hinsichtlich des Gehalts an Nitrat und Patulin
8.1 Anwendungsbereich des koordinierten Programms für 2005
Lebensmittel, die Kontaminanten in Mengen enthalten, welche toxikologisch nicht mehr akzeptabel sind, können möglicherweise ein Risiko für die Gesundheit der Bevölkerung darstellen, insbesondere für anfällige Bevölkerungsgruppen, wie z.B. Säuglinge und Kleinkinder. Das Vorhandensein von Kontaminanten kann durch gute Herstellungs- oder landwirtschaftliche Praxis vermindert werden.
Zum Schutz der Gesundheit der Bevölkerung wurden in der Verordnung (EG) Nr. 466/2001 der Kommission vom 8. März 2001 zur Festsetzung der Höchstgehalte für bestimmte Kontaminanten in Lebensmitteln 6 und Verordnung (EG) Nr. 655/2004 der Kommission vom 7. April 2004 zur Änderung der Verordnung (EG) Nr. 466/2001 im Hinblick auf Nitrat in Lebensmitteln für Säuglinge und Kleinkinder 7 spezifische Höchstgehalte für Nitrat und Patulin in Lebensmitteln festgesetzt, die für Säuglinge und Kleinkinder bestimmt sind.
Ziel dieses Programmelements ist es, zu überprüfen, ob für Säuglinge und Kleinkinder bestimmte im Handel befindliche Lebensmittel die in den Gemeinschaftsvorschriften festgelegten Höchstgehalte für Nitrat und Patulin einhalten, damit ein hohes Niveau an Verbraucherschutz gewährleistet ist.
8.2 Probenahme und Analysemethode
Die zuständigen Behörden der Mitgliedstaaten sollten repräsentative Proben von für Säuglinge und Kleinkinder bestimmten Lebensmitteln entnehmen, insbesondere von Lebensmitteln, die Karotten, Kartoffeln, Blattgemüse und Apfelerzeugnisse enthalten, und zwar insbesondere im Einzelhandel, wobei jedoch die Produktionsstufen der Herstellung und der Einfuhr (falls zutreffend) nicht außer Acht gelassen werden sollten, und diese auf Nitrat (Lebensmittel, die Karotten, Kartoffeln und Blattgemüse enthalten) und Patulin (andere als verarbeitete Lebensmittel auf Getreidebasis, die Apfelerzeugnisse enthalten) untersuchen.
Für die amtliche Kontrolle des Gehalts an Nitrat und Patulin werden die Probenahme- und Analysemethoden der folgenden Gemeinschafts-Vorschriften empfohlen:
Der Gesamtprobenumfang sollte im Ermessen der zuständigen Behörden der Mitgliedstaaten liegen.
Die Ergebnisse dieser Kontrollen sind in den Musterbogen in Anhang IV einzutragen.
| Bakteriologische Sicherheit von Käse aus Pasteurisierter Milch | Anhang I |
Mitgliedstaat: ______________________________
| Bakteriengruppen/ Kriterien 1 | Probe- nahmestufe | Produkt | Proben- anzahl | Analyseergebnisse 2 | Getroffene Maßnahmen (Anzahl und Art) 3 | |||
| Z | A | U | ||||||
| Salmonella spp. n=5 c=0 in 25 g nicht nachweisbar | Produktion | Unausgereifter (frischer) Weichkäse | ||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Einzelhandel | Unausgereifter (frischer) Weichkäse | |||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Staphylococcus aureus n=5 c=2 m=100 KBE/g M=1.000 KBE/g | Produktion | Unausgereifter (frischer) Weichkäse | ||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Einzelhandel | Unausgereifter (frischer) Weichkäse | |||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Escherichia coli n=5 c=2 m=100 KBE/g M=1.000 KBE/g | Produktion | Unausgereifter (frischer) Weichkäse | ||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Einzelhandel | Unausgereifter (frischer) Weichkäse | |||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Bakteriengruppen/ Kriterien 1 | Probe- nahmestufe | Produkt | Proben- anzahl | Analyseergebnisse 2 | Getroffene Maßnahmen (Anzahl und Art) 3 | |||
| Z | A | U | ||||||
| N | V | < 100 KBE/g | > 100 KBE/g | |||||
| Listeria monocytogenes n=5 c=0 in 25 g nicht nachweisbar | Produktion | Unausgereifter (frischer) Weichkäse | ||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| Einzelhandel | Unausgereifter (frischer) Weichkäse | |||||||
| Ausgereifter Weichkäse | ||||||||
| Halbfester Käse | ||||||||
| 1) Bei Probenahme im Einzelhandel kann die Probenanzahl (n) reduziert werden.
Die Reduzierung der Probenanzahl ist im Bericht anzugeben.
2) Z = Zufrieden stellend, A = Akzeptabel, U = Nicht zufrieden stellend; bei Listeria monocytogenes N = Nicht vorhanden, V = Vorhanden. Bei Staphylococcus aureus und Escherichia coli ist das Ergebnis zufrieden stellend, wenn alle beobachteten Werte <m sind, akzeptabel, wenn höchstens c Werte zwischen m und M liegen, und nicht zufrieden stellend, wenn mindestens ein Wert >M ist oder wenn mehr als c Werte zwischen m und M liegen. 3) Bei der Meldung der Durchführungsmaßnahmen wird folgende Unterteilung empfohlen: mündliche Verwarnung, schriftliche Verwarnung, verbesserte innerbetriebliche Überwachung erforderlich, Rückruf des Produkts gefordert, Verwaltungssanktion, gerichtliche Sanktion, Sonstige. | ||||||||
| Mikrobiologische Sicherheit gemischter Salate (in Bezug auf Listeria monocytogenes) | Anhang II |
Mitgliedstaat: _____________________
| Bakterielle Pathogene | Produkt 1 | Proben- Anzahl | Analyseergebnisse | Getroffene Maß nahmen (Anzahl und Art ) (z | |||||
| Nachweis: in 25 g | Zählung: KBE/g | ||||||||
| Nicht nachweisbar | Nachweisbar | < 10 | 10-99 | 100-999 | < 1.000 | ||||
| Listeria monocytogenes | |||||||||
| 1) Das Produkt sollte anhand seiner Hauptzutaten identifiziert werden.
2) Bei der Meldung der Durchführungsmaßnahmen wird die folgende Unterteilung empfohlen: mündliche Verwarnung, schriftliche Verwarnung, verbesserte innerbetriebliche Überwachung erforderlich, Rückruf des Produktes erforderlich, Verwaltungssanktion, gerichtliche Sanktion, sonstige. | |||||||||
| Sicherheit, Qualität und Etikettierung von Geflügelfleisch hinsichtlich der Verwendung von Wasserbindern | Anhang III |
Mitgliedstaat: _____________________
| Proben- code | Produkt- name und Beschrei- bung Etikettie- rung | Verpacker/ Verarbeiter und Genuss- tauglich- keitskenn- zeichen | Zutaten- liste | Etikettierung: Hähnchen Angabe | % Feuchtig- keit | % Fett | % Stick- stoff | % Protein | % Asche | Hydoxy- prolin g/100g | Übermäßiges Hydroxy- prolin g/100g | % Kohlen- hydrat | Errechneter Hähnchen- gehalt Bei Faktor 3,85 | Korrigierter Hähnchen- gehalt Bei Hydroxy- prolin > 0,08 | Getrof- fene Maß- nahmen Anzahl und Art) 1 |
| 1) Bei der Meldung der Durchführungsmaßnahmen wird die folgende Unterteilung empfohlen: mündliche Verwarnung, schriftliche Verwarnung, verbesserte innerbetriebliche Überwachung erforderlich, Rückruf des Produktes erforderlich, Verwaltungssanktion, gerichtliche Sanktion, Sonstige. | |||||||||||||||
| Sicherheit bestimmter für Säuglinge und Kleinkinder bestimmte Lebensmittel hinsichtlich des Gehalts an Nitrat und Patulin | Anhang IV |
Mitgliedstaat: _____________________
1. Nitrat
| Probenahmestufe | Produkt | Probenanzahl | Analyseergebnisse (mg/kg) | Getroffene Maßnahmen (Anzahl und Art) 1 | |||
| <100 | 100-150 | 151-200 | >200 | ||||
| Einzelhandel | |||||||
| Produktion | |||||||
| Einfuhr (falls zutreffend) | |||||||
2. Patulin
| Probenahmestufe | Produkt | Probenanzahl | Analyseergebnisse (mg/kg) | Getroffene Maßnahmen(Anzahl und Art) 1 | ||
| <10 | 10-25 | >25 | ||||
| Einzelhandel | ||||||
| Produktion | ||||||
| Einfuhr (falls zutreffend) | ||||||
| 1) Bei der Meldung der Durchführungsmaßnahmen wird die folgende Unterteilung empfohlen: mündliche Verwarnung, schriftliche Verwarnung, verbesserte innerbetriebliche Überwachung erforderlich, Rückruf des Produktes erforderlich, Verwaltungssanktion, gerichtliche Sanktion, Sonstige. | ||||||
| Analyseprotokoll | Anhang V |
Verfahren zur Bestimmung des Gehalts an Hähnchen oder an zugesetztem Wasser und an Proteinen auf
Kollagenbasis bei Hähnchenbrusterzeugnissen
Frische Hähnchenbrust (Gekühlt oder Gefroren)
Sofern die Hähnchenbrust keine zugesetzten Proteine, Stabilisatoren oder sonstige Zutaten enthält, wird das zugesetzte Wasser nach der amtlichen EG-Methode für Fremdwasser (Verordnung (EWG) Nr. 1538/91 der Kommission 10 berechnet. Als Mindestprobe für die amtliche Methode sind fünf Hähnchenbrüste ohne Haut und Knochen zu verwenden. Das zugesetzte Wasser kann bestimmt werden anhand der Kurve, die die Beziehung zwischen dem Verhältnis Wasser: Protein und dem Fremdwassergehalt in Hähnchenbrust ohne Haut und Knochen darstellt (Abbildung 1). Das Wasser-Protein-Verhältnis für Hähnchenbrust ohne Haut und Knochen und ohne zugesetztes Wasser beträgt 3,28, und bei 2 % Fremdwasser (der Grenzwert für Hähnchenbrust ohne Haut und Knochen) beträgt das Wasser-Protein-Verhältnis 3,40.
Gefrorene Hähnchenbrustzubereitungen
1. Erhalt und Lagerung der Probe
1.1 Beim Großhandel besteht eine Probe normalerweise aus einer 10-kg-Kiste tiefgefrorenen Hähnchenbrusterzeugnisses ohne Haut und Knochen. Im Einzelhandel ist eine Mindestprobe von fünf Hähnchenbrüsten ohne Haut und Knochen mit dem gleichen Haltbarkeitsdatum oder der gleichen Loskennzeichnung zu entnehmen.
1.2 Bei Erhalt sind die Proben zu prüfen, um sicherzustellen, dass die Verpackung nicht beschädigt und die Probe (sofern tiefgefroren) gut tiefgefroren ist.
1.3 Nach Erhalt sind die Proben vor der Analyse tiefgefroren aufzubewahren (- 18 °C ± 4 °C).
2. Zweck und Anwendungsbereich
2.1 Mit dieser Methode werden der Hähnchengehalt (und als Differenz das zugesetzte Wasser) sowie die Proteine auf Kollagenbasis in Hähnchenbrusterzeugnissen ohne Haut und Knochen bestimmt. Dabei werden Proteinstickstoff, Feuchtigkeit, Asche, Fett und Hydroxyprolin bestimmt.
3. Grundsatz
3.1 Der (scheinbare) fettfreie Hähnchengehalt wird errechnet aus dem Gehalt an Proteinstickstoff und einem Stickstofffaktor für Hähnchenbrust ohne Haut und Knochen (Abschnitt 9). Wurden der Hähnchenbrust Proteine auf Kollagenbasis zugesetzt, muss deren Anteil zuerst vom Gesamtproteinstickstoff abgezogen werden. Der gesamte Hähnchengehalt wird durch Addition des Fettgehalts und des fettfreien Hähnchengehalts errechnet. Ein Maß für das zugesetzte Wasser kann durch Abzug aller Hähnchenbestandteile (Hähnchengehalt, Asche und Kohlenhydrat) von 100 errechnet werden.
4. Gesundheit und Sicherheit
4.1 Bei der Untersuchungsmethode wird eine Reihe von möglicherweise gefährlichen Geräten verwendet, wie z.B. ein Hochleistungsfleischwolf und ein Homogenisierapparat, daher sollten geeignete Vorsichtsmaßnahmen getroffen werden.
5. Grundlegende Schulungsanforderungen
5.1 Eine Schulung in der Verwendung von gewerblichen Metzgereigeräten ist erforderlich.
6. Geräte
6.1 Präzisionswaage, deren Genauigkeit über ± 0,1 g liegt.
6.2 Hochleistungsfleischwolf und/oder Mixer, mit dem man gefrorene Hähnchenbrust homogenisieren kann.
Anmerkung: Es wird kein Fleischwolf-Fabrikat empfohlen, das verwendete Gerät sollte jedoch soviel Leistung bringen, dass gefrorenes oder tiefgefrorenes Hähnchen zu einer homogenen Mischung zerkleinert wird, die derjenigen aus einem Fleischwolf mit 4 mm Lochscheibe entspricht.
6.3 Gerät gemäß ISO 1442:1997 (BS 4401 - 3:1997) zur Bestimmung des Wassergehalts.
6.4 Gerät gemäß ISO 937:1978 (BS 4401 - 2:1980) zur Bestimmung des Proteingehalts, oder gleichwertig.
6.5 Gerät gemäß ISO 936:1998 1998 (BS 4401 - 1:1998) zur Bestimmung der Gesamtasche.
6.6 Geräte gemäß BS 4401 - 4:1970 zur Bestimmung des Gesamtfettgehalts.
6.7 Gerät gemäß ISO 3496:1994 (BS 4401 - 11:1995) zur Bestimmung von Hydroxyprolin.
7. Verfahren
Anmerkung: Die Probe ist bis zum Beginn der Analyse gemäß den Abschnitten 7.1 bis 7.10 (unten) gefroren aufzubewahren.
7.1 Die Probe ist aus der Verpackung zu nehmen und auf eine große gereinigte Kunststoffplatte zu legen, die mit Folie ausgelegt ist, damit Feuchtigkeitsverlust verhindert wird.
7.2 Die Probe ist portionsweise zu hacken oder zu homogenisieren und auf die Kunststoffplatte zurückzugeben. Dieser Vorgang wird wiederholt, bis die gesamte Probe zerhackt/homogenisiert ist.
7.3 Mit einem sauberen großen Kunststofflöffel ist die gesamte zerhackte Probe zu mischen, wobei darauf zu achten ist, dass alles "Abgetropfte" der Masse wieder zugegeben wird.
7.4 Bei Großhandelsproben ist eine 2-kg-Aliquote der Probe und bei Einzelhandelsproben, die gesamte Probe (sofern 2 kg) in einem Mixer oder einer Küchenmaschine fein zu homogenisieren.
Anmerkung: Die übrigen 8 kg der Großhandelsprobe können entsorgt werden.
7.5 Von den 2 kg sind zwei 50-g-Aliquoten (erforderlichenfalls für DNA) zu entnehmen und in einen Behälter geeigneter Größe zu geben. Der Rest ist in eine saubere, beschriftete Kunststofftüte zu geben oder der Einfachheit halber in Teilproben von je 200 g zu unterteilen. Proben, die nicht unmittelbar untersucht werden, sollten gefroren gelagert werden.
7.6 Von dem homogenisierten Material ist eine Probe zu entnehmen und deren Feuchtigkeitsgehalt gemäß ISO 1442 zu bestimmen.
7.7 Von dem homogenisierten Material ist eine Probe zu entnehmen und deren Stickstoffgehalt gemäß ISO 937 (oder gleichwertig) zu bestimmen.
7.8 Von dem homogenisierten Material ist eine Probe zu entnehmen und deren Aschegehalt gemäß ISO 936 zu bestimmen.
7.9 Von dem homogenisierten Material ist eine Probe zu entnehmen und deren Fettgehalt gemäß BS 4401-4 zu entnehmen.
7.10 Von dem homogenisierten Material ist eine Probe zu entnehmen und deren Hydroxyprolin-Gehalt gemäß ISO 3496 zu bestimmen.
8. Qualitätskontrolle bei der Analyse
8.1 Alle Laboratorien sollten bei jeder Charge ein geeignetes Referenzmaterial mit ausgewiesenem Gehalt an Stickstoff, Feuchtigkeit, Fett, Asche und Hydroxyprolin zur Qualitätskontrolle als Duplikat analysieren. Die Messung akzeptabler Chargen muss innerhalb von zwei Standardabweichungen des ausgewiesenen Wertes liegen. Die Analysen der Duplikate müssen innerhalb der Wiederholbarkeitsmerkmale der Methode liegen.
9. Berechnung der Ergebnisse
Die Berechnung der Ergebnisse wurde dem Informationsblatt 20/01 vom Dezember 2001 der britischen Food Standards Agency entnommen, dass mit folgender Adresse auf der Website der Agency zur Verfügung steht:
http://www.food.gov.uk/science/surveillance/fsis-2001/20chick
9.1 Ermittlung des Hähnchengehalts mit Hilfe des Stickstofffaktors
Nach Stubbs and More (The Analyst 1919, 44, 125) wird die Probe auf Stickstoff, Feuchtigkeit, Fett und Asche untersucht.
Die aus der Untersuchung hervorgehenden Daten werden zuerst zur Berechnung des scheinbaren fettfreien Fleischgehalts nach folgender Gleichung verwendet:
Scheinbarer fettfreier Fleischgehalt = Gesamter Stickstoff/SF × 100
wobei SF = Stickstofffaktor in Verbindung mit dem untersuchten Erzeugnis.
(3,85 bei magerem Hähnchenbrustfleisch gemäß der Empfehlung von AMC (The Analyst, 2000, 125, 1359-1366)). Dabei ist zu beachten, dass dieser Faktor offensichtlich für Hähnchen aus Drittländern gilt.
Der gemessene Fettgehalt wird dann zu dieser Zahl addiert, die Summe ergibt den scheinbaren Gesamthähnchengehalt.
Scheinbarer Gesamthähnchengehalt = Scheinbarer fettfreier Hähnchengehalt + Fett
9.2 Zugesetztes Collagen-Protein
Hydrolysiertes Protein aus Collagen kann als in einer Probe vorhanden betrachtet werden, sofern der bestimmte Hydroxyprolin-Gehalt höher ist als der mit magerer Hähnchenbrust normalerweise verbundene (AMC-Daten 0,08 g/100 g - The Analyst, 2000, 125, 1359-1366).
Bei der oben beschriebenen Berechnung des scheinbaren Gesamthähnchengehalts wird davon ausgegangen, dass der gesamte bestimmte Stickstoff aus dem Hähnchenmuskel stammt. Ist ein Überschuss an Hydroxyprolin vorhanden, so ist eine Korrektur erforderlich.
Der von Collagen stammende Stickstoffanteil in einer Probe errechnet sich folgendermaßen aus dem Hydroxyprolin:
Collagen-Stickstoff = Überschuss Hydroxyprolin × 1,28
Der Anteil an Collagen-Stickstoff wird danach vom Anteil an Gesamt-Stickstoff abgezogen und der scheinbare Gesamthähnchengehalt wie oben berechnet.
9.3 Zugesetztes Wasser
Die Menge an zugesetztem Wasser kann bestimmt werden durch Abzug des Hähnchengehalts und aller zugesetzten Zutaten von 100 nach folgender Gleichung:
Zugesetztes Wasser % = 100 - (scheinbarer Gesamthähnchengehalt + Asche + Kohlenhydrate + sonstige Zutaten)
Kohlenhydrate = 100 - (Protein + Fett + Asche + Feuchtigkeit),
wobei Gesamtproteingehalt = Gesamtstickstoff × Umrechnungsfaktor (6,25).
Daraus kann die Menge an zugesetztem Wasser wie folgt bestimmt werden:
Zugesetztes Wasser % = 100 - (scheinbarer Gesamthähnchengehalt + Asche + Kohlenhydrate)
9.4 Messungenauigkeit
Die mittlere Messungenauigkeit bei der Bestimmung des Hähnchengehalts wird bei einem Konfidenzintervall von 95 % auf knapp 3 % Hähnchengehalt geschätzt. Daher können Proben, bei denen der bestimmte Fleischgehalt 5 % geringer ist als der angegebene, als falsch ausgezeichnet eingestuft werden.
Abbildung 1 - Fremdwasser Ni in Bezug zu Grenzwerten für Wasser: Protein
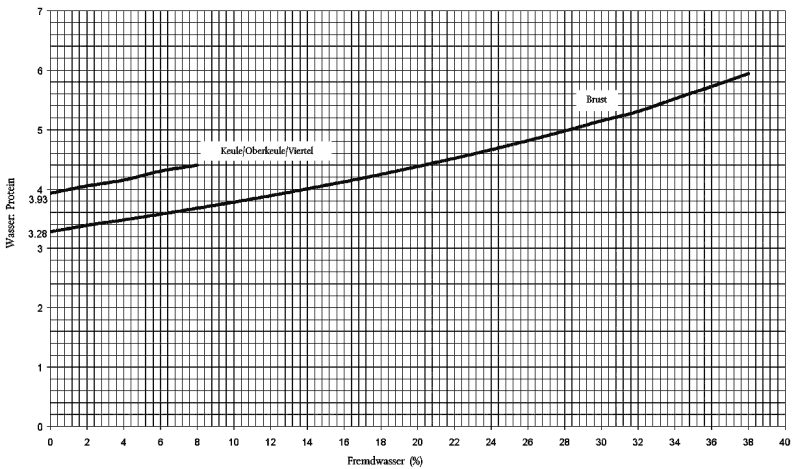
__________________
1) ABl. Nr. L 186 vom 30.06.1989 S. 23.
2) ABl. Nr. L 6 vom 10.01.2004 S. 29. 3) ABl. Nr. L 290 vom 24.11.1993 S. 14. Richtlinie zuletzt geändert durch die Verordnung (EG) Nr. 1882/2003 des Europäischen Parlaments und des Rates (ABl. Nr. L 284 vom 31.10.2003 S. 1).
3) ABl. Nr. L 290 vom 24.11.1993 S. 14. Richtlinie zuletzt geändert durch die Verordnung (EG) Nr. 1882/2003 des Europäischen Parlaments und des Rates (ABl. Nr. L 284 vom 31.10.2003 S. 1).
4) ABl. Nr. L 55 vom 08.03.1971 S. 23. Richtlinie zuletzt geändert durch die Verordnung (EG) Nr. 807/2003 (ABl. Nr. L 122 vom 16.05.2003 S. 36).
5) ABl. Nr. L 109 vom 06.05.2000 S. 29. Richtlinie zuletzt geändert durch die Richtlinie 2003/89/EG (ABl. Nr. L 308 vom 25.11.2003 S. 15).
6) ABl. Nr. L 77 vom 16.03.2001 S. 1. Verordnung zuletzt geändert durch die Verordnung (EG) Nr. 208/2005 (ABl. Nr. L 34 vom 08.02.2005 S. 3).
7) ABl. Nr. L 104 vom 08.04.2004 S. 48.
8) ABl. Nr. L 187 vom 16.07.2002 S. 30.
9) ABl. Nr. L 203 vom 12.08.2003 S. 40.
10) ABl. Nr. L 143 vom 07.06.1991 S. 11. Verordnung zuletzt geändert durch die Verordnung (EG) Nr. 814/2004 (ABl. Nr. L 153 vom 30.04.2004 S. 1).
 | ENDE |  |