 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. ▢ Regelwerk |  |
Richtwerte für gesättigte azyklische aliphatische C4- bis C11-Aldehyde in der Innenraumluft
- Mitteilungen der Adhoc-Arbeitsgruppe Innenraumrichtwerte der Innenraumlufthygiene-Kommissiondes Umweltbundesamtes und der Obersten Landesgesundheitsbehörden -
(Bundesgesundheitsbl. Nr. 6 vom 6/2009 S. 650)
Vorbemerkung
Aldehyde entstehen durch Oxidation primärer Alkohole. Eine Oxidation entspricht formal einem Entzug von 2 Wasserstoffatomen; diese Reaktion hat auch zur Namensgebung Aldehyd ("Alkohol dehydrogenatus") geführt. Anhand gemeinsamer Merkmale in der Molekülstruktur lassen sich Aldehyde verschiedenen Untergruppen zuordnen:
- gesättigte unverzweigte oder verzweigte aliphatische Aldehyde (IUPAC-Name: n- und i-Alkanale) wie zum Beispiel Methanal (ältere Bezeichnung: Formaldehyd), n-Hexanal, 3-Methylbutanal, 2-Ethylhexanal,
- gesättigte zyklische Aldehyde zum Beispiel Cyclohexylmethanal,
- aromatische Aldehyde wie zum Beispiel Phenylmethanal (Benzaldehyd) und aromatenähnliche ungesättigte zyklische Aldehyde zum Beispiel 2-Furylmethanal (Furfural),
- einfach oder mehrfach ungesättigte Aldehyde (Alkenale, Alkadienale) wie zum Beispiel Propenal (Acrolein), trans-Butenal (Crotonaldehyd), 3-Phenylpropenal (Zimtaldehyd), 2,4- undecadienal,
- mehrwertige Aldehyde (Alkandiale) wie zum Beispiel Ethandial (Glyoxal), Propandial (Malondialdehyd), Pentandial (Glutaraldehyd),
- Aldehyde mit benachbarten funktionellen Gruppen (Hydroxy-, Keto-, Säuregruppe) wie zum Beispiel Hydroxyethanal (Glykolaldehyd), 2,3-Dihydroxypropanal (Glycerinaldehyd).
Gesättigte azyklische aliphatische Aldehyde gehören zu den häufig vorkommenden und zumeist unerwünschten Verbindungen in der Innenraumluft. Eine Reihe von Aldehyden bildet sich durch Oxidation ungesättigter Fettsäuren wie Linol-, Linolen- oder Ölsäure, die sich durch den Einfluss von Wärme, Licht und Luftsauerstoff unter Bildung unter anderem von Aldehyden zersetzen. Beim Abbau von Linolsäure entsteht Hexanal, von Ölsäure die gesättigten C7- bis C10-Aldehyde Heptanal, Octanal, Nonanal und Decanal und von Linolensäure überwiegend ungesättigte Aldehyde. Wesentliche Emissionsquellen stellen fettsäurereiche Hölzer und Holzwerkstoffe, Lacke, Alkydharzfarben, Öle und Klebstoffe, Beschichtungsprodukte auf Naturöl-Basis sowie Bodenbeläge wie etwa Linoleum dar. Da die vorgenannten Zersetzungsprozesse oftmals relativ langsam ablaufen, kann es zu länger anhaltenden Geruchsbelästigungen kommen.
Aldehyde werden in geringen Mengen auch als Geruchs- und Aromastoffe in Raumsprays sowie in Lebensmitteln eingesetzt. In höheren Konzentrationen wird der Geruch als zunehmend fettig, ranzig, aber auch stechend beschrieben und kann Übelkeit auslösen. Während bestimmte Aldehyde wie zum Beispiel Formaldehyd oder der Dialdehyd Glutaraldehyd zumeist aufgrund spezifischer Anwendungen (in Desinfektionsmitteln) oder gezielter Verwendungen von Formaldehyd-Harnstoff-Harzen (Spanplatten, Ortschäume) vorkommen und daher in der Regel primären Quellen zugeordnet werden können, bilden sich die meisten gesättigten Aldehyde sekundär durch Oxidation von Vorläuferverbindungen. Die Ausgangsprodukte können insofern frei von Aldehyden sein.
Die besondere Bedeutung der gesättigten aliphatischen Aldehyde in der Innenraumluft lässt sich an folgender Untersuchung aufzeigen [1]: bei Kammeruntersuchungen von 50 üblicherweise im Innenraum eingesetzten Bauprodukten (unter anderem sieben Acryl- und sechs Silikondichtmassen, 13 Holzwerkstoffe, sechs Kunstharzfertigputze, fünf Lacke, sechs Wandfarben, vier Klebstoffe) wurde Hexanal als die zweithäufigste emittierte flüchtige organische Verbindung (nach Essigsäure) identifiziert. Auch die Aldehyde Nonanal, Octanal, Pentanal und Heptanal befanden sich (in dieser Abfolge) unter den 20 häufigsten von Bauprodukten abgegebenen Verbindungen. Bei Holz und Holzwerkstoffen stellte das Hexanal sogar die am häufigsten emittierte
Tabelle 1: Identifikation ausgewählter C 4- bis C11-Alkanale
| CAS-Nr. | IUPAC-Name | Synonym | Summenformel | Strukturformel |
| 78-84-2 | Methylpropanal | Isobutyraldehyd | C4H8O |  |
| 123-72-8 | n-Butanal | Butyraldehyd | C4H8O | 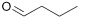 |
| 590-86-3 | 3-Methylbutanal | Isovaleraldehyd | C5H10O |  |
| 110-62-3 | n-Pentanal | Valeraldehyd | C5H10O |  |
| 66-25-1 | n-Hexanal | Capronaldehyd | C6H12O |  |
| 111-71-7 | n-Heptanal | Önanthaldehyd | C7H14O | 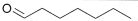 |
| 123-05-7 | 2-Ethylhexanal | - | C8H16O | 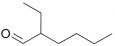 |
| 124-13-0 | n-Octanal | Caprylaldehyd | C8H16O |  |
| 124-19-6 | n-Nonanal | Pelargonaldehyd | C9H18O | 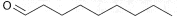 |
| 112-31-2 | n-Decanal | Caprinaldehyd | C10H20O | 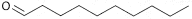 |
| 112-44-7 | n- undecanal | - | C11H22O | 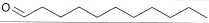 |
Verbindung dar, auch Pentanal, Heptanal und Nonanal fanden sich unter den io häufigsten gefundenen VOC. Angesichts der häufigen Verwendung der genannten Bauprodukte im Innenraum lassen sich diese Verbindungen deshalb auch fast immer in der Innenraumluft nachweisen.
In dieser Abhandlung soll die gesundheitliche Bewertung gesättigter unverzweigter oder verzweigter nichtzyklischer einfacher aliphatischer C4- bis C11-Aldehyde (n- und i-Alkanale) in der Innenraumluft dargestellt werden. Die Eingrenzung auf diese Stoffgruppe entspricht weitgehend der Einteilung des AgBB-Schemas, wonach bei Verwendung einer unpolaren Trennsäule C5- bis C11-Aldehyde definitionsgemäß den flüchtigen organischen Verbindungen (volatile organic compounds - VOC) zugeordnet werden [2]. Bei der derzeit üblichen VOC-Messpraxis werden jedoch in der Regel auch C4-Aldehyde miterfasst [3, 4]. Dieser Praxis folgend sollen deshalb abweichend vom AgBB-Vorschlagim Folgenden die C4-Alkanale in der Gruppe der gesättigten aliphatischen azyklischen Aldehyde mit berücksichtigt werden.
1 Identität und physikalisch-chemische Eigenschaften
In Tabelle 1 werden die im Innenraum bedeutsamen C4- bis C11-Alkanale benannt. Ausgewählte physikalisch-chemische Eigenschaften dieser Stoffgruppe zeigt Tabelle 2 auf.
2 Exposition gegenüber gesättigten aliphatischen C4- bis C11-Aldehyden
Alkanale werden seit mehr als zwei Jahrzehnten regelmäßig in der Luft nichtgewerblicher Innenräume nachgewiesen. Insbesondere Hexanal und Nonanal werden fast immer oberhalb der üblichen Bestimmungsgrenze (um 1 µg/m3) gefunden. Dabei weist Hexanal vielfach auch die
höchsten Konzentrationen in der Innenraumluft auf. Für die meisten C4- bis C11,-Alkanale liegen aktuelle Referenzwerte (95. Percentile) für Wohnräume vor [3], die das übliche Vorkommen in der Innenraumluft anzeigen (Tabelle 3). Gesättigte aliphatische Aldehyde lassen sich auch in Schulen (Tabelle 4) [5], Kindertagesstätten (Tabelle 5) [6] sowie in Büroräumen (Tabelle 6) [7] nachweisen.
Der zeitliche Abstand einer Messung zu einer vorangegangenen Renovierung oder einer anderen baulichen Maßnahme beeinflusst erwartungsgemäß die Höhe der gefundenen Konzentrationen an Alkanalen in der Innenraumluft. In einer umfangreichen Auswertung anlassbezogener Untersuchungen (zum Teil wenige Wochen bis Monate nach Renovierungsarbeiten) fanden sich im Vergleich zu Referenzwerten (Tabelle 3) vergleichbare Mediane, aber deutlich höhere Konzentrationen der 95. Percentilen und hohe Maximalwerte (Tabelle 7) [4].
Tabelle 2: Physikalisch-chemische Eigenschaften ausgewählter C 4- bis C11-Alkanale [37]
| CAS-Nr. | IUPAC-Name | Molmasse [g mol-1] | Schmelzpunkt [°C] | Siedepunkt [°C] | Dampfdruck [hPa bei 20°C] | Umrechnungsfaktor a |
| 78-84-2 | Methylpropanal | 72,10 | -65,9 | 64 | 230,6/25°C | 3,0 |
| 123-72-8 | n-Butanal | 72,10 | -97 | 75 | 113 | 3,0 |
| 590-86-3 | 3-Methylbutanal | 86,13 | -51 | 93 | 61 | 3,5 |
| 110-62-3 | n-Pentanal | 86,13 | -91,5 | 103 | 26 | 3,5 |
| 66-25-1 | n-Hexanal | 100,16 | -56 | 129 | 12 | 4,2 |
| 111-71-7 | n-Heptanal | 114,19 | -43 | 153 | 0,86 | 4,7 |
| 123-05-7 | 2-Ethylhexanal | 128,22 | < -100 | 163 | 2,4 | 5,3 |
| 124-13-0 | n-Octanal | 128,22 | 12 | 171 | 2 | 5,3 |
| 124-19-6 | n-Nonanal | 142,24 | -18 | 201 | 0,35/25°C | 5,9 |
| 112-31-2 | n-Decanal | 156,27 | 7 | 220 | 0,1 | 6,5 |
| 112-44-7 | n- undecanal | 170,29 | 0 | 239 | 0,5 | 7,1 |
| a) 1 ppm = [Umrechnungsfaktor] mg/m3 | ||||||
Tabelle 3: Wochenmittelwerte einer repräsentativen Untersuchung zum Vorkommen von azyklischen C 4- bis C11-Alkanalen in der Raumluft von Kinderzimmern (n = 586) in Deutschland 2003-2006 [3]
| Aldehyd | n < NG (%> NG) | Median [µg/m3] | 95. Percentil [µg/m3] | Maximalwert [µg/m3] |
| Butanal | 4 (99) | 2 | 8 | 43 |
| 3-Methylbutanal | 384 (35) | <1 | 4 | 16 |
| Pentanal | 7 (99) | 4 | 11 | 28 |
| Hexanal | 0 (100) | 10 | 30 | 92 |
| Heptanal | 68 (88) | 1 | 3 | 9 |
| Octanal | 3 (99) | 2 | 4 | 7 |
| Nonanal | 0 (100) | 7 | 15 | 30 |
| Decanal | 17 (97) | 3 | 6 | 10 |
| Undecanal | 327 (44) | <1 | 3 | 13 |
| Σ C4 - C11-Alkanale | n. a. | 33 | 70 | 187 |
Neben der inhalativen Exposition ist auch die orale Exposition gegenüber Alkanalen von Bedeutung. Alkanale kommen als natürliche Bestandteile in zahlreichen Lebensmitteln vor. Soweit einzelne Alkanale in Kosmetika verwendet werden, ist auch eine Aufnahme über die Haut möglich.
3 Toxikokinetik
Soweit untersucht, werden eingeatmete Alkanale rasch aufgenommen, im Körper verteilt, zu Säuren umgewandelt und fast ausschließlich mit dem Harn ausgeschieden. Invitro- und Invivo-Studien zeigen, dass gesättigte aliphatische Aldehyde rasch zu ihren korrespondierenden Säuren abgebaut werden. Die Aldehyde werden dabei durch die Aldehyddehydrogenase (ALDH) oxidiert [8].
Für die ALDH sind unterschiedliche Sequenzvarianten beim Menschen bekannt. Allerdings beschränkt sich dieser genetische Polymorphismus des ALDH2-Gens überwiegend auf die Bevölkerung des asiatischen Raums. Wang et al. [9] untersuchten den Einfluss von Polymorphismen des ALDH2-Gens auf den Metabolismus verschiedener Aldehyde an menschlichen mitochondrialen und zytosolischen Leberzellfraktionen. Im Ergebnis zeigte sich, dass Polymorphismen im ALDH2-Gen zu einer signifikanten Reduzierung der Metabolisierungsleistung unter anderem von n-Butanal, Hexanal und Heptanal führten. Unter den untersuchten Bedingungen wurde keine verringerte Enzymaktivität gegenüber Octanal und Decanal gefunden.
Tabelle 4: Vorkommen von azyklischen Alkanalen in der Luft von Schulräumen 2004 - 2005 (n = 165) [5]
| Aldehyd | n | Median [µg/m3] | 95. Perzentil [µg/m3] |
| Butanal | 165 | <1 | 2 |
| Pentanal | 76 | <1 | 2 |
| Hexanal | 165 | 6 | 14 |
| Octanal | 162 | 3 | 12 |
| Nonanal | 165 | 8 | 22 |
| Decanal | 165 | 4 | 15 |
Tabelle 5: Vorkommen von azyklischen Alkanalen in der Luft von Schulräumen und Kindergärten 2006 (n=273) [6]
| Aldehyd | n | Median [µg/ma] | 95. Perzentil [µg/m3] |
| Butanal | 273 | <1 | 3 |
| Pentanal | 273 | <1 | 5 |
| Hexanal | 273 | 1 | 11 |
| Heptanal | 273 | <2 | 2 |
| Octanal | 273 | <2 | 2 |
| Nonanal | 273 | 1 | 12 |
| Decanal | 273 | <2 | <2 |
4 Gesundheitliche Wirkung von C4-bis C11- gesättigten n- und isoaliphatischen Aldehyden
Hinsichtlich ihrer toxischen Eigenschaften sind in der Gruppe der aliphatischen Aldehyde vor allem die kurzkettigen Aldehyde gut untersucht. Alkanale wie zum Beispiel Methanal, Ethanal und auch ungesättigte Aldehyde wie zum Beispiel Propenal und trans-Butenal und das über zwei Aldehyd-Gruppen verfügende Glutaraldehyd weisen eine sehr starke irritative und nach Langzeitexposition auch eine tierexperimentell belegte Krebs erzeugende Wirkung in den Atemwegen auf.
Eine Reizwirkung auf den oberen Atemtrakt ist auch bei den höheren nichtzyklischen Alkanalen grundsätzlich vorhanden, aber im Vergleich mit den genannten kurzkettigen Alkanalen oder den zyklischen Aldehyden um mindestens zwei Größenordnungen geringer ausgeprägt [10]. Eine chronische Reizung verändert vor allem das Riechgewebe; eine Krebs erzeugende Wirkung wurde nicht beobachtet. Systematisch untersucht worden ist dies allerdings nur am Isobutanal, für das im Rahmen des US-amerikanischen Toxikologieprogramms Langzeittoxizitäts- und Kanzerogenitätsstudien durchgeführt worden sind. Vergleichbare Studien für die anderen gesättigten aliphatischen Aldehyde wurden nicht gefunden.
4.1 Inhalative Irritation
Tierexperimentelle Studien
Die sensorische Reizwirkung von eingeatmeten Alkanalen im Atemtrakt von Mäusen wurde in einer standardisierten Untersuchung (Nur-Kopf-Exposition) an Mäusen [11] ermittelt. Ziel war die Bestimmung der Konzentration, die zu einer 50 %igen Abnahme der Atemrate (respiratorische Dosis - RD50) führte. RD50-Werte liegen für die meisten C4 bis C6-Alkanale vor [10] (Tabelle 8). Eine eindeutige Abhängigkeit der Reizwirkung mit der Kettenlänge ergab sich nicht [12].
Tabelle 6: Vorkommen von azyklischen Alkanalen in der Luft von Büroräumen 2005 - 2008 unter Betriebsbedingungen (anlassbezogene Messung nach 3 Stunden ohne Lüftung) [7]
| Aldehyd | n | Median [µg/m3] | 95. Perzentil [µg/m3] | Maximalwert [µg/m3] |
| Butanal | 98 | <5 | 10 | 17 |
| 3-Methylbutanal | 98 | <5 | 6 | 12 |
| Pentanal | 98 | <5 | 18 | 38 |
| Hexanal | 98 | 7 | 42 | 79 |
| Heptanal | 59 | <5 | 6 | 8 |
| Octanal | 59 | <5 | <5 | 6 |
| Nonanal | 59 | 6 | 15 | 26 |
| Decanal | 59 | <5 | 6 | 7 |
Tabelle 7: Vorkommen von azyklischer C 4- bis C11 Alkanale in der Innenraumluft bei anlassbezogenen Messungen (v.a in zeitlicher nähe zu Renovierungen) in Deutschland 2002 - 2006. Bei den 2462 untersuchten Innenräumen handelte es sich überwiegend um Büroräume (n=984), Wohnungen (n = 738) und Schulräumen (n = 295), die jeweils mindestens 8 Stunden nicht gelüftet worden waren [4].
| Aldehyd | n | n > NG (%> NG) | Median [µg/m3] | 95. Perzentil [µg/m3] | Maximalwert [µg/m3] |
| Butanal | 1742 | 1343 (77) | 3 | 17 | 260 |
| 3-Methylbutanal | 176 | 0 (0) | 1 | 2 | 2 |
| Pentanal | 2297 | 2052 (89) | 5 | 36 | 197 |
| Hexanal | 2318 | 2242 (96) | 14 | 106 | 1301 |
| 2-Ethylhexanal | 342 | 7 (2) | < 1 | < 1 | 140 |
| Heptanal | 2109 | 1556 (74) | 2 | 11 | 62 |
| Octanal | 2100 | 1638 (78) | 3 | 13 | 49 |
| Nonanal | 2309 | 2027 (88) | 7 | 28 | 150 |
| Decanal | 2051 | 1135(55) | 2 | 10 | 160 |
| Undecanal | 329 | 138 (42) | <1 | 2 | 4 |
| F C4-C11-Alkanale | 329 | n.a. | 48 | 181 | 683 |
In einer subchronischen Ganzkörperinhalationstudie (sechs Stunden/Tag, fünf Tage/Woche über 13 Wochen) an männlichen und weiblichen F334-Ratten gegenüber 0, 360,1450 oder 5800 mg n-Butanal/ m3 zeigte sich bei allen Expositionskonzentrationen eine signifikante Zunahme der Umwandlung der Geruchszellen in Plattenepithelgewebe (squamöse Metaplasie). In einer 12-Wochen-Folgestudie, bei der männliche und weibliche Ratten gegenüber 0, 3, 30 oder 150 mg/m3 exponiert wurden, ergaben sich keine Veränderungen am nasalen, olfaktorischen oder respiratorischen Epithel. Beide Studien liegen nur als Zusammenfassung vor [8]. Auch an Beagle-Hunden ließen sich nach 14-wöchiger Exposition an sechs Stunden pro Tag und fünf Tagen pro Woche gegenüber 0, 360, 1450 oder 5800 mg Butanal/ m3 in allen exponierten Gruppen Zellhyperplasien der Nasenschleimhaut beobachten; bei der höchsten Dosis traten Entzündungen und schuppiges Gewebe in der Nase auf [8].
Richtwerte für gesättigte azyklische aliphatische C4- bis C17-Aldehyde in der Innenraumluft. Mitteilungen der Adhoc-Arbeitsgruppe Innenraumrichtwerte der Innenraumlufthygiene-Kommission des Umweltbundesamtes und der Obersten Landesgesundheitsbehörden
Zusammenfassung
Zum Schutz der Gesundheit der Bevölkerung setzt die Adhoc-Arbeitsgruppe Innenraumrichtwerte des Umweltbundesamtes und der Obersten Landesgesundheitsbehörden Richtwerte für die Innenraumluft fest. Für eine gesundheitliche Bewertung von n- und i-Alkanalen mit mindestens 4 C-Atomen in der Raumluft liegen keine geeigneten Humanstudien vor. Aus tierexperimentellen Untersuchungen ergibt sich die Reizwirkung im Atemtrakt als kritische Wirkung von C4- bis C6-Alkanalen; systematische Untersuchungen liegen jedoch nur für C4-Alkanale vor. In subchronischen Studien an n-Butanal und chronischen Studien an Isobutanal zeigten sich Entzündungen mit nichtneoplastischen und degenerativen Veränderungen des Nasenepithels. Die Adhoc-Arbeitsgruppe schätzt für Butanal einen LAEL für kontinuierliche Exposition von 16 mg Butanal/m3 ab. Unter Verwendung eines Extrapolationsfaktors von I für Interspeziesunterschiede und von 10 für die interindividuelle Variabilität der Reizwirkung ergibt sich ein Richtwert II (Gefahrenrichtwert) für Butanal von 2 mg/m3. Angesichts des derzeitigen Kenntnisstandes zur Reizwirkung einer inhalativen Exposition gegenüber C5- bis C11-Alkanalen empfiehlt die Adhoc-Arbeitsgruppe, den genannten Richtwert II von 2 mg/m3 auf die gesamte Gruppe der azyklischen C4- bis C11-Alkanale anzuwenden. Erhöhte C4- bis C11-Alkanal-Konzentrationen fallen in Innenräumen durch ihren Geruch auf. Zum Schutz vor Geruchsbelästigungen schlägt die Adhoc-Arbeitsgruppe einen Richtwert I (Vorsorgerichtwert) von 0,1 mg azyklische C4- bis C11-Alkanale/m3 Raumluft vor.
Schlüsselwörter
Aliphatische Aldehyde - Alkanale Innenraumluft - Irritation - Geruch - Richtwert
Indoorair guideiine values for saturated acydic aliphatic C4- C11 aldehydes
Abstract
To protect public health the German Working Group on Indoor Guidelines of the Federas Environmental Protection Agency and the States´Health Authorities is issuing indoor air guideline values. For health evaluatian of indoor air n- and ialkanals with at least 4 C atoms no appropriate human data is available. Based on animal studies irritation has been identified as crucial adverse effect following inhalative exposure to C4 to C6 alkanals. However, sufficient data is available for C4 alkanals only. Inflammation of the pose epithelium followed by nonneoplastic and degenerative lesions has been seen in inhalative subchronic studies with butanal and chronic studies with ibutanal. The lowest adverse effect level for continuous exposure is assessed by the Working Group as 16 mg butanal per cubic meter. By applying an interspecies factor of 1 and an intraspecies factor of 10 a socalled health hazard value of 2 mg butanal/m3 indoor air is obtained. Regarding the few and limited data on Inhalation toxicity of the higher homologues concerning irritation a health hazard value of 2 mg/m3 indoor air for the totai of acyclic C4 to C11 alkanals is recommended. Elevated C4 to C11 alkanal indoor air concentrations a n noy by odour. To prevent from unpleasant odour a socalled health precaution value of 0.1 mg acyclic C4 to C11 alkanals/m3 indoor is recommended.
Keywords
Aliphatic aldehydes - Alkanals - Indoor air - Irritation Odour - Guideline values
Die inhalative Langzeittoxizität von Isobutanal wurde in vier umfassend dokumentierten Studien an 6 Wochen alten männlichen und weiblichen F344/N-Ratten beziehungsweise B6C3 F1-Mäusen jeweils über 13 Wochen bzw. über 105 Wochen untersucht [13]. Die Exposition betrug an fünf Tagen pro Woche über sechs Stunden pro Tag in der subchronischen Studie jeweils 0, 1450, 2900, 5800, 11.600 oder 23.000 mg/m3 und in der chronischen Studie 0,1450, 2900 oder 5800 mg/ m3. In der subchronischen Studie an männlichen Ratten fiel ab einer Dosis von 1450 mg Isobutanal/m3 eine signifikante Senkung der epididymalen Spermienbeweglichkeit in den beiden unteren Dosisgruppen auf; dieser Effekt war jedoch nicht dosisabhängig (Tabelle 9). Bei den höheren Konzentrationen zeigten sich eitrige Entzündungen, Plattenepithelmetaplasien und Degeneration des Riechepithels bei Ratten und Mäusen beider Geschlechter.
In den Langzeitstudien an Ratten traten diese nasalen nichtneoplastischen Veränderungen ebenfalls bei den beiden höchsten Konzentrationen auf, bei weiblichen Ratten bereits ab 1450 mg Isobutanal/m3; bei den Mäusen waren die Effekte nicht so stark ausgeprägt (Tabelle 10). In keiner der vier Studien wurde eine Zunahme des Auftretens von Tumoren beobachtet. Parameter der Reproduktionstoxizität (Spermienbeweglichkeit oder Vaginalzytologie) wurden in den Langzeitstudien nicht evaluiert [13, 14].
Tabelle 8: Sensorische Reizwirkung von C 4- bis C5-Alkanalen im Atemtrakt von Mäusen [10]. Die Swiss-Webster-Maus wird als Standardteststamm empfohlen [11 ]
| Aldehyd | RD50 (Swiss-Webster-Maus) [mg/m3] |
| Butanal | 3050 |
| Methylpropanal | 12.500 |
| Pentanal | 3920 |
| 3-Methylbutanal | 3530 |
| Hexanal | 4320 |
| 2-Ethylbutanal | 3540 |
Humanstudien
Die sensorische trigeminale Reizwirkung ausgewählter gesättigter aliphatischer Aldehyde beim Menschen wurde nach einer intranasalen, einige Sekunden währenden Applikation bestimmt. Um eine Geruchswahrnehmung möglichst auszuschließen, wurde diese Untersuchung an vier als anosmisch eingestuften Probanden durchgeführt (deren Unvermögen, einen Geruch wahrzunehmen (Anosmie), war entweder angeboren oder infolge eines Unfalls oder einer Infektion entstanden). Folgende trigeminale Reizschwellen wurden ermittelt: Butanal 189.000 mg/m3, Pentanal 143.000 mg/ m3, Hexanal 23.300 mg/m3, Heptanal 5900 mg/m3, Octanal 15.000 mg/m3. Die Autoren stuften den Wert für Octanal als unsicher ein, da nur zwei der vier Probanden eine trigeminale irritative Wirkung von Octanal angaben [15].
Reizungen des menschlichen Auges ließen sich nach einer 6-sekündigen Exposition gegenüber Aldehyden noch bis zum Undecanal erzeugen, Dodecanal zeigte keine irritative Wirkung am Auge [16].
In einer Kammeruntersuchung wurden zwölf gesunde Probanden (sechs Männer und sechs Frauen im Alter von 21 bis 28 Jahren) zwei Stunden lang gegenüber 0, 8 oder 40 mg Hexanal/m3 exponiert. Bei beiden Expositionen gegenüber Hexanal wurden veränderte Geschmackswahrnehmungen angegeben. Nach zwei Stunden zeigten sich bei der höchsten Konzentration leichte Reizungen der Augen (vermehrtes Blinzeln) und es wurden Kopfschmerzen berichtet. Von den untersuchten neun Lungenfunktionsparametern war einer (der forcierte expiratorische Fluß bei 75% der Vitalkapazität - FEF75) während der Exposition signifikant erhöht, normalisierte sich aber in der Nachexpositionszeit wieder. Entzündungsmarker im Plasma waren nicht eindeutig erhöht [17].
In verschiedenen Studien wurden beim Menschen Reizungen im Atemtrakt mit einer erhöhten Exposition gegenüber Aldehyden (Hexanal und Nonanal) in Verbindung gebracht [18, 19, 20].
Tabelle 9: Reproduktionstoxizität (epididymale Rattenspermien) nach subchronischer inhalativer Exposition gegenüber Isobutanal [13]
| Konzentration [mg Isobutanal/m30] | 0 | 1450 | 2900 | 5800 | 11.600 |
| n (Anzahl Tiere) | 10 | 10 | 10 | 10 | 7 |
| Beweglichkeit [%] | 78 ± 7 | 17 ± 3 a | 20 ± 5 a | 80 ± 6 | 64 ± 13 |
| Abnormer Anteil [%] | 1,4 ± 0,2 | 1,6 ± 0,3 | 1,3 ± 0,2 | 1,5 ± 0,3 | 2,0 ± 0,3 |
| Konzentration [106/g epididymales Gewebe] | 348 ± 60 | 321 ± 53 | 433 ± 71 | 342 ± 54 | 293 ± 95 |
| a) Signifikant unterschiedlich (p < 0,01) zur Kontrollgruppe | |||||
Tabelle 10: Nichtneoplastische Effekte in der Nase von F344/N-Ratten (n = 50 je Geschlecht) und B6C3F1-Mäusen (n = 50 je Geschlecht) nach chronischer inhalativer Exposition gegenüber Isobutanal. In der Klammer ist der durchschnittliche Schweregrad der Schädigung angegeben (Stufe 1: minimal, 2: mild, 3: mäßig, 4: ausgeprägt) [13]
| Konzentration [mg Isobutanal/m3] | 0 | 1450 | 2900 | 5800 | |
| Eitrige Entzündungen | Ratte, m | 5 (3) | 3 (3) | 6 (2) | 15 (2) a |
| Ratte, w | 2 (2) | 3 (2) | 5 (3) | 11 (2) (a) | |
| Maus, m | 0 | 0 | 0 | 0 | |
| Maus, w | 0 | 0 | 0 | 0 | |
| Respiratorisches Epithel Schuppige Metaplasie | Ratte, m | 1 (2) | 1 (2) | 10 (2) a | 44 (2) a |
| Ratte, w | 1 (2) | 11 (1) a | 9(1) (a) | 44(1) a | |
| Maus, m | 0 | 0 | 0 | 0 | |
| Maus, w | 0 | 0 | 0 | 0 | |
| Olfaktorisches Epithel Degeneration | Ratte, m | 0 | 0 | 3 (2) | 44 (1) a |
| Ratte, w | 0 | 0 | 2(1) | 45(1) a | |
| Maus, m | 0 | 0 | 11(1) a | 45(1) a | |
| Maus, w | 1 (1) | 1 (2) | 27 (1) a | 49 (2) a | |
| a) Signifikant unterschiedlich (p
< 0,01) zur Kontrollgruppe;
(a) (p < 0,05) | |||||
4.2 Geruchswirkungen
Bei der individuellen Geruchswahrnehmungsschwelle handelt es sich um die Konzentration eines Geruchsstoffes, die in der Hälfte der Darbietungen bei einem Probanden eine Geruchswahrnehmung auslöst. Die individuelle Geruchswahrnehmungsschwelle kann innerhalb einer Messreihe oder zu verschiedenen Untersuchungszeitpunkten variieren. Die bevölkerungsbezogene Geruchswahrnehmungsschwelle (GS50) stellt die Konzentration eines Geruchsstoffes dar, die in der Hälfte der Darbietungen bei einem Probandenkollektiv eine Geruchswahrnehmung auslöst.
Vielfach zitiert wird eine zusammenfassende Auswertung von Ergebnissen älterer Untersuchungen zur Geruchswahrnehmung von Alkanalen, bei der Geruchswahrnehmungsschwellen von Butanal bis Undecanal bis in den unteren µ g/m3-Bereich abgeschätzt wurden [21]. Da diese Auswertung Studien unterschiedlicher Qualität einbezogen hat, lässt sich die Zuverlässigkeit der genannten Angaben zur Geruchsschwelle schwer beurteilen. Beispielhaft sei die maßgebliche Untersuchung von Guadagni et al. [22] vorgestellt. In dieser umfangreichen Untersuchung (n=25 Probanden) konnten Geruchswahrnehmungsschwellen wegen der sehr niedrigen Konzentrationen des jeweiligen Aldehyds in der Gasphase über der wässrigen Testlösung nicht direkt bestimmt werden, sondern mussten über zusätzlich ermittelte Verteilungsgleichgewichte abgeschätzt werden, die ihrerseits mit Unsicherheiten behaftet sind [22]. Bislang liegt nur eine Studie vor, die heutigen Anforderungen an die Bestimmung von Geruchswahrnehmungsschwellen entspricht [15]. Die dabei ermittelten Geruchswahrnehmungsschwellen von n-Butanal bis n-Octanal sind in Tabelle 11 aufgeführt. Vom Pentanal bis zum Octanal sinken die Geruchswahrnehmungsschwellen um drei Größenordnungen. Angesichts der Unsicherheiten der Angaben in der Literatur erscheint es geboten, mit den heutzutage zur Verfügung stehenden Methoden und Normvorgaben die Geruchswahrnehmungsschwellen gesättigter aliphatischer Aldehyde zu bestimmen.
Tabelle 11: Geruchswahrnehmungsschwelle Colf ausgewählter Aldehyde [15]
| Aldehyd | colf [mg/m3] N = 7 Nichtraucher |
| Butanal | 9 |
| Pentanal | 20 |
| Hexanal | 0,25 |
| Heptanal | 0,15 |
| Octanal | 0,02 |
Messverfahren: Wiederholte aufsteigende Exposition bei alternativer zweifacher Auswahl. Bei dieser Versuchsanordnung werden dem Probanden in unregelmäßiger Reihenfolgezwei Quetschflaschen mit beziehungsweise ohne Stimulus überreicht. Eine Quetschflasche ist zur Hälfte mit der zu riechenden, in Öl gelösten Substanz gefüllt. Die Konzentration der Geruchssubstanz im Dampfraum über der jeweiligen Lösung wird gaschromatografisch bestimmt. Aufgrund von Vorversuchen wird bei einer bestimmten Konzentrationsstufe unterhalb der vermuteten Geruchswahrnehmungsschwelle begonnen. Der Auslass der ersten Quetschflasche wird in ein Nasenloch geführt, die Quetschflasche gedrückt und das über dem Öl stehende, ausgepresste Gas für einige Sekunden gerochen. Dieser Vorgang wird mit der anderen Flasche im selben Nasenloch wiederholt. Der Proband wird aufgefordert, die Flasche zu nennen, die den stärkeren Geruchsreiz enthalten hat. Falls die Antwort nicht zutrifft, wird der Versuch mit der nächsten höheren Konzentrationsstufe der Verdünnungsreihe wiederholt. Die Stimuli werden abwechselnd jeweils einem Nasenloch angeboten. Die Versuchsreihe wird fortgesetzt, bis der Proband eine bestimmte Verdünnungsstufe 5-mal richtig angegeben hat. Eine Versuchsreihe umfasst in der Regel etwa 10 Tests pro Proband. Die Geruchswahrnehmungsschwelle Colf stellt den Median der untersuchten Kohorte dar.
Aldehyde fallen durch einen charakteristischen Geruch auf. Hexanal weist einen sogenannten grünen Geruch nach frisch geschnittenem Gras oder Blättern mit einer talgigen Beinote auf; Heptanal und Octanal haben eine öligfettige Beinote. Isobutanal hat einen stechenden Geruch mit einer fruchtigen Note. Pentanal riecht stechendbittermandelartig und Decanal orangenschalenartig.
Gemische verschiedener Alkanale in Konzentrationen unterhalb der Geruchswahrnehmungsschwelle des jeweiligen Einzelstoffs sind geruchlich wahrnehmbar und zeigen somit eine partiell additive Geruchswirkung [23]. Da C4- bis C11-Alkanale in der Innenraumluft in der Regel als Gemisch - mit einem höheren Anteil von Hexanal und Nonanal - auftreten und in erhöhten Konzentrationen regelmäßig mit gesundheitlichen Beschwerden in Zusammenhang gebracht werden, ist zu fordern, auch die Geruchswahrnehmungsschwellen bestimmter Alkanal-Gemische zu ermitteln.
4.3 Mutagenität
Hinsichtlich des gentoxischen Potentials von C4- bis C11-Alkanalen liegen nur wenige Ergebnisse vor. Isobutanal zeigte sowohl bei der überwiegenden Zahl der Invitro- als auch der Invivo-Untersuchungen ein mutagenes Potenzial; allerdings wurde in allen zytogenetischen Invivo-Untersuchungen eine Dosis benutzt, bei der die Tiere starben. Pentanal wies in einigen Invitro-Tests ohne metabolische Aktivierung ein gentoxisches Potenzial auf, dieses verschwand jedoch nach metabolischer Aktivierung. Ingesamt gibt es keine überzeugenden Hinweise für ein mutagenes Potential von Pentanal [8]. In einer Invitro-Studie an menschlichen Leberzellen führte eine Exposition gegenüber Butanal, Pentanal, Hexanal oder Nonanal zu keiner signifikanten DNA-Reparatursynthese [24].
5 Gesundheitliche Bewertung von C4- bis C17- gesättigten n- und isoaliphatischen Aldehyden in der Innenraumluft
Zur Toxikologie dieser Substanzgruppe liegen nur wenige grundlegende Untersuchungen vor. Soweit gesättigte nichtzyklische aliphatische Aldehyde mit 4 oder mehr C-Atomen untersucht wurden, weisen sie ein schwaches irritatives Potenzial auf. In subchronischen Studien an Butanal und chronischen Studien an Isobutanal zeigten sich Entzündungen mit nichtneoplastischen und degenerativen Veränderungen des Nasenepithels. Eindeutige Hinweise auf eine Krebs erzeugende Wirkung von Isobutanal wurden nicht gefunden. Der Kenntnisstand zur Reizwirkung einer inhalativen Exposition gegenüber C7- bis C11-Alkanalen ist sehr gering; hier bedarf es dringend weiterer toxikologischer Untersuchungen.
5.1 Einstufungen und Regelungen
Am Arbeitsplatz gilt in Deutschland ein Grenzwert für Butanal von 64 mg/m3 [25]. Darüber hinaus existiert in einigen europäischen Ländern sowie in den USA ein Arbeitsplatzgrenzwert für Pentanal von 175mg/m3 [2].
Von der kalifornischen Umweltbehörde wurde ein Verfahren zur Ableitung einer akuten Expositionskonzentration (reference exposure level - REL1h) vorgeschlagen, unterhalb der nach einer einstündigen Exposition keine nachteiligen gesundheitlichen Wirkungen für die Allgemeinbevölkerung zu erwarten sind [26]. Für die meisten C4- bis C6-Alkanale ergaben sich nach diesem Verfahren REL1h-Werte in der Größenordnung um ro-20mg/m3 (Tabelle 12).
5.2 Ableitung von Richtwerten für C4- bis C11- gesättigte n- und isoaliphatische Aldehyde in der Innenraumluft
Nach Auffassung der Adhoc-Arbeitsgruppe Innenraumrichtwerte stellt die Reizwirkung auf den Atemtrakt die wesentliche Wirkung einer inhalativen Exposition gegenüber gesättigten aliphatischen Aldehyden mit 4 oder mehr C-Atomen dar. Dies wurde tierexperimentell für einzelne n- oder i-Alkanale in mehreren Kurzzeitstudien, in subchronischen und in Langzeitstudien an Mäusen und Ratten sowie in wenigen Humanstudien belegt.
In einer Humanstudie zur Untersuchung der irritativen Wirkung einer akuten inhalativen Exposition gegenüber Hexanal nennen die Autoren als niedrigste Konzentration mit einer nachteiligen Wirkung (lowest observed adverse effect level - LOAEL) einen Wert von 40 mg/m3 nach zweistündiger Exposition [17]; dieser LOAEL steht größenordnungsmäßig im Einklang mit dem tierexperimentell abgeleiteten REL1h von 19 mg Hexanal/m3 (s. Abschnitt 5.1, Tabelle 12), bei dem nach einstündiger Exposition keine nachteiligen gesundheitlichen Wirkungen zu erwarten sind. Die Adhoc-Arbeitsgruppe sieht diese akute Humanstudie jedoch als ungeeignet für eine Ableitung von Richtwerten an, da erhebliche Unsicherheiten bestehen, wie von einer akuten auf eine chronische Exposition extrapoliert werden könnte, und fordert deshalb mindestens eine subakute Humanstudie. Immerhin lässt sich aus der bereits vorliegenden Humanstudie abschätzen, dass ein LAEL bei chronischer Exposition im unteren mg/m3-Bereich liegen dürfte.
Zur Ableitung von Richtwerten für azyklische C4- bis C11-Alkanale in der Innenraumluft greift die Adhoc-Arbeitsgruppe deshalb auf Ergebnisse tierexperimenteller Untersuchungen zurück. Sie hält die subchronische Inhalationsstudie mit n-Butanal an Ratten [8] für hinreichend aussagekräftig und zieht diese für die Ableitung eines Richtwertes für Butanal heran. Die Ergebnisse dieser Studie werden durch die Ergebnisse der subchronischen und chronischen Inhalationsstudien an Isobutanal unterstützt. Butanal wird wegen der im Vergleich zu Isobutanal stärkeren irritativen Wirkung gewählt.
Gemäß Basisschema [27] geht die Adhoc-Arbeitsgruppe zur Festsetzung von Richtwerten für die Innenraumluft vom LOAEL aus. In der subchronischen Studie traten bei einer sechsstündigen Exposition an fünf von sieben Tagen ab 360 mg Butanal/m3 bei Ratten beiden Geschlechts entzündungsbedingte Gewebeschäden am Riechepithel auf. Diese Veränderungen wurden als advers angesehen und 360 mg Butanal/m3 als LOAELsubchron eingestuft [8]. Zur Abschätzung einer chronischen Expositionskonzentration (LAELchron) verwendet die Adhoc-Arbeitsgruppe den vom Ausschuss für Gefahrstoffe vorgeschlagenen Faktor 4 zur Zeitextrapolation bei lokalen Effekten von subchronischer auf chronische Exposition [28] und extrapoliert auf eine kontinuierliche Exposition. Daraus ergibt sich für den LAELchron, Ratte ein Wert von 360 / 4*6/24*5/7 = 16 mg Butanal/m3.
Zur Interspeziesextrapolation wird üblicherweise ein Faktor von 10 verwendet. Dieser Extrapolationsfaktor gilt jedoch nur für sytemische Wirkungen, aber nicht für lokale Effekte im Atemtrakt [28]. Hier bestimmt die Dosis eines Stoffes (beziehungsweise seiner wirksamen Metaboliten) pro Fläche das Ausmaß der toxischen Reaktion. Hinsichtlich lokaler Effekte in den Atemwegen sind Ratten empfindlicher als Menschen, da Ratten im Unterschied zum Menschen obligate Nasenatmer sind und über ein größeres olfaktorisches Epithel verfügen. Nach Auffassung des Ausschusses für Gefahrstoffe ist es deshalb ausreichend, beim Fehlen stoffspezifischer Daten im Prinzip die gleiche Empfindlichkeit von Mensch und Tier anzunehmen [28]. Die Adhoc-Arbeitsgruppe Innenraumrichtwerte folgt dieser Auffassung und setzt für den Interspeziesfaktor einen Wert von i an.
Für die interindividuelle Variabilität der inhalativen Irritation wurde ein Standardfaktor von 5 vorgeschlagen [29]. Dieser Faktor stützt sich auf Untersuchungen zur Variabilität von Effekten auf den Atemtrakt nach kurzzeitiger Exposition, die einen Faktor von 6 für das Verhältnis des 95. Percentils zum Durchschnitt ergab [30]. Auch hinsichtlich der interindividuellen Variabilität der Irritation in der Nase zeigte sich, dass die Mehrheit (97,5%) der Allgemeinbevölkerung mit einem Faktor 5 um die durchschnittliche nasale Reizschwelle geschützt ist [31]. Es wird angenommen, dass der Zugang einer Substanz zu den trigeminalen Nervenendigungen wesentlich von den Dicken der Schleimschicht in der Nase und des Präcornealfilms im Auge abhängt. Wesentliche Einflussfaktoren auf die Schichtdicke sind die Umgebungsfeuchtigkeit, höhere Raumtemperatur, bestimmte Krankheiten und bestimmte Medikamente, das Tragen von Kontaktlinsen sowie eine Bildschirmtätigkeit [32].
Tabelle 12: Referenzexpositionskonzentration, bezogen auf eine Stunde (reference exposure level - REL 1h). Berechnet nach [10] und [26]
| Aldehyd | REL1h [mg/m3] |
| Butanal | 13 |
| Methylpropanal | 95 |
| Pentanal | 18 |
| 3-Methylbutanal | 15 |
| Hexanal | 19 |
| 2-Ethylbutanal | 14 |
Eine besondere Empfindlichkeit von Kindern gegenüber Reizstoffen ist nicht bekannt. Einzelne Studien weisen auf eine erhöhte Empfindlichkeit im Alter gegenüber irritativen Substanzen hin, in anderen Studien zeigte sich keine eindeutige Altersabhängigkeit. Zur Abbildung dieser Unkenntnis der Altersabhängigkeit der Reizwirkung wurde ein Unsicherheitsfaktor von 2 als ausreichend angesehen [29].
Die Adhoc-Arbeitsgruppe hat darüber hinaus betrachtet, ob angesichts des im Abschnitt Toxikokinetik vorgestellten genetischen Polymorphismus des Aldehyddehydrogenase (ALDH2)-Gens ein zusätzlicher Unsicherheitsfaktor notwendig ist. Im Fall des Propanals hat die US-amerikanische Umweltbehörde keinen zusätzlichen Unsicherheitsfaktor verwendet [33]. Da in der Untersuchung von Wang et al. [9] (siehe Abschnitt 3) die Wirkung von Butanal, Hexanal, Heptanal, Octanal oder Decanal im Vergleich zum Propanal schwächer ausgeprägt war, lässt sich nach Ansicht der Adhoc-Arbeitsgruppe ein zusätzlicher Unsicherheitsfaktor zur Berücksichtigung von
ALDH-Polymorphismen nicht ausreichend begründen. Vor diesem Hintergrund hält die Adhoc-Arbeitsgruppe einen Gesamtfaktor für die interindividuelle Variabilität der Reizwirkung von 5 X 2 =10 für angemessen. Damit ergibt sich für den Richtwert II ein Wert von 16/:L/10 = gerundet 2 mg Butanal/m3; der Richtwert 1 wird entsprechend zu 0,2mg Butanal/m3 festgesetzt.
Da das Butanal nur eines von mehreren Alkanalen in der Innenraumluft darstellt, stellte die Adhoc-Arbeitsgruppe Überlegungen an, wie die Gesamtgruppe der azyklischen C4 C11-Alkanale gesundheitlich zu bewerten ist. Eine grundsätzliche Schwierigkeit sieht die Adhoc-Arbeitsgruppe darin, dass der Kenntnisstand zur Toxizität dieser Verbindungen, insbesondere der n- und i-Alkanale mit 7 und mehr C-Atomen, sehr begrenzt ist. Hinsichtlich der Reizwirkung im Atemtrakt der Maus liegen Ergebnisse für ausgewählte geradkettige und verzweigte C4 - C6-Alkanale vor; hierbei zeigte sich eine vergleichbare Wirkungsstärke dieser Substanzen (Tabelle 8). Dagegen nahm bei der Untersuchung von Probanden mit fehlendem Geruchssinn die irritative Wirkungsstärke der C4 - C8-Alkanale mit ansteigender Kohlenstoffzahl zu. Aus Sicht der Adhoc-Arbeitsgruppe Innenraumrichtwerte sind diese Ergebnisse in regulatorischer Hinsicht wegen der besonderen experimentellen Bedingungen schwer zu bewerten, da die Exposition nur wenige Sekunden betrug, es sich um eine sehr untypische Personengruppe mit einem chronischen Leiden handelte, die untersuchte Gruppe nur vier Probanden umfasste und eine partielle Anosmie, die die Ergebnisse zumindest teilweise erklären könnte, nicht vollständig ausgeschlossen werden kann. Auch die Autoren der Studie sehen die sehr kurze Expositionszeit sowie die unterschiedliche Expositionsart als wesentliche Ursachen für die unterschiedlichen Ergebnisse der Human- und tierexperimentellen Studien an [15]. Für die Verwendung der Ergebnisse der tierexperimentellen RD50-Untersuchungen spricht dagegen die allgemein gute Korrelation dieser Daten mit Humandaten zur Reizschwelle [34] und die übliche Verwendung von tierexperimentellen Reizwirkungsdaten als ein Kriterium bei der Ableitung von Arbeitsplatzgrenzwerten [26, 29, 35, 36].
Angesichts des gegenwärtigen Kenntnisstandes geht die Adhoc-Arbeitsgruppe vereinfachend von einem zum Butanal vergleichbaren Wirkungsprofil aller geradkettigen und verzweigten azyklischen C4- bis C11-Alkanale aus und setzt folgenden Summenrichtwert II für diese Gruppe fest:
Summenrichtwert 11 = 2 mg C4 bis C11-gesättigten- und isoaliphatische Aldehyde pro Kubikmeter Raumluft.
Gemäß Basisschema [27] ergäbe sich ein Summenrichtwert I von 0,2 mg C4- bis C11-gesättigten n- und isoaliphatischen Aldehyden pro Kubikmeter Raumluft. Nach Auffassung der Adhoc-Arbeitsgruppe berücksichtigt dieser Summenrichtwert I jedoch nicht ausreichend die Geruchsproblematik höherer Alkanale. Beispielsweise lässt sich aus den Tabellen 3, 6 und 7 ein Octanal-Anteil von 4 bis 7 % am Gesamtgemisch der C4- bis C11-Alkanale abschätzen, dies entspräche beim genannten Summenrichtwert I einer Octanal-Konzentration um 0,01 mg/m3 und läge damit nahe an der Geruchswahrnehmungsschwelle von 0,02 mg Octanal/m3, die in der als valide eingeschätzten Studie von Cometto-Muniz et al. [15] für Octanal (Tabelle 11) ermittelt wurde. Die Adhoc-Arbeitsgruppe hält deshalb einen zusätzlichen Unsicherheitsfaktor von 2 für angemessen und setzt folgenden Summenrichtwert I fest:
Summenrichtwert 1 = 0,1 mg C4- bis C11-gesättigte n- und isoaliphatische Aldehyde pro Kubikmeter Raumluft.
Die Adhoc-Arbeitsgruppe Innenraumrichtwerte weist an dieser Stelle noch einmal ausdrücklich darauf hin, dass die genannten Summenrichtwerte weder für die kurzkettigen (Anzahl der C-Atome < 4) noch für die zyklischen, ungesättigten oder mehrfachen Aldehyde gelten, bei denen starke Reizwirkungen im Vordergrund stehen. Insofern wird das Vorkommen dieser Aldehyde nicht in die Summenbildung einbezogen, vielmehr müssen diese Aldehyde getrennt bewertet werden.
Anmerkungen
Der Text dieser Empfehlung wurde federführend von Dr. Helmut Sagunski und Dr. Jutta Witten mit Beiträgen von Christoph Baudisch, Dr. Hermann Fromme, Dr. Birger Heinzow, Dr. Wolfgang Heger, Thomas Lahrz, Dr. Inge Mangelsdorf und Dr. Ludwig Müller erstellt und von der Adhoc-Arbeitsgruppe Innenraumrichtwerte im März 2009 verabschiedet. I)ie Literaturrecherche wurde im Oktober 2008 abgeschlossen.
- Horn W, Jann 0, Kasche J, etal. (2007) Umwelt- und Gesundheitsanforderungen an Bauprodukte - Ermittlung und Bewertung derVOC-Emissionen und geruchlichen Belastungen. Texte 16/07. Umweltbundesamt (Hrsg.), Berlin. Unter: http://www. umweltdaten.de/publikationen/fpdf-I/3197.pdf
- AgBB (2008) Vorgehensweise bei der gesundheitlichen Bewertung der Emissionen von flüchtigen organischen Verbindungen (VOC) aus Bauprodukten. Ausschuss zur gesundheitlichen Bewertung von Bauprodukten. Unter: http://www. umweltbundesamt.de/bauprodukte/agbb.htm
- Umweltbundesamt (2008) Vergleichswerte für flüchtige organische Verbindungen (VOC und Aldehyde) in der Innenraumluft von Haushalten in Deutschland. Bundesgesundheitsbl Gesundheitsforsch Gesundheitsschutz 51:109-112
- Hofmann H, Plieninger P (2008) Bereitstellung einer Datenbank zum Vorkommen von flüchtigen organischen Verbindungen in der Raumluft. Arbeitsgemeinschaft Ökologischer Forschungsinstitute (AGÖF) e.V., Springe-Eldagsen. Umweltbundesamt (Hrsg.), Berlin. Unter: http://www. umweltdaten.de/publikationen/fpdf-1/3633.pdf
- Fromme H, Heitmann D, Dietrich S, etal. (2008) Raumluftqualität in Schulen - Belastungen von Klassenräumen mit Kohlendioxid (CO2), flüchtigen organischen Verbindungen (VOC), Aldehyden, Endotoxinen und Katzenallergenen. Gesundheitswesen 70:88-97
- Heinzow B (2008) Unveröffentlichte Messergebnisse des LAGA-SH, Kiel
- Baudisch C (2008) Unveröffentlichte Messergebnisse des LAGUS-MV, Schwerin
- OECD SIDS (2005) N-Vateraldehyde. UNEP Publications, Washington. Unter: http://www.inchem.org/ docu ments/sids/sids/110623.pdf
- Wang RS, NakajimaT, KawamotoT, HonmaT (2002) Effects of aldehyde dehydrogenase-2 genetic polymorphisms an rnetabolism of structurally different aldehydes in human liver. Drug Metab Dispos 30:69-73
- Steinhagen WH, Barrow CS (1984) Sensory irritation structureactivity study of inhaled aldehydes in B6C3F1 and Swiss-Webster mice.Toxicol Appl Pharmacol 72:495-503
- ASTM (1984) Standardtest method for estimating sensory irritation of airborne chemicals. Designation E 981-84. American Society for Testing and Materials, Philadelphia
- Alarie Y, Schaper M, Nielsen GD, Abraham MH (1998) Structureactivity relationships of volatile organic chemicals as sensory irritants. Arch Toxicol 72:125-140
- US-NTP (1999) NTPToxicology and carcinogenesis studies of isobutyraldehyde in F344/N rats and B6C3F1 mice (inhalation studies). Natl Toxicol Program Tech Rep Ser 472:1-242
- Abdo KM, Haseman JK, Nyska A (1998) Isobutyraldehyde administered by inhalation (whole body exposure) for up to thirteen weeks or two years was a respiratory tract toxicant but was not carcinogenic in F344/N rats and B6C3F1 mice.Toxicol Sci 42:136-151
- Cometto-Muniz JE, Cain WS, Abraham MH (1998) Nasal pungency and odor of homologues aldehydes and carboxylic acids. Exp Brain Res 118:180-188
- Cometto-Muniz JE, Cain WS, Abraham MH, Sanchez-Moreno R (2007) Cutoff in detection of eye irritation from vapors of homologous carboxylic acids and aliphatic aldehydes. Neuroscience 145:1130-1137
- Ernstgard L, Iregren A, Sjögren B, etal. (2006) Acute effects of exposure to hexanal vapors in humans. J Occup Environ Med 48:573-580
- Brown SK (2002) Volatile organic pollutants in new and established buildings in Melbourne, Australia. Indoar Air 12:55-63
- SaijoY, Kishi R, Sata F, etal. (2004) Symptoms in relation to chemicals and dampness in newly built dwellings. Int Arch Occup Environ Health 77: 461-470
- Schünemann D,Thumulla J (2004) Belastungen mit höheren Aldehyden durch OSB-Platten in einem Niedrigenergiehaus. In: Weber S (Hrsg.) Umwelt, Gebäude & Gesundheit: Innenraumhygiene, Raumluftqualität und Energieeinsparung. Ergebnisse des 7. Fachkongresses der Arbeitsgemeinschaft Ökologischer Forschungsinstitute (AGÖF) am 4. und 5. März 2004 in München. AGÖF e.V., Springe-Eldagsen:12 2-126
- Devos M, Patte F, RouaultJ, etal. (1990) Standardized human olfactory thresholds. IRL Press, Oxford
- Guadagni DG, Buttery RG, Okano S (1963) Odour thresholds of some organic compounds associated with food flavours. J Sci Fd Agric 14:761-765
- Guadagni DG, Buttery RG, Okano S, Burr HK (1963) Additive effect of subthreshold concentrations of some organic compounds associated with food aromas. Nature 200:1288-1289
- Martelli A, Canonero R, Cavanna M, etal. (1994) Cytotoxic and genotoxic effects of five nalkanes in primary cultures of rat and human hepatocytes. Mutat Res 323:121-126
- BMAS (2008) Arbeitsplatzgrenzwerte.Technische Regeln für Gefahrstoffe. TRGS 900. Bundesministerium für Arbeit und Sozialordnung. GMBl 28: 578-579. Unter: http://www.baua.de/nn_16806/ de/Themenvon-A-Z/Gefa hrstoffe/TRGS/ TRGS-900.html
- Kuwabara Y, Alexeeff GV, Broadwin R, Salmon AG (2007) Evaluation and application of the RD50 for determining acceptable exposure levels of airborne sensory irritants for the general public. Environ Health Perspect 115:1609-1616
- Adhoc-AG IRK/AOLG (1996) Richtwerte für die Innenraumluft: Basisschema. Bundesgesundheitsbl 39:422-426
- BMAS (2006) Begründungen und Erläuterungen zu Grenzwerten in der Luft am Arbeitsplatz. Technische Regeln für Gefahrstoffe.TRGS 901. Bundesministerium für Arbeit und Sozialordnung. BArbBI 1/2006: 55. Unter: http://www.baua.de/ nn_16806/de/Themenvon-A-Z/Gefahrstoffe/ TRG S/pdf/TRG S-901. pdf
- Nielsen GD, Wolkoff P, Alarie Y (2007) Sensory irritation: Risk assessment approaches. Regul Toxicol Pharmacol 48:6-18
- Alexeeff GV, Broadwin R, Liaw J, etal. (2002) Characterization of the LOAEL-to-NOAEL uncertainty factor for mild adverse effects from acute inhalation exposures. RegulToxicol Pharmacol 36:96-105
- Hau KM, Connel DW, Richardson BJ (2000) Use of partition models in setting health guidelines for volatile organic compounds. Regul Toxicol Pharmacol 31:22-29
- Wolkoff P (2008)"Healthy" eye in officelike environments. Environ Int 34:1204-1214
- US-EPA (2008) Toxicological review of propionaldehyde. Unter: http://www.epa.gov/iris
- Cain WS, Cometto-Muniz JE (1995) Irritation and odor as indicators of indoor pollution. Occup Med: State of the Art Rev 10:133-145
- Schaper M (1993) Development of a database for sensory irritants and its use in establishing occupational exposure limits. Am Ind Hyg Assoc J 54:488-544
- Paustenbach DJ, Gaffney SH (2006) The rote of odor and irritation, as well as risk perception, in setting of occupational exposure limits. Int Arch Occup Environ Health 79:339-342
- BGIA (2008) GESTIS-Stoffdatenbank. Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. Unter: http://www.dguv.de/bgia/ de/gestis/stoffdb/index.jsp
 | ENDE |  |
...
X
⍂
↑
↓
