umwelt-online: Verordnung (EG) Nr. 440/2008 zur Festlegung von Prüfmethoden gemäß der VO (EG) Nr. 1907/2006 zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH) (6)
 | zurück |
Teil B 23 24
Methoden zur Bestimmung der Toxizität und sonstiger Auswirkungen auf die Gesundheit
A. Charakterisierung der Prüfsubstanz
Die Zusammensetzung der Prüfsubstanz, einschließlich der Hauptverunreinigungen, ihre relevanten physikalischchemischen Eigenschaften sowie die Stabilität der Substanz müssen vor Beginn einer Toxizitätsuntersuchung bekannt sein.
Die physikalischchemischen Eigenschaften der Prüfsubstanz sind mitentscheidend für die Auswahl des Verabreichungsweges, die Art der einzelnen Prüfungen sowie für die Handhabung und Lagerung der Prüfsubstanz.
Der eigentlichen Untersuchung sollte daher die Entwicklung eines Analyseverfahrens zur qualitativen und quantitativen Bestimmung der Prüfsubstanz (möglichst einschließlich der Hauptverunreinigungen) im Verabreichungsmedium und im biologischen Material vorausgehen.
Alle Angaben bezüglich der Identifikation, der physikalischchemischen Eigenschaften, der Reinheit und des Verhaltens der Prüfsubstanz sollten im Prüfbericht enthalten sein.
B. Tierpflege
Eine strenge Kontrolle der Umweltbedingungen sowie eine den jeweiligen Tierarten angemessene Tierhaltung sind wesentliche Voraussetzungen für toxikologische Untersuchungen.
i) Haltungsbedingungen
Die Umgebungsbedingungen in den Versuchstierräumen sind der jeweiligen Tierart anzupassen. Für Ratten, Mäuse und Meerschweinchen ist eine Raumtemperatur von 22 °C ± 3 °C bei einer relativen Luftfeuchtigkeit von 30-70 % angezeigt; bei Kaninchen sollte die Temperatur 20 ± 3 °C bei einer relativen Luftfeuchtigkeit von 30-70 % betragen.
Einige Untersuchungsmethoden sind besonders empfindlich gegenüber Temperatureinflüssen. Für diese Fälle sind Einzelheiten über die entsprechenden Umgebungsbedingungen in der Beschreibung des Prüfverfahrens enthalten. Bei allen Untersuchungen auf toxische Wirkungen sind Temperatur und Luftfeuchtigkeit zu überwachen, aufzuzeichnen und in den Abschlussbericht der Untersuchung aufzunehmen.
Die Beleuchtung sollte künstlich sein und die Hell- und Dunkelphasen sollten sich im Abstand von 12 Stunden abwechseln. Einzelheiten des Beleuchtungsmusters sind aufzuzeichnen und in den Abschlussbericht der Studie aufzunehmen.
Sofern in der Beschreibung der Prüfmethode nichts anderes angegeben ist, sollten die Tiere einzeln oder in kleinen Gruppen aus Tieren desselben Geschlechts in Käfigen untergebracht sein. Bei Gruppenhaltung sollten maximal fünf Tiere in einem Käfig untergebracht sein.
In Berichten über Tierversuche ist unbedingt die Art der Käfighaltung sowie die Anzahl der in einem Käfig untergebrachten Tiere sowohl während der Exposition gegenüber der Prüfsubstanz als auch während der darauf folgenden Beobachtungszeit anzugeben.
ii) Fütterungsbedingungen
Das Futter muss allen ernährungswissenschaftlichen Anforderungen für die jeweils eingesetzte Spezies entsprechen. Werden den Tieren Prüfsubstanzen im Futter verabreicht, so kann der Nährwert durch Wechselwirkung zwischen der jeweiligen Substanz und einem Futterbestandteil eingeschränkt sein. Die Möglichkeit einer solchen Reaktion muss bei der Interpretation der Ergebnisse berücksichtigt werden. Es kann herkömmliches Labortierfutter verwendet werden bei uneingeschränkter Versorgung mit Trinkwasser. Die Auswahl des Futters kann auch dadurch mitbestimmt werden, dass eine geeignete Beimischung der Prüfsubstanz gewährleistet sein muss, wenn die Prüfsubstanz auf diese Art verabreicht werden soll.
Verunreinigungen im Futter, die sich nachweislich auf die Toxizität auswirken, dürfen nicht in störenden Konzentrationen vorhanden sein.
C. Alternative Prüfmethoden
Die Europäische Union ist fest entschlossen, die Entwicklung und Validierung alternativer Verfahren, welche dieselben Informationen liefern können wie die gegenwärtigen Tierversuche, aber weniger Tiere erfordern, weniger Leiden verursachen oder die Verwendung von Tieren völlig überflüssig machen, zu fördern.
Solche Methoden müssen, sobald sie zur Verfügung stehen, nach Möglichkeit für die Charakterisierung von Gefahren und die anschließende Einstufung und Kennzeichnung im Hinblick auf substanzeigene Gefahren in Betracht gezogen werden.
D. Bewertung und Interpretation
Bei der Auswertung und Interpretation von Tests sind gewisse Grenzen hinsichtlich der direkten Extrapolation der Ergebnisse der Tier- und In-vitro-Versuche auf den Menschen zu berücksichtigen; deshalb können Belege für unerwünschte Wirkungen beim Menschen, soweit solche vorliegen, zur Bestätigung der Versuchsergebnisse herangezogen werden.
E. Literaturhinweise
Die meisten dieser Methoden werden im Rahmen des OECD-Programms für Prüfrichtlinien entwickelt und sollten in Übereinstimmung mit den Grundsätzen der guten Laborpraxis durchgeführt werden, um eine möglichst breite gegenseitige Datenakzeptanz zu gewährleisten.
Weitere Informationen finden sich in den in den OECD-Richtlinien genannten Literaturangaben sowie in der an anderen Stellen publizierten einschlägigen Literatur.
B.1 bis - Akute orale Toxizität - Fest-Dosis-Methode
1. Methode
Diese Prüfmethode entspricht der OECD TG 420 (2001).
1.1 Einleitung
Herkömmliche Methoden zur Bewertung der akuten Toxizität verwenden den Tod der Versuchstiere als Endpunkt. 1984 hat die British Toxicology Society einen neuen Ansatz zur Bewertung der akuten Toxizität vorgeschlagen, der von der Verabreichung einer Serie fester Dosen ausging (1). Dieser Ansatz bezog sich nicht auf den Tod der Versuchstiere als Endpunkt, sondern stützte sich auf die Beobachtung deutlicher Toxizitätszeichen, die bei einer bestimmten Dosis aus einer Serie fester Dosierungen auftraten. Nach In-vivo-Validierungsstudien im Vereinigten Königreich (2) sowie in internationalem Rahmen (3) wurde das Verfahren im Jahre 1992 als Prüfmethode anerkannt. Später wurden die statistischen Eigenschaften der Fest-Dosis-Methode mit Hilfe mathematischer Modelle in einer Reihe von Studien berechnet (4) (5) (6). Mit In-vivo-Studien und anhand von Modellstudien konnte nachgewiesen werden, dass das Verfahren reproduzierbar ist, mit einer geringeren Anzahl an Versuchstieren auskommt und weniger Leiden verursacht als die herkömmlichen Methoden und eine ähnliche Bewertung der Substanzen ermöglicht wie die sonstigen Methoden zur Prüfung der akuten Toxizität.
Leitlinien für die Auswahl der geeignetsten Testmethode für einen bestimmten Zweck enthält das Guidance Document on Acute Oral Toxicity Testing (7). Dieser Leitfaden beinhaltet darüber hinaus weitere Informationen zur Durchführung und Auswertung der Prüfmethode B.1 bis.
Eines der Prinzipien der Methode besteht darin, dass in der Hauptstudie nur mäßig toxische Dosen eingesetzt werden und dass die Verabreichung von voraussichtlich letalen Dosen vermieden werden sollte. Außerdem brauchen keine Dosierungen verabreicht zu werden, die aufgrund ätzender oder stark reizender Wirkungen bekanntermaßen starke Schmerzen und schweres Leiden verursachen. Moribunde Tiere oder Tiere, die offensichtlich unter Schmerzen leiden oder Anzeichen von schwerem und anhaltendem Leiden zeigen, sind auf humane Weise zu töten und werden bei der Auswertung der Testergebnisse auf die gleiche Weise gewertet wie während des Tests gestorbene Tiere. Kriterien für die Entscheidung, moribunde oder schwer leidende Tiere zu töten, sowie Hinweise zur Erkennung des absehbaren oder bevorstehenden Todes sind Gegenstand eines gesonderten Leitfadens (8).
Die Methode führt zu Informationen über die gefährlichen Eigenschaften und ermöglicht die Bewertung und Klassifizierung der Substanz gemäß dem Globalen Harmonisierten System (GHS) zur Klassifizierung chemischer Stoffe mit akut toxischer Wirkung (9).
Das Prüflabor soll vor der Durchführung der Studie sämtliche verfügbaren Informationen berücksichtigen. Zu diesen Informationen gehören die Identität und die chemische Struktur der zu testenden Substanzen, die physikalischchemischen Eigenschaften der Substanzen, die Ergebnisse sonstiger In-vivo- oder In-vitro-Toxizitätstests in Verbindung mit den betreffenden Substanzen, toxikologische Daten über strukturverwandte Substanzen sowie die vorgesehene(n) Verwendung(en) der Substanzen. Diese Informationen werden benötigt, um die zuständigen Stellen zu überzeugen, dass der Test für den Schutz der menschlichen Gesundheit wichtig ist und bei der Wahl der geeigneten Startdosis hilft.
1.2 Definitionen
Akute orale Toxizität: Schädliche Wirkungen, die nach der oralen Verabreichung einer Einzeldosis oder mehrerer innerhalb von 24 Stunden verabreichter Dosen einer Substanz auftreten.
Verzögerter Tod: Das betreffende Tier stirbt zwar nicht binnen 48 Stunden und wirkt in diesem Zeitraum nicht moribund; der Tod tritt jedoch später während des 14-tägigen Beobachtungszeitraums ein.
Dosis: Verabreichte Menge der Testsubstanz; die Dosis wird als Gewicht der Testsubstanz pro Gewichtseinheit des Versuchstiers ausgedrückt (z.B. mg/kg).
Evidente Toxizität: Ein allgemeiner Begriff, der deutliche Anzeichen von Toxizität nach der Verabreichung einer Testsubstanz dahin gehend beschreibt, dass bei der nächsthöheren festen Dosis entweder starke Schmerzen und anhaltende Anzeichen für schweres Leiden, ein moribunder Zustand (Kriterien siehe Humane Endpoints Guidance Document (8)) oder wahrscheinlich der Tod der meisten Versuchstiere zu erwarten sind (siehe z.B. (3)).
GHS: Globally Harmonised Classification System for Chemical Substances and Mixtures (Weltweit harmonisiertes Klassifizierungssystem für chemische Substanzen und Gemische); ein gemeinsames Projekt von OECD (Menschliche Gesundheit und Umwelt), UN-Expertenausschuss für den Transport von Gefahrgütern (physikalischchemische Eigenschaften) und ILO (Gefahrenanzeige) koordiniert im Rahmen des Interorganisation Programme for the Sound Management of Chemicals (IOMC).
Bevorstehender Tod: Der moribunde Zustand oder Tod ist vor dem nächsten vorgesehenen Beobachtungszeitpunkt zu erwarten. Anzeichen für diesen Zustand können bei Nagetieren Krämpfe, Seitenlage, liegende Stellung und Tremor sein (siehe Humane Endpoint Guidance Document (8)).
LD50 (mittlere Letaldosis): Statistisch ermittelte Einzeldosis einer Substanz, bei der davon ausgegangen werden kann, dass sie bei oraler Verabreichung den Tod von 50 % der Tiere verursacht; der LD50-Wert wird als Gewicht der Testsubstanz pro Gewichtseinheit der Versuchstiere ausgedrückt (mg/kg).
Limit-Dosis: Dosis am oberen Grenzwert für den betreffenden Versuch (2.000 oder 5.000 mg/kg)
Moribunder Zustand: Zustand des Sterbens oder des Unvermögens, (selbst bei Behandlung) zu überleben (siehe Humane Endpoint Guidance Document (8))
Voraussagbarer Tod: Vorhandensein klinischer Zeichen, die auf den Eintritt des Todes zu einem bekannten Zeitpunkt in der Zukunft - vor dem planmäßigen Ende des Experiments - hinweisen, z.B. das Unvermögen, Wasser oder Nahrung aufzunehmen (siehe Humane Endpoint Guidance Document (8))
1.3 Prinzip der Prüfmethode
An Gruppen von Versuchstieren eines Geschlechts wird in einem schrittweisen Verfahren jeweils die feste Dosis 5, 50, 300 und 2.000 mg/kg verabreicht. (Im Ausnahmefall kann eine weitere feste Dosis von 5.000 mg/kg in Betracht gezogen werden (siehe Abschnitt 1.6.2)). Als Startdosis wird auf der Grundlage einer Vorstudie die Dosis gewählt, die voraussichtlich gewisse Toxizitätsanzeichen verursachen wird, ohne schwere toxische Wirkungen oder Mortalität hervorzurufen. Klinische Anzeichen und Zustände, die mit Schmerzen, Leiden und bevorstehendem Tod verbunden sind, werden in einem gesonderten OECD-Leitfaden (8) ausführlich beschrieben. Weiteren Versuchstiergruppen können höhere oder niedrigere feste Dosen in Abhängigkeit davon verabreicht werden, ob Anzeichen von Toxizität oder Mortalität zu erkennen sind. Diese Vorgehensweise wird fortgesetzt, bis die Dosis ermittelt ist, die offensichtlich toxisch wirkt oder den Tod maximal eines Versuchstieres verursacht hat, bzw. bis bei der höchsten Dosis keine Wirkungen zu erkennen sind oder bis bereits bei der niedrigsten Dosis der Tod von Versuchstieren eintritt.
1.4 Beschreibung der Prüfmethode
1.4.1 Auswahl der Tierspezies
Die bevorzugte Nagetierspezies ist die Ratte, es können aber auch andere Spezies verwendet werden. In der Regel werden weibliche Tiere verwendet (7). Weibliche Tiere werden bevorzugt, da die in der Literatur zitierten Untersuchungen zu konventionellen LD50-Tests zwischen den Geschlechtern in der Regel nur geringfügige Unterschiede hinsichtlich der Empfindlichkeit belegen, in den Fällen, in denen Unterschiede beobachtet werden, jedoch zeigen, dass weibliche Tiere im Allgemeinen etwas empfindlicher sind (10). Wenn jedoch die vorhandenen Informationen über die toxikologischen oder toxikokinetischen Eigenschaften von strukturverwandten Chemikalien darauf hinweisen, dass vermutlich die männlichen Tiere empfindlicher sind, sollten männliche Tiere verwendet werden. Wird ein Versuch an männlichen Tieren durchgeführt, sollte dies hinreichend begründet werden.
Es sollen junge, gesunde, ausgewachsene Tiere aus üblicherweise eingesetzten Laborstämmen verwendet werden. Die weiblichen Tiere dürfen weder bereits geworfen haben noch momentan trächtig sein. Alle Tiere müssen zu Beginn der Verabreichung zwischen 8 und 12 Wochen alt sein; ihre Gewichtswerte müssen im Bereich von ± 20 % des mittleren Gewichts sämtlicher zuvor verwendeter Tiere liegen.
1.4.2 Haltung und Fütterung
Die Temperatur des Versuchstierraums soll 22 °C (± 3 °C) betragen. Die relative Luftfeuchtigkeit soll mindestens 30 % betragen und außer während der Reinigung vorzugsweise nicht über 70 % liegen; anzustreben ist ein Wert von 50-60 %. Der Raum soll künstlich beleuchtet sein, wobei die Beleuchtung im 12-Stunden-Rhythmus ein- und ausgeschaltet werden soll. An die Versuchstiere kann herkömmliches Laborfutter verfüttert werden, wobei eine unbegrenzte Trinkwasserversorgung zu gewährleisten ist. Die Tiere können in den Käfigen nach Verabreichungsdosen gruppiert werden, wobei aber die Anzahl der Tiere pro Käfig noch eine genaue Beobachtung der einzelnen Tiere ermöglichen muss.
1.4.3 Vorbereitung der Versuchstiere
Die Tiere werden nach Zufallskriterien ausgewählt, zwecks Identifizierung markiert und für die Dauer von mindestens 5 Tagen vor Versuchsbeginn in ihren Käfigen gehalten, damit sie sich an die Laborbedingungen gewöhnen können.
1.4.4 Vorbereitung der Dosen
Generell sollen die Testsubstanzen mit einem für den gesamten zu testenden Dosierungsbereich gleichbleibenden Volumen verabreicht werden, indem jeweils die Konzentration der Dosiszubereitung variiert wird. Wenn jedoch ein flüssiges Endprodukt oder Gemisch zu testen ist, kann die Anwendung der unverdünnten, d. h. mit gleichbleibender Konzentration verabreichten Testsubstanz für die anschließende Risikobewertung der betreffenden Substanz größere Relevanz haben und wird daher von verschiedenen Behörden vorgeschrieben. In jedem Fall darf das maximal zu verabreichende Dosisvolumen nicht überschritten werden. Welches Flüssigkeitsvolumen jeweils höchstens auf einmal verabreicht werden kann, hängt von der Größe des Versuchstiers ab. Bei Nagetieren soll das Volumen im Normalfall 1 ml pro 100 g Körpergewicht nicht überschreiten; bei wässrigen Lösungen können aber auch 2 ml pro 100 g Körpergewicht in Betracht gezogen weiden. Bezüglich der Formulierung wird, wenn dies möglich ist, eine wässrige Lösung/Suspension/Emulsion empfohlen, danach in der Reihenfolge der Präferenz eine Lösung/Suspension/Emulsion in Öl (z. 8. Maisöl) sowie an dritter Stelle eventuell eine Lösung in anderen Vehikeln. Bei anderen Vehikeln als Wasser sollen die toxikologischen Eigenschaften des jeweiligen Vehikels bekannt sein. Die Dosen dürfen erst kurz vor der Verabreichung zubereitet werden, sofern die Zubereitung über den Zeitraum, in dem sie angewandt werden soll, nicht bekanntermaßen eine annehmbare Stabilität aufweist.
1.5 Verfahrensweise
1.5.1 Verabreichung der Dosen
Die Testsubstanz wird als Einzeldosis mit einer Sonde über eine Magensonde oder über eine geeignete Intubationskanüle verabreicht. In dem seltenen Fall, dass die Verabreichung als Einzeldosis nicht möglich ist, kann die Dosis über einen Zeitraum von maximal 24 Stunden in kleineren Teilmengen verabreicht werden.
Die Versuchstiere sollten vor der Verabreichung nüchtern sein (z.B. sollte Ratten das Futter (nicht das Wasser) über Nacht vorenthalten werden; Mäusen sollte das Futter (nicht das Wasser) 3-4 Stunden zuvor vorenthalten werden). Nach diesem Futterentzug sollen die Tiere gewogen werden und die Testsubstanz verabreicht bekommen. Nach der Verabreichung der Substanz kann das Futter bei Ratten weitere 3-4 Stunden bzw. bei Mäusen weitere 1-2 Stunden zurückgehalten werden. Wenn die Dosis über einen bestimmten Zeitraum hinweg in Teilmengen verabreicht wird, kann es je nach Länge dieses Zeitraums erforderlich sein, die Tiere mit Futter und Wasser zu versorgen.
1.5.2 Vorstudie
Zweck der Sichtungsstudie ist die Ermittlung der zweckmäßigen Ausgangsdosis für die Hauptuntersuchung, Die Testsubstanz wird einzelnen Tieren in einem sequenziellen Verfahren gemäß den Flussdiagrammen in Anlage 1 verabreicht. Die Sichtungsstudie ist abgeschlossen, wenn eine Entscheidung über die Ausgangsdosis für die Hauptstudie getroffen werden kann (oder wenn bereits bei der niedrigsten festen Dosis der Tod eines Versuchstiers eintritt).
Als Ausgangsdosis für die Sichtungsstudie wird von den festen Dosierungen 5, 50, 300 und 2.000 mg/kg die Dosis ausgewählt, die voraussichtlich eine evidente Toxizität bewirken wird, wobei nach Möglichkeit die Erkenntnisse aus In-vivo- und In-vitro-Daten für denselben chemischen Stoff sowie für strukturverwandte chemische Stoffe zugrunde liegen sollten. Wenn keine entsprechenden Informationen vorliegen, wird die Ausgangsdosis 300 mg/kg verwendet.
Zwischen den Versuchen an jedem einzelnen Tier liegt ein zeitlicher Abstand von mindestens 24 Stunden. Alle Tiere sollten mindestens 14 Tage lang beobachtet werden,
In Ausnahmefallen - und nur, wenn dies durch konkrete Vorschriften begründet ist - kann die Anwendung einer weiteren festen oberen Dosis von 5.000 mg pro kg Körpergewicht in Erwägung gezogen werden (siehe Anlage 3). Aus Tierschutzgründen wird von Tierversuchen im Bereich der GHS-Kategorie 5 (2.000 - 5.000 mg/kg) abgeraten; diese Versuche sollten nur dann in Betracht gezogen werden, wenn die Ergebnisse eines solchen Tests für den Schutz der Gesundheit von Menschen oder Tieren oder der Umwelt mit hoher Wahrscheinlichkeit direkt relevant sind.
Wenn ein Versuchstier, das mit der niedrigsten festen Dosis (5 mg/kg) getestet wird, bei der Sichtungsstudie stirbt, wird die Studie normalerweise beendet und die Substanz der GHS-Kategorie 1 zugewiesen (wie in Anlage 1 dargestellt). Ist jedoch eine weitere Bestätigung dieser Klassifizierung erforderlich, kann das folgende ergänzende Verfahren in Betracht gezogen werden: Ein zweites Versuchstier wird mit der Dosis 5 mg/kg getestet. Wenn dieses zweite Tier stirbt, wird die GHS-Kategorie 1 bestätigt und die Studie sofort beendet. Wenn das zweite Tier überlebt, wird maximal drei weiteren Tieren die Dosis 5 mg/kg verabreicht. Da ein hohes Mortalitätsrisiko besteht, sollten diese Tiere aus Tierschutzgründen nacheinander getestet werden. Der zeitliche Abstand zwischen den Versuchen an den einzelnen Tieren sollte groß genug sein, um die Überlebenswahrscheinlichkeit des vorherigen Tieres bestätigen zu können. Wenn ein zweites Tier stirbt, wird die Versuchsreihe sofort beendet, und es werden keine weiteren Tiere getestet. Da der Tod eines zweiten Tieres (unabhängig davon, wie viele Tiere bis zum Zeitpunkt der Beendigung getestet wurden) zu Ergebnis A zählt (2 oder mehr tote Tiere), wird nach der Klassifizierungsregel aus Anlage 2 für die feste Dosis 5 mg/kg vorgegangen (Kategorie 1 bei zwei oder mehr toten Versuchstieren bzw. Kategorie 2, wenn nur ein Tier stirbt). Zur Ergänzung wird in Anlage 4 die Klassifizierung im EU-System bis zur Einführung des neuen GHS erläutert.
1.5.3 Hauptstudie
1.5.3.1 Anzahl der Versuchstiere und Dosierung
Welche Maßnahmen nach dem Versuch mit der Anfangsdosierung durchgeführt werden sollen, ist den Flussdiagrammen in Anlage 2 zu entnehmen. In Betracht kommt jeweils eine von drei Maßnahmen: Versuch beenden und die entsprechende Gefahrenklassifikationsklasse zuweisen, mit einer höheren festen Dosis testen oder mit einer niedrigeren festen Dosis testen. Aus Tierschutzgründen wird jedoch eine Dosierung, die in der Sichtungsstudie zum Tod geführt hat, in der Hauptstudie nicht wiederholt (siehe Anlage 2). Die bisher gemachten Erfahrungen lassen als wahrscheinlichstes Ergebnis bei der Ausgangsdosierung vermuten, dass die Substanz ohne weitere Tests klassifiziert werden kann.
Im Normalfall werden für jede untersuchte Dosierung insgesamt fünf Tiere gleichen Geschlechts verwendet. Zu diesen fünf Tieren gehören ein Tier aus der Sichtungsstudie, dem die gewählte Dosierung verabreicht wurde, sowie vier weitere Tiere (außer wenn im Ausnahmefall eine in der Hauptstudie verwendete Dosierung in der Sichtungsstudie nicht enthalten war).
Der Zeitabstand zwischen den Versuchen mit der jeweiligen Dosierung richtet sich nach dem Einsetzen, der Dauer und dem Schweregrad der Toxizitätsanzeichen. Die Behandlung der Versuchstiere mit der nächsten Dosis sollte hinausgezögert werden, bis angenommen werden kann, dass die zuvor verwendeten Tiere überlebt haben. Bei Bedarf wird ein Abstand von drei bis vier Tagen zwischen den Versuchen mit den einzelnen Dosierungen empfohlen, um die Feststellung einer zeitverzögerten Toxizität zu ermöglichen. Dieser Zeitabstand kann nach Bedarf angepasst werden, wenn z.B. die beobachteten Reaktionen keine Schlussfolgerungen zulassen.
Wenn eine obere feste Dosis von 5.000 mg/kg in Erwägung gezogen wird, sollte verfahren werden, wie in Anlage 3 beschrieben (siehe auch Abschnitt 1.6.2).
1.5.3.2 Limit-Test
Der Limit-Test wird hauptsächlich dann eingesetzt, wenn die Person, die den Test durchführt, nach ihr vorliegenden Informationen annehmen kann, dass das zu testende Material wahrscheinlich nicht toxisch ist, d. h. nur oberhalb der in Vorschriften festgelegten Grenzdosen toxisch wirkt. Informationen über die Toxizität des Testmaterials können aus Kenntnissen über ähnliche getestete Verbindungen, Gemische oder Produkte gewonnen werden, wobei Art und Prozentanteil der Komponenten zu berücksichtigen sind, deren toxikologische Relevanz bekannt ist. In den Fällen, in denen nur wenige oder keine Informationen über die Toxizität des Testmaterials vorliegen oder in denen von einer Toxizität des Testmaterials ausgegangen wird, sollte der Haupttest durchgeführt werden.
Bei der normalen Vorgehensweise wird für den Limit-Test im Rahmen dieses Leitfadens eine Ausgangsdosis von 2.000 mg/kg (bzw. im Ausnahmefall 5.000 mg/kg) für die Sichtungsstudie verwendet; anschließend werden vier weitere Tiere dieser Dosis ausgesetzt.
1.6 Beobachtungen
Die Tiere werden nach der Verabreichung einzeln beobachtet: mindestens einmal während der ersten 30 Minuten, in regelmäßigen Abständen während der ersten 24 Stunden, wobei die ersten vier Stunden besonders zu beachten sind, sowie anschließend täglich während einer Gesamtdauer von 14 Tagen, sofern die Tiere nicht aus Tierschutzgründen aus dem Versuch genommen und auf humane Weise gelötet werden müssen oder ihr Tod festgestellt wird. Die Beobachtungsdauer sollte nicht strikt festgelegt werden, sondern abhängig von den toxischen Reaktionen, vom Zeitpunkt des Einsetzens dieser Reaktionen und von der Länge der Erholungsdauer festgelegt werden und kann daher ausgedehnt werden, wenn dies erforderlich scheint. Der Zeitpunkt, zu dem die Anzeichen von Toxizität auftreten und wieder verschwinden, ist insbesondere dann von Bedeutung, wenn eine Tendenz zur zeitlichen Verzögerung der Toxizitätsanzeichen besteht (11). Sämtliche Beobachtungen werden für die Tiere systematisch jeweils in Einzelprotokollen dokumentiert.
Zusätzliche Beobachtungen sind erforderlich, wenn bei den Tieren weiterhin Anzeichen für Toxizität zu beobachten sind. Die Beobachtungen sollten Veränderungen an Haut und Fell, Augen und Schleimhäuten erfassen und auch die Atmung, den Kreislauf, das vegetative und zentrale Nervensystem sowie somatomotorische Aktivitäten und Verhaltensmuster berücksichtigen. Auf Symptome wie Tremores, Krämpfe, Speichelfluss, Durchfall, Lethargie, Schlaf und Koma sollte geachtet werden. Die im Humane Endpoints Guidance Document (8) zusammengefassten Prinzipien und Kriterien sind zu berücksichtigen. Tiere, bei denen ein moribunder Zustand festgestellt wird, sowie Tiere, die starke Schmerzen haben oder anhaltende Anzeichen von schwerem Leiden zeigen, sollten auf humane Weise getötet werden. Wenn Tiere aus humanen Gründen getötet werden oder ihr Tod festgestellt wird, sollte der Todeszeitpunkt so genau wie möglich registriert werden.
1.6.1 Körpergewicht
Das Gewicht der einzelnen Tiere soll kurz vor der Verabreichung der Testsubstanz sowie spätestens eine Woche danach ermittelt werden. Gewichtsveränderungen sollen berechnet und registriert werden. Am Ende des Tests werden die überlebenden Tiere gewogen und anschließend auf humane Weise getötet.
1.6.2 Pathologie
Alle Versuchstiere (einschließlich der Tiere, die während des Tests sterben oder aus Tierschutzgründen aus der Studie genommen werden) sollen auf makrologische Veränderungen untersucht werden. Alle makrologischen Veränderungen sollen für jedes einzelne Tier registriert werden. Bei Tieren, die 24 oder mehr Stunden lang überlebt haben, kann auch eine mikroskopische Untersuchung von Organen mit makropathologischen Befunden in Erwägung gezogen werden, da sich hieraus eventuell nützliche Informationen gewinnen lassen.
2. Daten
Es sollen Daten zu den einzelnen Tieren bereitgestellt werden. Darüber hinaus sollen sämtliche Daten in tabellarischer Form zusammengefasst werden, wobei für jede Testgruppe die folgenden Daten zu erfassen sind; Anzahl der verwendeten Tiere, Anzahl der Tiere mit Anzeichen für eine toxische Wirkung, Anzahl der Tiere, deren Tod während des Versuchs festgestellt wurde oder die aus humanen Gründen getötet wurden, Todeszeitpunkt der einzelnen Tiere, Beschreibung und Zeitverlauf der toxischen Wirkungen und ihrer Reversibilität sowie pathologische Befunde.
3. Bericht
3.1 Testbericht
Der Prüfbericht muss die folgenden Angaben enthalten (soweit angemessen):
Testsubstanz:
- physikalische Beschaffenheit, Reinheit und, sofern relevant, physikalischchemische Eigenschaften (einschließlich Isomerisierung),
- Identifizierungsdaten, einschließlich CAS-Nummer.
Vehikel (wenn verwendet):
- Begründung für die Auswahl des Vehikels (außer bei Wasser).
Versuchstiere:
- verwendete Spezies/Stamm,
- mikrobiologischer Zustand der Tiere, sofern bekannt,
- Anzahl, Alter und Geschlecht der Tiere (gegebenenfalls mit Begründung für den Einsatz von männlichen statt weiblichen Tieren),
- Bezugsquelle der Tiere, Haltungsbedingungen, Futter usw.
Testbedingungen:
- Angaben über die Zubereitung der Testsubstanz, einschließlich Angaben über die physikalische Beschaffenheit des verabreichten Stoffs,
- Angaben über die Verabreichung der Testsubstanz, einschließlich Applikationsvolumen und Zeitpunkt der Verabreichung,
- Angaben zur Futter- und Wasserqualität (einschließlich Art/Herkunft des Futters, Herkunft des Wassers),
- Begründung für die Wahl der Startdosis.
Ergebnisse:
- tabellarische Erfassung der erhobenen Daten und der Dosis für jedes einzelne Tier (d. h. Tiere, die Anzeichen für Toxizität zeigen, einschließlich Mortalität sowie Art, Schweregrad und Dauer der Wirkungen),
- tabellarische Erfassung des Körpergewichts und der Änderungen des Körpergewichts,
- Gewicht der einzelnen Tiere am Tag der Verabreichung, danach in wöchentlichen Abständen sowie am Tag des Todes bzw. der Tötung,
- Datum und Uhrzeit des Todes, sofern vor der planmäßigen Tötung eingetreten,
- zeitlicher Verlauf des Einsetzens von Toxizitätsanzeichen sowie Angabe, ob diese reversibel waren (für jedes Tier gesondert),
- Obduktionsergebnisse und histopathologische Ergebnisse für jedes einzelne Tier (wenn vorhanden).
Diskussion und Interpretation der Ergebnisse.
Schlussfolgerung.
4. Literatur
(1) British Toxicology Society Working Party on Toxicity (1984). Special report: a new approach to the classification of substances and preparations on the basis of their acute toxicity. Human Toxicol., 3, 85-92.
(2) Van den Heuvel, M.J., Dayan, A.D. and Shillaker, R.O. (1987), Evaluation of the BTS approach to the testing of substances and preparations for their acute toxicity. Human Toxicol., 6, 279-291.
(3) Van den Heuvel, M.J., Clark, D.G., Fielder, R.J., Koundakjian, P.P., Oliver, G.J.A., Pelling, D., Tomlinson, N.J. and Walter, AP. (1990). The international validation of a fixeddose procedure as an alternative to the classical LD50 test. Fd. Chem. Toxicol. 28, 469-482.
(4) Whitehead, A. and Cumow, R.N. (1992). Statistical evaluation of the fixeddose procedure. Fd. Chem. Toxicol., 30, 313-324.
(5) Stallard, N. and Whitehead, A. (1995). Reducing numbers in the fixeddose procedure. Human Exptl. Toxicol. 14, 315-323. Human Exptl. Toxicol.
(6) Stallard, N., Whitehead, A. and Ridgeway, P. (2002). Statistical evaluation of the revised fixed dose procedure. Human Exptl. Toxicol., 21, 183-196.
(7) OECD (200l). Guidance Document on Acute Oral Toxicity Testing. Environmental Health and Safety Monograph Series on Testing and Assessment N. 24. Paris
(8) OECD (2000). Guidance Document on the Recognition, Assessment and Use of Clinical Signs as Humane Endpoints for Experimental Animals Used in Safety Evaluation. Environmental Health and Safety Monograph Series on Testing and Assessment N. 19.
(9) OECD (1998), Harmonised Integrated Hazard Classification for Human Health and Environmental Effects of Chemical Substances as endorsed by the 28th Joint Meeting of the Chemicals Committee and the Working Party on Chemicals in November 1998, Part 2, S. 11 (http://webnet1.oecd.org/oecd/pages/ home/displaygener; d/0,3380,EN- documents-521-14-no-24-no-0,FF.html).
(10) Lipnick, R.L., Cotruvo, J.A., Hill, R.N.; Bruce, R.D., Stitzel, K.A., Walker, A.P., Chu, I., Goddard, M., Segal, L., Springer, J.A. and Myers, R.C. (1995). Comparison of the Upand-Down, Conventional LD50, and Fixed-Dose Acute Toxicity Procedures. Fd. Chem. Toxicol. 33, 223-231.
(11) Chan P.K and A.W. Hayes (1994) Chapter 16 Acute Toxicity and Eye Irritation. In: Principles and Methods of Toxicology. 3rd Edition. A.W. Hayes, Editor. Raven Press, Ltd, New York, USA.
| Prüfverfahren für die Vorstudie | Anlage 1 |


| Prüfverfahren für die Hauptstudie | Anlage 2 |


| Kriterien für die Klassifizierung von Testsubstanzen mit erwarteten LD50-Werten über 2.000 mg/kg ohne erforderliche Tests | Anlage 3 |
Die Kriterien für die Gefahrenkategorie 5 sollen die Identifikation von Testsubstanzen ermöglichen, die eine vergleichsweise geringe akute Toxizitätsgefahr aufweisen, aber unter bestimmten Umstanden eine Gefahr für anfällige Bevölkerungsgruppen darstellen.
Bei diesen Substanzen wird von einer oralen oder dermalen LD50 im Bereich 2.000-5.000 mg/kg bzw. von vergleichbaren Dosen für andere Verabreichungswege ausgegangen.
Die Testsubstanzen sollte in den folgenden Fällen in die Gefahrenkategorie 2.000 mg/kg < LD50 < 5.000 mg/kg (GHS-Kategorie 5) eingestuft werden:
- wenn eines der Prüfschemata aus Anlage 2 aufgrund von Mortalitätsfällen dieser Kategorie zuzuordnen ist;
- wenn bereits zuverlässige Erkenntnisse dafür vorliegen, dass der LD50-Wert im Bereich der Kategorie 5 liegt, oder wenn andere Tierversuche oder toxische Wirkungen auf Menschen akute Folgen für die menschlichen Gesundheit erwarten lassen;
- wenn nach Extrapolierung, Schätzung oder Messung von Daten die Zuordnung zu einer höheren Gefahrenklasse nicht gerechtfertigt ist und
- zuverlässige Informationen vorliegen, die auf signifikante toxische Wirkungen beim Menschen hinweisen, oder
- Mortalitäten bei oraler Verabreichung in Versuchen mit Dosen bis zu der Kategorie 4 auftreten, oder
- eine fachkundige Beurteilung bei Versuchen mit Dosierungen bis zu den in Kategorie 4 genannten Werten signifikante klinische Toxizitätsanzeichen bestätigt (außer Durchfall, Haaraufrichtung oder zerzaustes Fell), oder
- eine fachkundige Beurteilung verlässliche Informationen bestätigt, die aus den anderen Tierversuchen ein Potenzial für signifikante akute Wirkungen erkennen lassen.
Versuche mit Dosen über 2.000 mg/kg
In Ausnahmefällen - und nur, wenn dies durch konkrete Vorschriften begründet ist - kann die Anwendung einer weiteren festen oberen Dosis von 5.000 mg pro kg Körpergewicht in Erwägung gezogen werden. Aus Tierschutzgründen wird von Versuchen mit 5.000 mg/kg abgeraten; diese Versuche sollen nur dann in Erwägung gezogen werden, wenn die Ergebnisse eines solchen Versuchs für den Schulz der Gesundheit von Menschen oder Tieren oder der Umwelt mit hoher Wahrscheinlichkeit direkt relevant sind (9).
Vorstudie
Die Entscheidungsgrundlagen für das in Anlage 1 vorgestellte sequenzielle Verfahren werden auf eine Dosis von 5.000 mg/ kg erweitert: Wenn eine Startdosis von 5.000 mg/kg für die Vorstudie verwendet wird, bedingt Ergebnis A (Tod) den Test eines zweiten Tieres mit 2.000 mg/kg; die Ergebnisse B und C (evidente Toxizität oder keine Toxizität) führen zum Einsatz von 5.000 mg/kg als Startdosis für die Hauptstudie. Analog wird bei Verwendung einer anderen Startdosis als 5.000 mg/kg der Versuch mit 5.000 mg/kg fortgesetzt, wenn bei 2.000 mg/kg Ergebnis B oder C eintritt; wenn anschließend bei 5.000 mg/kg Ergebnis A eintritt, bedingt dies eine Startdosis von 2.000 mg/kg bei der Hauptstudie, während die Ergebnisse B und C zu einer Startdosis von 5.000 mg/kg bei der Hauptstudie führen.
Hauptstudie
Die Entscheidungsgrundlagen für das in Anlage 2 vorgestellte sequenzielle Verfahren werden auf eine Dosierung von 5.000 mg/kg erweitert: Wenn in der Hauptstudie eine Startdosis von 5.000 mg/kg verwendet wird, ist bei Ergebnis A (> 2 tote Versuchstiere) eine zweiten Gruppe mit 2.000 mg/kg zu testen; die Ergebnisse B (evidente Toxizität und/oder < 1 totes Versuchstier) oder C (keine Toxizität) fuhren dazu, dass die Substanz keine Klassifizierung gemäß GHS erhält. Analog wird bei Verwendung einer anderen Startdosis als 5.000 mg/kg der Versuch mit 5.000 mg/kg fortgesetzt, wenn bei 2.000 mg/kg Ergebnis C eintritt; führt eine Gabe von 5.000 mg/kg zu Ergebnis A, wird die Substanz GHS-Kategorie 5 zugewiesen; bei den Ergebnissen B und C wird die Substanz nicht klassifiziert.
| Prüfmethode B.1 bis | Anlage 4 |
Anleitung für die Klassifizierung gemäß dem EU-System zur Überbrückung des Übergangszeitraums bis zur vollständigen Umsetzung des "Globalen Harmonisierten Systems" (GHS) (Auszug aus Literaturhinweis (8))


B.1.tris. Akute orale Toxizität - Akut-toxische Klassenmethode
1. Methode
Diese Prüfmethode entspricht der OECD TG 423 (2001).
1.1 Einleitung
Die hier beschriebene Akut-Toxische Klassenmethode (1) besteht aus einem schrittweisen Verfahren, bei dem pro Einzelschritt jeweils drei Tiere des gleichen Geschlechts verwendet werden. Je nach Mortalität und/oder moribundem Zustand der Tiere können im Mittel zwei bis vier Schritte erforderlich sein, um eine Beurteilung der akuten Toxizität der Testsubstanz zu ermöglichen. Dieses Verfahren ist reproduzierbar, erfordert nur sehr wenige Tiere und ermöglicht eine gleichartige Bewertung der Substanzen wie andere Methoden zur Prüfung der akuten Toxizität. Die Akut-Toxische Klassenmethode basiert auf biometrischen Berechnungen (2) (3) (4) (5) mit festgesetzten Dosen, die sich hinreichend unterscheiden, um die Einordnung einer Substanz zu Klassifizierungszwecken und zur Bewertung des Gefährdungspotenzials zu ermöglichen. Die Methode, wie sie 1996 anerkannt wurde, wurde durch umfassende In-vivo-Versuche im Vergleich mit LD50-Daten aus der Literatur sowohl auf nationaler (6) als auch auf internationaler (7) Ebene validiert.
Leitlinien für die Auswahl der geeignetsten Testmethode für einen bestimmten Zweck enthält das Guidance Document on Acute Oral Toxicity Testing (8). Dieser Leitfaden beinhaltet darüber hinaus weitere Informationen zur Durchführung und Auswertung der Prüfmethode B.1 tris.
Testsubstanzen sind nicht in Dosen zu verabreichen, wenn diese aufgrund ätzender oder stark reizender Wirkungen bekanntermaßen starke Schmerzen und schweres Leiden verursachen. Moribunde Tiere oder Tiere, die offensichtlich unter Schmerzen leiden oder Anzeichen von schwerem und anhaltendem Leiden zeigen, sind auf humane Weise zu töten und werden bei der Auswertung der Testergebnisse auf die gleiche Weise gewertet wie während des Tests gestorbene Tiere. Kriterien für die Entscheidung, moribunde oder schwer leidende Tiere zu töten, sowie Hinweise zur Erkennung des absehbaren oder bevorstehenden Todes sind Gegenstand eines gesonderten Leitfadens (9).
Die Methode beruht auf festgesetzten Dosen, und die Ergebnisse ermöglichen die Bewertung und Klassifizierung von Substanzen gemäß dem Globalen Harmonisierten System (GHS) zur Klassifizierung chemischer Stoffe mit akuttoxischen Wirkungen (10).
Vom Prinzip her ist die Methode nicht zur Berechnung eines exakten LD50-Wertes geeignet, sondern zur Bestimmung definierter Expositionsbereiche, in denen eine Letalität auftreten kann, da der Tod eines Teils der Tiere noch immer den wichtigsten Endpunkt dieser Methode darstellt. Ein LD50-Wert kann nur dann mit dieser Methode bestimmt werden, wenn mindestens zwei Dosen zu einer Mortalität von über 0 %, aber unter 100 % führen. Die Auswahl von festgesetzten Dosen unabhängig von der Testsubstanz zusammen mit der Koppelung an eine Anzahl von Tieren in unterschiedlichem Zustand an eine Klassifizierung verbessert die Konsistenz und die Reproduzierbarkeit zwischen den Laboratorien.
Das Prüflabor soll vor der Durchführung der Studie sämtliche verfügbaren Informationen berücksichtigen. Zu diesen Informationen gehören die Identität und die chemische Struktur der Substanz, ihre physikalischchemischen Eigenschaften, das Ergebnis anderer In-vivo- oder In-vitro-Toxizitätstests der betreffenden Substanz, toxikologische Daten über die strukturverwandten Substanzen sowie die vorgesehene(n) Verwendung(en) der Substanz. Diese Informationen werden benötigt, um die zuständigen Stellen zu überzeugen, dass der Test für den Schutz der menschlichen Gesundheit wichtig ist und bei der Wahl der geeigneten Startdosis hilft.
1.2 Definitionen
Akute orale Toxizität: Schädliche Wirkungen, die nach der oralen Verabreichung einer Einzeldosis oder mehrerer innerhalb von 24 Stunden verabreichter Dosen einer Substanz auftreten.
Verzögerter Tod: Das betreffende Tier stirbt zwar nicht binnen 48 Stunden und wirkt in diesem Zeitraum nicht moribund; der Tod tritt jedoch später während des 14-tägigen Beobachtungszeitraums ein.
Dosis: Verabreichte Menge der Testsubstanz; die Dosis wird als Gewicht der Testsubstanz pro Gewichtseinheit des Versuchstiers ausgedrückt (z.B. mg/kg).
GHS: Globally Harmonised Classification System for Chemical Substances and Mixtures (Weltweit harmonisiertes Klassifizierungssystem für chemische Substanzen und Gemische); ein gemeinsames Projekt von OECD (Menschliche Gesundheit und Umwelt), UN-Expertenausschuss für den Transport von Gefahrgütern (physikalisch-chemische Eigenschaften) und ILO (Gefahrenanzeige) koordiniert im Rahmen des Interorganisation Programme for the Sound Management of Chemicals (IOMC).
Bevorstehender Tod: Der moribunde Zustand oder Tod ist vor dem nächsten vorgesehenen Beobachtungszeitpunkt zu erwarten. Anzeichen für diesen Zustand können bei Nagetieren Krämpfe, Seitenlage, liegende Stellung und Tremores sein (siehe Humane Endpoint Guidance Document (9)).
LD50 (mittlere orale Letaldosis): Eine statistisch ermittelte Einzeldosis einer Substanz, bei der davon ausgegangen werden kann, dass sie bei oraler Verabreichung den Tod von 50 % der Tiere verursacht; der LD50-Wert wird als Gewicht der Testsubstanz pro Gewichtseinheit der Versuchstiere ausgedrückt (mg/kg).
Limit-Dosis: Dosis am oberen Grenzwert für den betreffenden Versuch (2.000 oder 5.000 mg/kg).
Moribunder Zustand: Zustand des Sterbens oder des Unvermögens, (selbst bei Behandlung) zu überleben (siehe Humane Endpoint Guidance Document (9)).
Voraussagbarer Tod: Vorhandensein klinischer Zeichen, die auf den Eintritt des Todes zu einem bekannten Zeitpunkt in der Zukunft - vor dem planmäßigen Ende des Experiments - hinweisen, z.B. das Unvermögen, Wasser oder Nahrung aufzunehmen (siehe Humane Endpoint Guidance Document (9)).
1.3 Prinzip der Prüfmehode
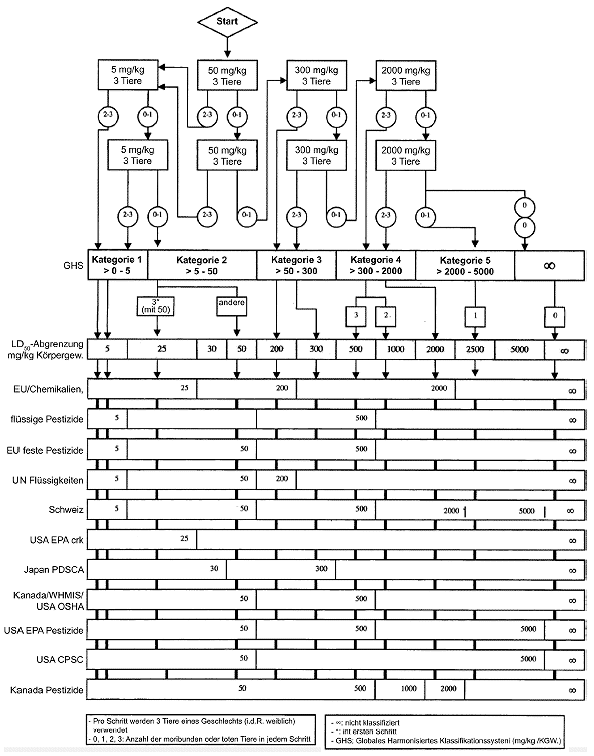
Das Versuchsprinzip besteht darin, in einem schrittweisen Verfahren bei Verwendung einer minimalen Anzahl von Tieren pro Einzelschritt genügend Informationen über die akute Toxizität der Testsubstanz zu gewinnen, um ihre Klassifizierung zu ermöglichen, Die Substanz wird einer Gruppe von Versuchstieren oral mit einer der festgelegten Dosen verabreicht. Die Substanz wird in einem schrittweisen Verfahren getestet, wobei für jeden Schritt jeweils drei Tiere des gleichen Geschlechts (normalerweise weibliche Tiere) verwendet werden. Das Eintreten oder Nichteintreten von prüfsubstanzbedingten Todesfällen bei dem in einem Schritt behandelten Tieren bestimmt über den nächsten Schritt, d. h.:
- ob keine weiteren Tests erforderlich sind,
- ob drei weitere Tiere mit der gleichen Dosis zu behandeln sind,
- ob der nächste Schritt an drei weiteren Tieren mit der nächsthöheren oder nächstniedrigeren Dosis durchzuführen ist.
In Anlage 1 ist die Testmethode im Einzelnen beschrieben. Die Methode ermöglicht die Beurteilung, eine Testsubstanz innerhalb einer Reihe von Toxizitätsklassen einzuordnen, die durch feste LD50-Abgrenzungswerte definiert sind.
1.4 Beschreibung der Prüfmethode
1.4.1 Auswahl der Tierspezies
Die bevorzugte Nagetierspezies ist die Ratte, es können aber auch andere Spezies verwendet werden. In der Regel werden weibliche Tiere verwendet (9). Weibliche Tiere werden bevorzugt, da die in der Literatur zitierten Untersuchungen zu konventionellen LD50-Tests zwischen den Geschlechtern in der Regel nur geringfügige Unterschiede hinsichtlich der Empfindlichkeit belegen, in den Fällen, in denen Unterschiede beobachtet werden, jedoch zeigen, dass weibliche Tiere im Allgemeinen etwas empfindlicher sind (11). Wenn jedoch die vorhandenen Informationen über die toxikologischen oder toxikokinetischen Eigenschaften von strukturverwandten Chemikalien darauf hinweisen, dass vermutlich die männlichen Tiere empfindlicher sind, sollten männliche Tiere verwendet werden. Wenn der Versuch an männlichen Tieren durchgeführt wird, sollte dies hinreichend begründet werden.
Es sollen junge, gesunde, ausgewachsene Tiere aus üblicherweise eingesetzten Laborstämmen verwendet werden. Die weiblichen Tiere dürfen weder bereits geworfen haben noch momentan trächtig sein. Alle Tiere müssen zu Beginn der Verabreichung zwischen 8 und 12 Wochen all sein; ihre Gewichtswerte müssen im Bereich von ± 20 % des mittleren Gewichts sämtlicher zuvor verwendeter Tiere liegen.
1.4.2 Haltung und Fütterung
Die Temperatur im Versuchstierraum soll 22 °C (± 3 °C) betragen. Die Temperatur des Versuchstierraums soll 22 °C (± 3 °C) betragen. Die relative Luftfeuchtigkeit soll mindestens 30 % betragen und außer während der Reinigung vorzugsweise nicht über 70 % liegen; anzustreben ist ein Wert von 50-60 %. Der Raum soll künstlich beleuchtet sein, wobei die Beleuchtung im 12-Stunden-Rhythmus ein- und ausgeschaltet werden soll. An die Versuchstiere kann herkömmliches Laborfutter verfüttert werden, wobei eine unbegrenzte Trinkwasserversorgung zu gewährleisten ist. Die Tiere können in den Käfigen nach Verabreichungsdosen gruppiert werden, wobei aber die Anzahl der Tiere pro Käfig noch eine genaue Beobachtung der einzelnen Tiere ermöglichen muss.
1.4.3 Vorbereitung der Versuchstiere
Die Tiere werden nach Zufallskriterien ausgewählt, zwecks Identifizierung markiert und für die Dauer von mindestens 5 Tagen vor Versuchsbeginn in ihren Käfigen gehalten, damit sie sich an die Laborbedingungen gewöhnen können.
1.4.4 Vorbereitung der Dosen
Generell sollen die Testsubstanzen mit einem für den gesamten zu testenden Dosierungsbereich gleichbleibenden Volumen verabreicht werden, indem jeweils die Konzentration der Dosiszubereitung variiert wird. Wenn jedoch ein flüssiges Endprodukt oder Gemisch zu testen ist, kann die Anwendung der unverdünnten, d. h. mit gleichbleibender Konzentration verabreichten Testsubstanz für die anschließende Risikobewertung der betreffenden Substanz größere Relevanz haben und wird daher von verschiedenen Behörden vorgeschrieben. In jedem Fall darf das maximal zu verabreichende Dosisvolumen nicht überschritten werden. Welches Flüssigkeitsvolumen jeweils höchstens auf einmal verabreicht werden kann, hängt von der Größe des Versuchstiers ab. Bei Nagetieren soll das Volumen im Normalfall 1 ml pro 100 g Körpergewicht nicht überschreiten; bei wässrigen Lösungen können aber auch 2 ml pro 100 g Körpergewicht in Betracht gezogen werden. Bezüglich der Formulierung wird, wenn dies möglich ist, eine wässrige Lösung/Suspension/Emulsion empfohlen, danach in der Reihenfolge der Präferenz eine Lösung/Suspension/Emulsion in Öl (z.B. Maisöl) sowie an dritter Stelle eventuell eine Lösung in anderen Vehikeln. Bei anderen Vehikeln als Wasser sollen die toxikologischen Eigenschaften des jeweiligen Vehikels bekannt sein. Die Dosen dürfen erst kurz vor der Verabreichung zubereitet werden, sofern die Zubereitung über den Zeitraum, in dem sie angewandt werden soll, nicht bekanntermaßen eine annehmbare Stabilität aufweist.
1.5 Verfahrensweise
1.5.1 Verabreichung der Dosen
Die Testsubstanz wird als Einzeldosis mit einer Sonde über einen Magensonde oder über eine geeignete Intubationskanüle verabreicht. In dem seltenen Fall, dass die Verabreichung als Einzeldosis nicht möglich ist, kann die Dosis über einen Zeitraum von maximal 24 Stunden in kleineren Teilmengen verabreicht werden.
Die Versuchstiere sollten vor der Verabreichung nüchtern sein (z.B. sollte Ratten das Futter (nicht das Wasser) über Nacht vorenthalten werden; Mäusen sollte das Futter (nicht das Wasser) 3-4 Stunden zuvor vorenthalten werden). Nach diesem Futterentzug sollen die Tiere gewogen werden und die Testsubstanz verabreicht bekommen. Nach der Verabreichung der Substanz kann das Futter bei Ratten weitere 3-4 Stunden bzw. bei Mäusen weitere 1-2 Stunden zurückgehalten werden. Wenn die Dosis über einen bestimmten Zeitraum hinweg in Teilmengen verabreicht wird, kann es je nach Länge dieses Zeitraums erforderlich sein, die Tiere mit Futter und Wasser zu versorgen.
1.5.2 Anzahl der Versuchstiere und Dosierung
Für jeden Schritt werden drei Tiere verwendet. Die als Ausgangsdosis zu verwendende Dosis wird aus vier festen Dosiswerten gewählt: 5, 50, 300 und 2.000 mg pro kg Körpergewicht. Als Startdosis soll die Dosis gewählt werden, die mit der größten Wahrscheinlichkeit zur Mortalität einiger der behandelten Tiere führt. Die Prüfschemata in Anlage 1 beschreiben für jede dieser Ausgangsdosen die jeweils zu befolgende Vorgehensweise. Zur Ergänzung wird in Anlage 4 die Klassifizierung im EU-System bis zur Einführung des neuen GHS erläutert.
Wenn bereits verfügbare Informationen vermuten lassen, dass bei der höchsten Startdosis (2.000 mg pro kg Körpergewicht) keine Mortalität zu erwarten ist, soll ein Limit-Test durchgeführt werden. Wenn für eine zu testende Substanz keine Informationen zur Verfügung stehen, wird aus Tierschutzgründen empfohlen, als Ausgangsdosis 300 mg pro kg Körpergewicht zu verwenden.
Der Zeitabstand zwischen den einzelnen Behandlungsgruppen richtet sich nach dem Einsetzen, der Dauer und dem Schweregrad der toxischen Zeichen. Die Behandlung der Versuchstiere mit der nächsten Dosis soll so lange abgewartet werden, bis angenommen werden kann, dass die zuvor behandelten Tiere überleben.
In Ausnahmefällen - und nur, wenn dies durch konkrete Vorschriften begründet ist - kann die Anwendung einer weiteren oberen Dosis von 5.000 mg pro kg Körpergewicht in Erwägung gezogen werden (siehe Anlage 2). Aus Tierschutzgründen wird von Tierversuchen im Bereich der GHS-Kategorie 5 (2.000- 5.000 mg/kg) abgeraten; diese Versuche sollen nur dann in Betracht gezogen werden, wenn die Ergebnisse eines solchen Tests für den Schutz der Gesundheit von Menschen oder Tieren oder der Umwelt mit hoher Wahrscheinlichkeit direkt relevant wären.
1.5.3 Limit-Test
Der Limit-Test wird hauptsächlich dann eingesetzt, wenn die Person, die den Test durchführt, nach ihr vorliegenden Informationen davon ausgehen kann, dass das zu testende Material wahrscheinlich nicht toxisch ist, d. h. nur oberhalb der regulatorisch festgelegten Grenzdosen toxisch wirkt. Informationen über die Toxizität des Testmaterials können aus Kenntnissen über ähnliche getestete Verbindungen, Mischungen oder Produkte gewonnen werden, wobei Art und Prozentanteil der Komponenten zu berücksichtigen sind, deren toxikologische Relevanz bekannt ist. In den Fällen, in denen nur wenige oder keine Informationen über die Toxizität des Testmaterials vorliegen oder in denen von einer Toxizität des Testmaterials ausgegangen wird, sollte der Haupttest durchgeführt werden.
Ein Limit-Test mit einer Dosis von 2.000 mg pro kg Körpergewicht kann mit sechs Tieren durchgeführt werden (drei Tiere pro Schritt). In Ausnahmefällen kann ein Limit-Test mit einer Dosis von 5.000 mg/kg mit drei Tieren durchgeführt werden (siehe Anlage 2). Wenn eine mit der Testsubstanz in Zusammenhang stehende Mortalität ermittelt wird, müssen eventuell weitere Prüfungen mit der nächstniedrigeren Dosis durchgeführt werden.
1.6 Beobachtungen
Die Tiere werden nach der Verabreichung einzeln beobachtet: mindestens einmal während der ersten 30 Minuten, in regelmäßigen Abständen während der ersten 24 Stunden, wobei die ersten vier Stunden besonders zu beachten sind, sowie anschließend täglich während einer Gesamtdauer von 14 Tagen, sofern die Tiere nicht aus Tierschutzgründen aus dem Versuch genommen und auf humane Weise getötet werden müssen oder ihr Tod festgestellt wird. Die Beobachtungsdauer sollte jedoch nicht strikt festgelegt werden; vielmehr sollte sie in Abhängigkeit von den toxischen Reaktionen, vom Zeitpunkt des Einsetzens dieser Reaktionen und von der Länge der Erholungsdauer festgelegt werden und kann daher ausgedehnt werden, wenn dies erforderlich scheint. Der Zeitpunkt, zu dem die Anzeichen von Toxizität auftreten und wieder verschwinden, ist von Bedeutung, und zwar insbesondere dann, wenn eine Tendenz zur zeitlichen Verzögerung der Toxizitätsanzeichen besteht (12). Sämtliche Beobachtungen werden für die Tiere systematisch jeweils in Einzelprotokollen dokumentiert.
Zusätzliche Beobachtungen sind erforderlich, wenn bei den Tieren weiterhin Anzeichen für Toxizität zu beobachten sind. Die Beobachtungen sollten Veränderungen an Haut und Fell, Augen und Schleimhäuten erfassen und auch die Atmung, den Kreislauf, das vegetative und zentrale Nervensystem sowie somatomotorische Aktivitäten und Verhaltensmuster berücksichtigen. Auf Beobachtungen wie Tremores, Krämpfe, Speichelfluss, Durchfall, Lethargie, Schlaf und Koma sollte geachtet werden. Die im Humane Endpoints Guidance Document (9) zusammengefassten Prinzipien und Kriterien sind zu berücksichtigen. Tiere, bei denen ein moribunder Zustand festgestellt wird, sowie Tiere, die starke Schmerzen haben oder anhaltende Anzeichen von schwerem Leiden zeigen, sollten auf humane Weise getötet werden. Wenn Tiere aus humanen Gründen getötet werden oder ihr Tod festgestellt wird, sollte der Todeszeitpunkt so genau wie möglich registriert werden.
1.6.1 Körpergewicht
Das Gewicht der einzelnen Tiere sollte kurz vor der Verabreichung der Testsubstanz sowie spätestens eine Woche danach ermittelt werden. Gewichtsveränderungen sollen berechnet und registriert werden. Am Ende des Tests werden die überlebenden Tiere gewogen und auf humane Weise getötet.
1.6.2 Pathologie
Alle Versuchstiere (einschließlich der Tiere, die während des Tests sterben oder aus Tierschutzgründen aus der Studie genommen werden) sollen auf makroskopische Veränderungen untersucht werden. Alle makroskopischen Veränderungen sollen für jedes einzelne Tier registriert werden. Bei Tieren, die 24 oder mehr Stunden lang überlebt haben, kann auch eine mikroskopische Untersuchung von Organen mit makropathologischen Befunden in Erwägung gezogen werden, da sich hieraus eventuell nützliche Informationen gewinnen lassen.
2. Daten
Es sollen Daten zu den einzelnen Tieren bereitgestellt werden. Darüber hinaus sollen sämtliche Daten in tabellarischer Form zusammengefasst werden, wobei für jede Testgruppe die folgenden Daten zu erfassen sind: Anzahl der verwendeten Tiere, Anzahl der Tiere mit Anzeichen für eine toxische Wirkung, Anzahl der Tiere, deren Tod während des Versuchs festgestellt wurde oder die aus humanen Gründen getötet wurden, Todeszeitpunkt der einzelnen Tiere, Beschreibung und Zeitverlauf der toxischen Wirkungen und ihrer Reversibilität sowie pathologische Befunde.
3. Bericht
3.1 Prüfbericht
Der Prüfbericht muss die folgenden Angaben enthalten (soweit angemessen):
Testsubstanz:
- physikalische Beschaffenheit, Reinheit und, wenn maßgeblich, physikalischchemische Eigenschaften (einschließlich Isomerisierung),
- Identifizierungsdaten, einschließlich CAS-Nummer.
Vehikel (wenn verwendet):
- Begründung für die Auswahl des Vehikels (außer bei Wasser).
Versuchstiere:
- verwendete Spezies/Stamm,
- mikrobiologischer Zustand der Tiere (wenn bekannt),
- Anzahl, Alter und Geschlecht der Tiere (gegebenenfalls mit Begründung für den Einsatz von männlichen statt weiblichen Tieren),
- Bezugsquelle der Tiere, Haltungsbedingungen, Futter usw.
Testbedingungen:
- Angaben über die Zubereitung der Testsubstanz, einschließlich Angaben über die physikalische Beschaffenheit des verabreichten Stoffs,
- Angaben über die Verabreichung der Testsubstanz, einschließlich Applikationsvolumen und Zeitpunkt der Verabreichung,
- Angaben zur Futter- und Wasserqualität (einschließlich Art/Herkunft des Futters, Herkunft des Wassers),
- Begründung für die Wahl der Startdosis.
Ergebnisse:
- tabellarische Erfassung der erhobenen Daten und der Dosis für jedes einzelne Tier (d. h. Tiere, die Anzeichen für Toxizität zeigen, einschließlich Mortalität sowie Art, Schweregrad und Dauer der Wirkungen),
- tabellarische Erfassung des Körpergewichts und der Änderungen des Körpergewichts,
- Gewicht der einzelnen Tiere am Tag der Verabreichung, danach in wöchentlichen Abständen sowie am Tag des Todes bzw. der Tötung,
- Datum und Uhrzeit des Todes, sofern vor der planmäßigen Tötung eingetreten,
- zeitlicher Verlauf des Einsetzens von Toxizitätsanzeichen sowie Angabe, ob diese reversibel waren, für jedes einzelne Tier,
- Obduktionsergebnisse und histopathologische Ergebnisse für jedes einzelne Tier (wenn vorhanden).
Diskussion und Interpretation der Ergebnisse.
Schlussfolgerung.
4. Literaturhinweise
(1) Roll R., Höfer-Bosse Th. and Kayser D. (1986). New Perspectives in Acute Toxicity Testing of Chemicals. Toxicol. Lett., Suppl. 31, 86
(2) Roll R., Riebschläger M., Mischke U. and Kayser D. (1989). Neue Wege zur Bestimmung der akuten Toxizität von Chemikalien. Bundesgesundheitsblatt 32, 336-341.
(3) Diener W., Sichha L., Mischke U., Kayser D. and Schiede E. (1994). The Biometric Evaluation of the Acute-Toxic-Class Method (Oral). Arch. Toxicol. 68, 559-610
(4) Diener W., Mischke U., Kayser D. and Schiede E. (1995). The Biometric Evaluation of the OECD Modified Version of the Acute-Toxic-Class Method (Oral). Arch. Toxicol. 69, 729-734.
(5) Diener W. and Schiede E. (1999) Acute Toxicity Class Methods: Alterations to LD/LC50 Tests. ALTEX 16, 129-134
(6) Schiede E., Mischke U., Roll R. and Kayser D. (1992). A National Validation Study of the Acute-Toxic-Class Method - An Alternative to the LD50 Test. Arch. Toxicol. 66, 455-470.
(7) Schiede E., Mischke U., Diener W. and Kayser D. (1994). The International Validation Study of the Acute-Toxic-Class Method (Oral). Arch. Toxicol. 69, 659-670.
(8) OECD (2001) Guidance Document on Acute Oral Toxicity Testing. Environmental Health and Safety Monograph Series on Testing and Assessment N. 24. Paris.
(9) OECD (2000) Guidance Document on the Recognition, Assessment and Use of Clinical Signs as Humane Endpoints for Experimental Animals Used in Safety Evaluation. Environmental Health and Safety Monograph Series on Testing and Assessment N 19.
(10) OECD (1998) Harmonized Integrated Hazard Classification System For Human Health And Environmental Effects Of Chemical Substances as endorsed by the 28th Joint Meeting of the Chemicals Committee and the Working Party on Chemicals in November 1998, Part 2, S. 11 (http:// webnet1.oecd.org/oecd/pages/home/displaygeneral/0,3380,EN-documents-521-14-no-24-no-0,FF.html),
(11) Lipnick R.L., Cotruvo, J.A., Hill R.N., Bruce R.D., Stitzel K.A., Walker A.P., Chu I.; Goddard M., Segal L., Springer J.A. and Myers R.C. (1995) Comparison of the Upand Down, Conventional LD50, and Fixed Dose Acute Toxicity Procedures. Fd. Chem. Toxicol 33, 223-231.
(12) Chan P.K. and A.W. Hayes. (1994). Chap. 16. Acute Toxicity and Eye Irritancy. Principles and Methods of Toxicology. Third Edition. A.W. Hayes, Editor. Raven Press, Ltd, New York, USA.
| Zu beachtende Vorgehensweise für alle Startdosen | Anlage 1 |
Allgemeine Hinweise
Die in dieser Anlage dargestellten Prüfschemata geben für jede Ausgangsdosis die jeweils zu beachtende Vorgehensweise an.
- Anlage 1A: Startdosis 5 mg pro kg Körpergewicht
- Anlage 1B: Startdosis 50 mg pro kg Körpergewicht
- Anlage 1C: Startdosis 300 mg pro kg Körpergewicht
- Anlage 1D: Startdosis 2.000 mg pro kg Körpergewicht
Der Testverlauf folgt je nach Anzahl der auf humane Weise getöteten oder gestorbenen Versuchstiere den angegebenen Pfeilen.
| Prüfverfahren bei einer Startdosis von 5 mg pro kg Körpergewicht | Anlage 1A |
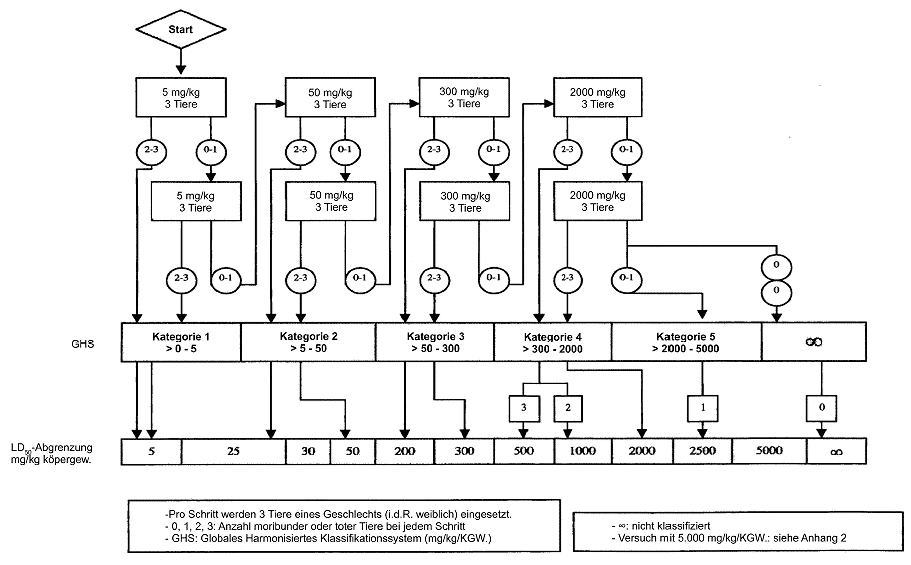
| Prüfverfahren bei einer Startdosis von 50 mg pro kg Körpergewicht | Anlage 1B |

| Prüfverfahren bei einer Startdosis von 300 mg pro kg Körpergewicht | Anlage 1C |

| Prüfverfahren bei einer Startdosis von 2.000 mg pro kg Körpergewicht | Anlage 1D |

| Kriterien für die Klassifizierung von Testsubstanzen mit erwarteten LD50-Werten über 2.000 mg/kg ohne erforderliche Tests | Anlage 2 |
Die Kriterien für die Gefahrenkategorie 5 sollen die Identifikation von Testsubstanzen ermöglichen, die eine vergleichsweise geringe akute Toxizitätsgefahr aufweisen, die aber unter bestimmten Umständen eine Gefahr für anfällige Bevölkerungsgruppen darstellen.
Bei diesen Substanzen wird von einer oralen oder dermalen LD50 im Bereich 2.000-5.000 mg/kg bzw. von vergleichbaren Dosen für andere Verabreichungswege ausgegangen.
Die Testsubstanz sollte in den folgenden Fällen in die Gefahrenkategorie 2.000 mg/kg < LD50 < 5.000 mg/kg (GHS-Kategorie 5) eingestuft werden:
- wenn eines der Prüfschemata - aus Anlage 1A-1D aufgrund von Mortalitätsfällen zu dieser Kategorie führt;
- wenn bereits zuverlässige Erkenntnisse dafür vorliegen, dass der LD50-Wert im Bereich der Kategorie 5 liegt, oder wenn andere Tierversuche oder toxische Wirkungen auf Menschen akute Folgen für die menschlichen Gesundheit erwarten lassen;
- wenn nach Extrapolierung, Schätzung oder Messung von Daten die Zuordnung zu einer höheren Gefahrenklasse nicht gerechtfertigt ist und
- zuverlässige Informationen vorliegen, die auf signifikante toxische Wirkungen bei Menschen hinweisen, oder
- Mortalitäten bei oraler Verabreichung in Versuchen mit Dosen bis zu der Kategorie 4 auftreten, oder
- eine fachkundige Beurteilung bei Versuchen mit Dosen bis zu den in Kategorie 4 genannten Werten signifikante klinische Toxizitätsanzeichen bestätigt (außer Durchfall, Haaraufrichtung oder zerzaustes Fell), oder
- eine fachkundige Beurteilung verlässliche Informationen bestätigt, die aus den anderen Tierversuchen ein Potenzial für signifikante akute Wirkungen erkennen lassen.
Versuche mit Dosen über 2.000 mg/kg
Aus Tierschutzgründen wird von Tierversuchen im Bereich der Kategorie 5 (5.000 mg/kg) abgeraten; diese Versuche sollen nur dann in Erwägung gezogen werden, wenn die Ergebnisse eines solchen Versuchs für den Schutz der Gesundheit von Menschen oder Tieren oder der Umwelt mit hoher Wahrscheinlichkeit direkt relevant wären (10). Weitere Versuche mit noch höheren Dosierungen sollen nicht durchgeführt werden.
Wenn Versuche mit einer Dosis von 5.000 mg/kg notwendig sind, ist nur ein Schritt (d. h. drei Tiere) erforderlich. Wenn das erste Versuchstier stirbt, wird der Versuch mit einer Dosis von 2.000 mg/kg gemäß den Prüfschemata in Anlage 1 fortgesetzt. Wenn das erste Tier überlebt, wird die Substanz zwei weiteren Tieren verabreicht. Wenn nur eines der drei Tiere stirbt, wird ein LD50-Wert von über 5.000 mg/kg angenommen. Wenn beide Tiere sterben, wird der Versuch mit der Dosis von 2.000 mg/kg fortgesetzt.
| Prüfverfahren B.1 tris | Anlage 3 |
Anleitung für die Klassifizierung gemäß dem EU-System zur Überbrückung des Übergangszeitraums bis zur vollständigen Umsetzung des "Globalen Harmonisierten Systems" (GHS) (Auszug aus Literaturhinweis (8))



 | weiter . |  |
...
X
⍂
↑
↓
