Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. ▢ Regelwerk, EU 2021, Lebensmittel - EU Bund |
Durchführungsverordnung (EU) 2021/1318 der Kommission vom 9. August 2021 zur Berichtigung der Durchführungsverordnung (EU) 2017/2470 zur Erstellung der Unionsliste der neuartigen Lebensmittel, der Entscheidung 2008/968/EG zur Genehmigung des Inverkehrbringens von arachidonsäurereichem Öl aus Mortierella alpina als neuartige Lebensmittelzutat und der Durchführungsverordnung (EU) 2020/484 zur Genehmigung des Inverkehrbringens von Lacto-N-tetraose als neuartiges Lebensmittel
(Text von Bedeutung für den EWR)
(ABl. L 286 vom 10.08.2021 S. 5)
Die Europäische Kommission -
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) 2015/2283 des Europäischen Parlaments und des Rates vom 25. November 2015 über neuartige Lebensmittel, zur Änderung der Verordnung (EU) Nr. 1169/2011 des Europäischen Parlaments und des Rates und zur Aufhebung der Verordnung (EG) Nr. 258/97 des Europäischen Parlaments und des Rates und der Verordnung (EG) Nr. 1852/2001 der Kommission 1, insbesondere auf Artikel 12,
in Erwägung nachstehender Gründe:
(1) Gemäß Artikel 8 der Verordnung (EU) 2015/2283 musste die Kommission bis zum 1. Januar 2018 die Unionsliste der neuartigen Lebensmittel erstellen, die gemäß der Verordnung (EG) Nr. 258/97 des Europäischen Parlaments und des Rates 2 genehmigt oder gemeldet wurden.
(2) Die Unionsliste der gemäß der Verordnung (EG) Nr. 258/97 genehmigten oder gemeldeten neuartigen Lebensmittel wurde mit der Durchführungsverordnung (EU) 2017/2470 der Kommission 3 erstellt.
(3) Die Kommission hat Fehler im Anhang der Durchführungsverordnung (EU) 2017/2470 festgestellt. Um Klarheit und Rechtssicherheit für die Lebensmittelunternehmer und die zuständigen Behörden der Mitgliedstaaten zu schaffen, sind Berichtigungen erforderlich, damit die Unionsliste der neuartigen Lebensmittel ordnungsgemäß umgesetzt und verwendet werden kann.
(4) Das neuartige Lebensmittel "arachidonsäurereiches Öl aus Mortierella alpina" wurde unter bestimmten Verwendungsbedingungen mit der Entscheidung 2008/968/EG der Kommission 4, von der zuständigen niederländischen Behörde 5 und auch gemäß Artikel 5 der Verordnung (EG) Nr. 258/97 zugelassen. Die Angabe der entsprechenden Lebensmittelkategorie "Lebensmittel für besondere medizinische Zwecke für Frühgeborene im Sinne der Verordnung (EU) Nr. 609/2013" nimmt irrtümlicherweise nur auf Frühgeborene Bezug; die Lebensmittelkategorie der Genehmigung sollte sich jedoch nicht allein auf Frühgeborene, sondern auf Säuglinge insgesamt beziehen. Daher ist es notwendig, Artikel 1 der Entscheidung 2008/968/EG und den Eintrag "Arachidonsäurereiches Öl aus dem Pilz Mortierella alpina" in Tabelle 1 des Anhangs der Durchführungsverordnung (EU) 2017/2470 zu berichtigen.
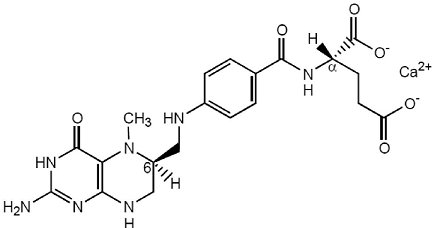
(5) Das neuartige Lebensmittel "Calcium-L-methylfolat" wurde von der zuständigen irischen Behörde im Januar 2008 gemäß den Bestimmungen der Verordnung (EG) Nr. 258/97 unter bestimmten Verwendungsbedingungen zugelassen, und zwar auf Grundlage einer befürwortenden Stellungnahme der Europäischen Behörde für Lebensmittelsicherheit zur Sicherheit des neuartigen Lebensmittels 6 . Das neuartige Lebensmittel wurde irrtümlicherweise nicht in die ursprüngliche Unionsliste aufgenommen. Daher sollte "Calcium-L-methylfolat" in die Unionsliste zugelassener neuartiger Lebensmittel aufgenommen werden, auch angesichts der Tatsache, dass "Calcium-L-methylfolat" mit der Delegierten Verordnung (EU) 2021/571 der Kommission 7 als Folatquelle in Säuglingsanfangsnahrung, Folgenahrung, Getreidebeikost und anderer Beikost zugelassen wurde.
(6) Das neuartige Lebensmittel "Lacto-N-tetraose ("LNT") (mikrobiell)" wurde mit der Durchführungsverordnung (EU) 2020/484 der Kommission 8 unter bestimmten Verwendungsbedingungen zugelassen. In den Spezifikationen ist als chemische Formel von Lacto-N-tetraose irrtümlicherweise C26H45O21 statt der richtigen Formel C26H45NO21 angegeben. In der Beschreibung von Lacto-N-tetraose fehlt irrtümlicherweise der Zusatz "oder Agglomerat", und der in geringem Umfang vorhandene Bestandteil "Lacto-N-triose II" wird irrtümlicherweise als "Lacto-N-tetraose II" bezeichnet. Daher sollten die Spezifikationen von "Lacto-N-tetraose ("LNT") (mikrobiell)" in Tabelle 2 des Anhangs der Durchführungsverordnung (EU) 2020/484 und der Durchführungsverordnung (EU) 2017/2470 in Bezug auf die chemische Formel von Lacto-N-tetraose und auf Lacto-N-tetraose II entsprechend berichtigt werden.
(7) Die Entscheidung 2008/968/EG und die Durchführungsverordnungen (EU) 2017/2470 und (EU) 2020/484 sollten entsprechend berichtigt werden.
(8) Die in der vorliegenden Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für Pflanzen, Tiere, Lebensmittel und Futtermittel
- hat folgende Verordnung erlassen:
Artikel 1 Absatz 2 der Entscheidung 2008/968/EG wird wie folgt berichtigt:
"Die Hinzufügung von Pilzöl aus Mortierella alpina zu Säuglingsanfangsnahrung und Folgenahrung wird durch seinen Gehalt an Arachidonsäure gemäß den Vorschriften in Anhang I Nummer 5.7 und Anhang II Nummer 4.7 der Richtlinie 2006/141/EG beschränkt. Seine Verwendung in Säuglingsanfangsnahrung erfolgt im Einklang mit den Bestimmungen der Richtlinie 89/398/EWG des Rates * zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über Lebensmittel, die für eine besondere Ernährung bestimmt sind.
______
*) Richtlinie 89/398/EWG des Rates vom 3. Mai 1989 zur Angleichung der Rechtsvorschriften der Mitgliedstaaten über Lebensmittel, die für eine besondere Ernährung bestimmt sind (ABl. L 186 vom 30.06.1989 S. 27)."
Der Anhang der Durchführungsverordnung (EU) 2020/484 wird gemäß dem Anhang der vorliegenden Verordnung berichtigt.
Der Anhang der Durchführungsverordnung (EU) 2017/2470 wird gemäß dem Anhang der vorliegenden Verordnung berichtigt.
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 9. August 2021.
2) Verordnung (EG) Nr. 258/97 des Europäischen Parlaments und des Rates vom 27. Januar 1997 über neuartige Lebensmittel und neuartige Lebensmittelzutaten (ABl. L 43 vom 14.02.1997 S. 1).
3) Durchführungsverordnung (EU) 2017/2470 der Kommission vom 20. Dezember 2017 zur Erstellung der Unionsliste der neuartigen Lebensmittel gemäß der Verordnung (EU) 2015/2283 des Europäischen Parlaments und des Rates über neuartige Lebensmittel (ABl. L 351 vom 30.12.2017 S. 72).
4) Entscheidung 2008/968/EG der Kommission vom 12. Dezember 2008 zur Genehmigung des Inverkehrbringens von arachidonsäurereichem Öl aus Mortierella alpina als neuartige Lebensmittelzutat im Sinne der Verordnung (EG) Nr. 258/97 des Europäischen Parlaments und des Rates (ABl. L 344 vom 20.12.2008 S. 123).
5) Schreiben vom 19. Dezember 2011 (https://ec.europa.eu/food/system/files/2016-10/novel-food_authorisation_2011_auth-letter_arachidonic_acid_rich_oil_en.pdf).
6) https://doi.org/10.2903/j.efsa.2004.135.
7) Delegierte Verordnung (EU) 2021/571 der Kommission vom 20. Januar 2021 zur Änderung des Anhangs der Verordnung (EU) Nr. 609/2013 des Europäischen Parlaments und des Rates im Hinblick auf die Liste der Stoffe, die Säuglingsanfangsnahrung und Folgenahrung sowie Getreidebeikost und anderer Beikost zugesetzt werden dürfen (ABl. L 120 vom 08.04.2021 S. 1).
8) Durchführungsverordnung (EU) 2020/484 der Kommission vom 2. April 2020 zur Genehmigung des Inverkehrbringens von Lacto-N-tetraose als neuartiges Lebensmittel gemäß der Verordnung (EU) 2015/2283 des Europäischen Parlaments und des Rates sowie zur Änderung der Durchführungsverordnung (EU) 2017/2470 der Kommission (ABl. L 103 vom 03.04.2020 S. 3).
| Anhang |
1. Der Anhang der Durchführungsverordnung (EU) 2017/2470 wird wie folgt berichtigt:
a) Der Eintrag "Arachidonsäurereiches Öl aus dem Pilz Mortierella alpina" in Tabelle 1 (Zugelassene neuartige Lebensmittel) erhält folgende Fassung:
| Zugelassenes neuartiges Lebensmittel | Bedingungen, unter denen das neuartige Lebensmittel verwendet werden darf | zusätzliche spezifische Kennzeichnungsvorschriften | sonstige Anforderungen | |
| "Arachidonsäurereiches Öl aus dem Pilz Mortierella alpina | Spezifizierte Lebensmittelkategorie | Höchstgehalte | Die Bezeichnung des neuartigen Lebensmittels, die in der Kennzeichnung des jeweiligen Lebensmittels anzugeben ist, lautet "Öl aus Mortierella alpina" oder " Mortierella-alpina-Öl." | |
| Säuglingsanfangsnahrung und Folgenahrung im Sinne der Verordnung (EU) Nr. 609/2013 | Gemäß der Verordnung (EU) Nr. 609/2013 | |||
| Lebensmittel für besondere medizinische Zwecke für Säuglinge im Sinne der Verordnung (EU) Nr. 609/2013 | Gemäß der Verordnung (EU) Nr. 609/2013 | |||
b) Zwischen dem Eintrag "Öl aus Calanus finmarchicus" und dem Eintrag "Kaubase (Monomethoxypolyethylenglycol)" wird in Tabelle 1 (Zugelassene neuartige Lebensmittel) und Tabelle 2 (Spezifikationen) folgender Eintrag eingefügt:
- Tabelle 1:
| "Calcium-L-Methylfolat | Spezifizierte Lebensmittelkategorie | Höchstgehalte (ausgedrückt als Folsäure) | Die Bezeichnung des neuartigen Lebensmittels, die in der Kennzeichnung des jeweiligen Lebensmittels anzugeben ist, lautet "Calcium-L-Methylfolat." | ||
| Lebensmittel für besondere medizinische Zwecke und Tagesration für gewichtskontrollierende Ernährung im Sinne der Verordnung (EU) Nr. 609/2013 | Gemäß der Verordnung (EU) Nr. 609/2013 | ||||
| Säuglingsanfangsnahrung und Folgenahrung im Sinne der Verordnung (EU) Nr. 609/2013 | Gemäß der Verordnung (EU) Nr. 609/2013 | ||||
| Getreidebeikost und andere Beikost für Säuglinge und Kleinkinder im Sinne der Verordnung (EU) Nr. 609/2013 | Gemäß der Verordnung (EU) Nr. 609/2013 | ||||
| Nahrungsergänzungsmittel im Sinne der Richtlinie 2002/46/EG, ausgenommen solche für Säuglinge und Kleinkinder | Gemäß der Richtlinie 2002/46/EG | ||||
| Gemäß der Verordnung (EG) Nr. 1925/2006 angereicherte Lebensmittel | Gemäß der Verordnung (EU) Nr. 1925/2006 |
- Tabelle 2:
| "Calcium-L-Methylfolat | Beschreibung: Das neuartige Lebensmittel wird durch chemische Synthese aus Folsäure hergestellt. Es handelt sich um ein weißes bis hellgelbliches, fast geruchloses, kristallines Pulver, das in Wasser mäßig löslich ist und in den meisten organischen Lösungsmitteln sehr gering löslich oder unlöslich ist. Definition: Merkmale Mikrobiologische Kriterien: |
| KBE: | koloniebildende Einheiten" |
2. Nummer 2 des Anhangs der Durchführungsverordnung (EU) 2020/484 wird wie folgt berichtigt.
Der Eintrag für "Lacto-N-tetraose ("LNT") (mikrobiell)" in Tabelle 2 (Spezifikationen) erhält folgende Fassung:
| "Lacto- N-tetraose ("LNT") (mikrobiell) | Definition: Chemische Formel: C26H45NO21 Chemische Bezeichnung: β-d-Galactopyranosyl-(1→ 3)-2-acetamido-2-desoxy-β-d-glucopyranosyl-(1 → 3)β-d-galactopyranosyl-(1 → 4)-D-glucopyranose Molmasse: 707,63 Da CAS-Nr. 14116-68-8 Beschreibung: Quelle: Merkmale/Zusammensetzung: Mikrobiologische Kriterien: |
KBE: koloniebildende Einheiten"
 | ENDE |
...
X
⍂
↑
↓