 Für einen individuellen Ausdruck passen Sie bitte die
Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk, EU 2024, Lebensmittel - Futtermittel
 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk, EU 2024, Lebensmittel - Futtermittel |
Durchführungsverordnung (EU) 2024/771 der Kommission vom 29. Februar 2024 zur Änderung der Verordnung (EG) Nr. 152/2009 zur Festlegung der Probenahmeverfahren und Analysemethoden für die amtliche Untersuchung von Futtermitteln
(Text von Bedeutung für den EWR)
(ABl. L 2024/771 vom 15.03.2024)
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Verordnung (EU) 2017/625 des Europäischen Parlaments und des Rates vom 15. März 2017 über amtliche Kontrollen und andere amtliche Tätigkeiten zur Gewährleistung der Anwendung des Lebens- und Futtermittelrechts und der Vorschriften über Tiergesundheit und Tierschutz, Pflanzengesundheit und Pflanzenschutzmittel, zur Änderung der Verordnungen (EG) Nr. 999/2001, (EG) Nr. 396/2005, (EG) Nr. 1069/2009, (EG) Nr. 1107/2009, (EU) Nr. 1151/2012, (EU) Nr. 652/2014, (EU) 2016/429 und (EU) 2016/2031 des Europäischen Parlaments und des Rates, der Verordnungen (EG) Nr. 1/2005 und (EG) Nr. 1099/2009 des Rates sowie der Richtlinien 98/58/EG, 1999/74/EG, 2007/43/EG, 2008/119/EG und 2008/120/EG des Rates und zur Aufhebung der Verordnungen (EG) Nr. 854/2004 und (EG) Nr. 882/2004 des Europäischen Parlaments und des Rates, der Richtlinien 89/608/EWG, 89/662/EWG, 90/425/EWG, 91/496/EWG, 96/23/EG, 96/93/EG und 97/78/EG des Rates und des Beschlusses 92/438/EWG des Rates (Verordnung über amtliche Kontrollen) 1, insbesondere auf Artikel 34 Absatz 6,
in Erwägung nachstehender Gründe:
(1) In der Verordnung (EG) Nr. 152/2009 der Kommission 2 sind die Probenahmeverfahren und Analysemethoden für die amtliche Untersuchung von Futtermitteln festgelegt.
(2) Die mit der Verordnung (EG) Nr. 152/2009 festgelegten Probenahmeverfahren und Analysemethoden sollten an den wissenschaftlichen und technologischen Fortschritt angepasst werden. Mehrere geringfügige Änderungen sollten in diese Verordnung aufgenommen werden; dabei sollte den mit der Anwendung der Analysemethoden gewonnenen Erfahrungen Rechnung getragen oder es sollten bestimmte Vorschriften präzisiert werden.
(3) Das in der Verordnung (EG) Nr. 152/2009 beschriebene Probenahmeverfahren eignet sich nicht für die Probenahme zur Kontrolle der mikrobiologischen Kontamination und ist daher vom Anwendungsbereich ausgenommen. Da es infolge der Änderung durch die Verordnung (EU) Nr. 691/2013 der Kommission 3 nicht mehr ausdrücklich vom Anwendungsbereich ausgenommen war, hat dies jedoch zu einer gewissen Verwirrung geführt, weshalb es erneut ausdrücklich vom Anwendungsbereich ausgenommen werden sollte.
(4) Es ist angezeigt, besondere Bestimmungen für die Probenahme von Futtermitteln einzuführen, die von Futtermittelunternehmern über Fernkommunikationsmittel zum Verkauf angeboten werden, da der Verkauf von Futtermitteln mithilfe von Fernkommunikationsmitteln zunimmt. Zusätzlich zu den Bestimmungen über die analytische Messunsicherheit und Wiederfindungsrate bei der Analyse auf unerwünschte Stoffe sollten solche Bestimmungen auch für die Analyse des Inhalts von Futtermittelzusatzstoffen eingeführt werden, da diese Bestimmungen auch dafür relevant sind. Da die Anwendung der Analysemethode zur Bestimmung von Harnstoff außerhalb des Zulassungsbereichs von Harnstoff als Futtermittelzusatzstoff nachweislich zu falschen Analyseergebnissen führt, sollte der Anwendungsbereich dieser Methode präzisiert und es sollten Informationen über die Bewertung der Methode und die Ergebnisse einer Ringstudie ergänzt werden.
(5) Mehrere in der Verordnung (EG) Nr. 152/2009 festgelegte Analysemethoden sollten gestrichen werden, da sie ihre Validität für den vorgesehenen Zweck verloren haben. Die Analysemethode für die Bestimmung flüchtiger stickstoffhaltiger Basen und die Methode zur Bestimmung von Carbonaten sollten gestrichen werden, da eine Kontrolle der Einhaltung nach dem Futtermittelrecht der Union nicht mehr rechtlich vorgeschrieben ist. Die geltende Analysemethode zur Bestimmung von Diclazuril enthält redaktionelle Fehler und liefert somit keine zuverlässigen Analyseergebnisse. Sie sollte daher durch eine veränderte Methode ersetzt werden, die nachweislich zuverlässige Ergebnisse liefert. Neue Analysemethoden für die Bestimmung von freiem und Gesamtgossypol haben nachweislich gezeigt, dass die mit der Verordnung (EG) Nr. 152/2009 eingeführte Analysemethode zur Bestimmung von freiem und Gesamtgossypol keine zuverlässigen Ergebnisse liefert und daher gestrichen und durch einen Verweis auf europäische Normen (EN) ersetzt werden sollte. Die Analysemethoden zur Untersuchung von Futtermitteln auf das Vorhandensein nicht mehr zugelassener Zusatzstoffe sollten gestrichen werden, da inzwischen empfindlichere Screening-Verfahren und Analysemethoden entwickelt wurden.
(6) Zusätzlich zu den in den Anhängen dieser Verordnung beschriebenen Analysemethoden sollte ein Verweis auf europäische Normen (EN) im Hinblick auf ihre Verwendung in amtlichen Kontrollen aufgenommen werden.
(7) Da der neue Futtermittelzusatzstoff Amprolium mit der Durchführungsverordnung (EU) 2021/2047 der Kommission 4 zugelassen wurde, sollte in Anhang IV der Verordnung (EG) Nr. 152/2009 eine Analysemethode zur Bestimmung von Amprolium aufgenommen werden.
(8) Da die Änderungen der Verordnung (EG) Nr. 152/2009 wesentlich sind und mehrere Bestimmungen in ihren Anhängen betreffen, ist es aus Gründen der Klarheit angezeigt, diese Anhänge vollständig zu ersetzen.
(9) Die in dieser Verordnung vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für Pflanzen, Tiere, Lebensmittel und Futtermittel
- hat folgende Verordnung erlassen:
Artikel 1 Änderungen der Verordnung (EG) Nr. 152/2009
Die Verordnung (EG) Nr. 152/2009 wird wie folgt geändert:
1. Artikel 1 Absatz 1 erhält folgende Fassung:
"Die Probenahmen für die amtliche Untersuchung von Futtermitteln, insbesondere auf ihre Bestandteile, eingeschlossen Material, das genetisch veränderte Organismen (GVO) enthält, aus ihnen besteht oder aus ihnen hergestellt ist, Futtermittelzusatzstoffe gemäß der Verordnung (EG) Nr. 1831/2003 des Europäischen Parlaments und des Rates * und unerwünschte Stoffe gemäß der Richtlinie 2002/32/EG des Europäischen Parlaments und des Rates **, erfolgen mit Ausnahme der Probenahme für die Untersuchung auf mikrobiologische Kontamination nach den in Anhang I aufgeführten Verfahren.
____
*) Verordnung (EG) Nr. 1831/2003 des Europäischen Parlaments und des Rates vom 22. September 2003 über Zusatzstoffe zur Verwendung in der Tierernährung (ABl. L 268 vom 18.10.2003 S. 29)."
**) Richtlinie 2002/32/EG des Europäischen Parlaments und des Rates vom 7. Mai 2002 über unerwünschte Stoffe in der Tierernährung (ABl. L 140 vom 30.05.2002 S. 10)."
2. Anhang I erhält die Fassung des Anhangs I der vorliegenden Verordnung.
3. Anhang II erhält die Fassung des Anhangs II der vorliegenden Verordnung.
4. Anhang III erhält die Fassung des Anhangs III der vorliegenden Verordnung.
5. Anhang IV erhält die Fassung des Anhangs IV der vorliegenden Verordnung.
6. Anhang V erhält die Fassung des Anhangs V der vorliegenden Verordnung.
7. Anhang VII erhält die Fassung des Anhangs VI der vorliegenden Verordnung.
8. Anhang VIII wird gestrichen.
Artikel 2 Inkrafttreten
Diese Verordnung tritt am zwanzigsten Tag nach ihrer Veröffentlichung im Amtsblatt der Europäischen Union in Kraft.
Diese Verordnung ist in allen ihren Teilen verbindlich und gilt unmittelbar in jedem Mitgliedstaat.
Brüssel, den 29. Februar 2024.
2) Verordnung (EG) Nr. 152/2009 der Kommission vom 27. Januar 2009 zur Festlegung der Probenahmeverfahren und Analysemethoden für die amtliche Untersuchung von Futtermitteln (ABl. L 54 vom 26.02.2009 S. 1).
3) Verordnung (EU) Nr. 691/2013 der Kommission vom 19. Juli 2013 zur Änderung der Verordnung (EG) Nr. 152/2009 hinsichtlich der Probenahmeverfahren und Analysemethoden (ABl. L 197 vom 20.07.2013 S. 1).
4) Durchführungsverordnung (EU) 2021/2047 der Kommission vom 23. November 2021 zur Zulassung von Amproliumhydrochlorid (COXAM) als Futtermittelzusatzstoff für Masthühner und Junghennen (Zulassungsinhaber: HuvePharma NV) (ABl. L 418 vom 24.11.2021 S. 13).
| Anhang I |
"Anhang I
Probenahmeverfahren
1. Zweck und Anwendungsbereich
Die zur amtlichen Untersuchung bestimmten Futtermittelproben werden gemäß den nachstehenden Verfahren entnommen. Die so gewonnenen Proben gelten als repräsentativ für die Teilpartien.
Zweck der repräsentativen Beprobung ist es, einen kleinen Teil einer Partie zu untersuchen und durch die Bestimmung eines spezifischen Merkmals bei diesem Teil den Durchschnittswert des Merkmals für die gesamte Partie zu ermitteln. Die Partie wird mittels wiederholter Entnahme von Einzelproben an verschiedenen Stellen der Partie untersucht. Diese Einzelproben werden zu einer Sammelprobe gemischt, aus der durch repräsentative Teilung repräsentative Endproben herzustellen sind.
Wenn bei der Sichtprüfung oder aufgrund anderer einschlägiger Informationen Teile des zu beprobenden Futtermittels einen Qualitätsunterschied zum übrigen Futtermittel derselben Partie aufweisen, werden diese Teile vom übrigen Futtermittel abgesondert und als getrennte Teilpartie behandelt. Ist eine Aufteilung des Futtermittels in getrennte Teilpartien nicht möglich, so wird das Futtermittel als eine einzige Partie beprobt. In solchen Fällen ist dies im Probenahmebericht zu vermerken.
Ist ein Futtermittel, das gemäß den Bestimmungen der vorliegenden Verordnung beprobt wurde und nachweislich die EU-Anforderungen nicht erfüllt, Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
Auch Futtermittel, die gemäß Artikel 11 Absatz 3 der Verordnung (EG) Nr. 767/2009 des Europäischen Parlaments und des Rates 1 über eine Fernkommunikationstechnik zum Verkauf angeboten werden, können beprobt werden. Die Beprobung von Futtermitteln, die über eine Fernkommunikationstechnik zum Verkauf angeboten werden, unterliegt grundsätzlich den in diesem Anhang dargelegten Punkten. Spezifische Aspekte der Beprobung über Fernkommunikation angebotener Futtermittel werden in Nummer 11 beschrieben.
2. Begriffsbestimmungen
3. Allgemeine Bestimmungen
Der Plombenstempel sollte eindeutig identifizierbar und gut sichtbar sein.
4. Geräte
4.1. Die Geräte zur Probenahme müssen aus Materialien bestehen, die die zu beprobenden Erzeugnisse nicht kontaminieren können. Geräte, die für eine mehrfache Anwendung vorgesehen sind, müssen leicht zu reinigen sein, damit eine Kreuzkontamination vermieden wird.
4.2. Empfohlene Geräte für die Probenahme fester Futtermittel
4.2.1. Manuelle Probenahme
4.2.1.1. Probenahmeschaufel mit ebenem Boden und rechteckig hochgebogenem Rand.
4.2.1.2. Probenahmestab mit langem Schlitz oder Kammern. Die Dimensionierung des Probenahmestabes ist den Merkmalen der Teilpartie (Tiefe des Behälters, Größe des Sacks usw.) und der Partikelgröße des Futtermittels anzupassen.
Falls es sich um einen Probenahmestab mit mehreren Öffnungen handelt, sollten diese durch Kammern oder fortlaufend versetzte Öffnungen voneinander getrennt sein, damit sichergestellt ist, dass die Probe an verschiedenen Stellen entlang des Probenahmestabes entnommen wird.
4.2.2. Mechanische Probenahme
Geeignete mechanische Geräte dürfen zur Probenahme aus in Bewegung befindlichen Futtermitteln verwendet werden. Ein mechanisches Gerät gilt als geeignet, wenn mindestens der gesamte Fließquerschnitt beprobt wird.
Die Probenahme aus in Bewegung befindlichen Futtermitteln (bei hohen Durchflussraten) kann mittels automatischer Probenehmer erfolgen.
4.2.3. Probenteiler
Soweit möglich und sinnvoll, sollten zur Herstellung reduzierter Proben Geräte verwendet werden, die zur Zerlegung der Probe in ungefähr gleiche Teile in repräsentativer Form bestimmt sind.
5. Quantitative Anforderungen hinsichtlich der Anzahl von Einzelproben
5.1. Quantitative Anforderungen an Einzelproben bezüglich der Untersuchung auf Stoffe oder Erzeugnisse, die gleichmäßig im Futtermittel verteilt sind
5.1.1. Feste Futtermittel in loser Form
| Teilpartie | Mindestanzahl der Einzelproben |
| ≤ 2,5 t | 7 |
| > 2,5 t | √ (20-mal die Anzahl von Tonnen, aus denen die Teilpartie besteht) *, bis zu 40 Einzelproben |
| *) Wenn sich hierbei eine Bruchzahl ergibt, ist diese auf die nächsthöhere ganze Zahl aufzurunden. | |
5.1.2. Flüssige Futtermittel in loser Form
| Teilpartie | Mindestanzahl der Einzelproben |
| ≤ 2,5 t bzw. ≤ 2.500 l | 4 * |
| > 2,5 t bzw. > 2.500 l | 7 * |
| *) Ist eine Homogenisierung der Flüssigkeit nicht möglich, so muss die Anzahl der Einzelproben erhöht werden. | |
5.1.3. Verpackte Futtermittel
Futtermittel (fest und flüssig) können in Beuteln, Säcken, Dosen, Fässern usw. verpackt sein, die in der Tabelle als Einheiten bezeichnet werden. Große Einheiten (≥ 500 kg bzw. l) sind nach den Vorschriften für lose Futtermittel (siehe Nummern 5.1.1 und 5.1.2) zu beproben.
| Teilpartie | Mindestanzahl der Einheiten, aus denen (mindestens) eine Einzelprobe zu entnehmen ist * |
| 1 bis 20 Einheiten | 1 Einheit ** |
| 21 bis 150 Einheiten | 3 Einheiten ** |
| 151 bis 400 Einheiten | 5 Einheiten ** |
| > 400 Einheiten | ¼ der √ (Anzahl von Einheiten, aus der die Teilpartie besteht) ***, bis zu 40 Einheiten |
| *) Kann durch das Öffnen einer Einheit die Analyse beeinträchtigt werden (z.B. leicht verderbliches Nassfutter), so gilt die ungeöffnete Einheit als Einzelprobe.
**) Bei Einheiten, deren Inhalt höchstens 1 kg bzw. 1 l beträgt, gilt der Inhalt einer Originaleinheit als Einzelprobe. ***) Wenn sich hierbei eine Bruchzahl ergibt, ist diese auf die nächsthöhere ganze Zahl aufzurunden. | |
5.1.4. Futterblöcke und Lecksteine
Zu beproben ist mindestens ein Futterblock oder Leckstein je Teilpartie zu 25 Einheiten, die Höchstzahl beträgt vier Futterblöcke oder Lecksteine.
Bei Futterblöcken oder Lecksteinen mit einem Gewicht von jeweils maximal 1 kg gilt der Inhalt eines Futterblocks oder Lecksteins als Einzelprobe.
5.1.5. Raufutter/Grünfutter
| Teilpartie | Mindestanzahl der Einzelproben * |
| ≤ 5 t | 5 |
| > 5 t | √ (5-mal die Anzahl von Tonnen, aus der die Teilpartie besteht) **, bis zu 40 Einzelproben |
| *) In bestimmten Fällen (z.B. bei Silage) können die vorgeschriebenen Einzelproben nicht ohne eine unannehmbare Beschädigung der Partie entnommen werden. In diesen Fällen ist ein alternatives Probenahmeverfahren zulässig, und entsprechende Leitlinien für die Beprobung solcher Partien können hier abgerufen werden: https://food.ec.europa.eu/system/files/2016-10/animal-feed-guidance_documents_691_2013_en.pdf
**) Wenn sich hierbei eine Bruchzahl ergibt, ist diese auf die nächsthöhere ganze Zahl aufzurunden. | |
5.2. Quantitative Anforderungen an Einzelproben bezüglich der Untersuchung auf Bestandteile oder Stoffe, die ungleichmäßig im Futtermittel verteilt sein können
Diese quantitativen Anforderungen an Einzelproben gelten in folgenden Fällen:
Hat die Untersuchungsbehörde den starken Verdacht, dass eine solche ungleichmäßige Verteilung auch im Fall einer Kreuzkontamination durch einen Bestandteil oder einen Stoff in einem Futtermittel-Ausgangserzeugnis auftritt, so können die in der nachstehenden Tabelle festgelegten quantitativen Anforderungen gestellt werden.
| Teilpartie | Mindestanzahl der Einzelproben |
| < 80 t | Siehe quantitative Anforderungen in Nummer 5.1. Die Anzahl der zu entnehmenden Einzelproben ist mit dem Faktor 2,5 zu multiplizieren. |
| ≥ 80 t | 100 |
5.3. Quantitative Anforderungen an Einzelproben bei sehr großen Partien
Bei großen Teilpartien (> 500 t) ist die Anzahl der zu entnehmenden Einzelproben wie folgt zu festzulegen: 40 Einzelproben + √-Tonnen für die Untersuchung auf Stoffe oder Erzeugnisse, die im gesamten Futtermittel gleichmäßig verteilt sind, oder 100 Einzelproben + √-Tonnen für die Untersuchung auf Bestandteile oder Stoffe, die ungleichmäßig im Futtermittel verteilt sein können.
6. Quantitative Anforderungen an Sammelproben
Je Teilpartie ist eine einzelne Sammelprobe erforderlich.
| Art des Futtermittels | Mindestgröße der Sammelprobe * ** | |
| 6.1. | Lose Futtermittel | 4 kg |
| 6.2. | Verpackte Futtermittel | 4 kg *** |
| 6.3. | Flüssige oder halbflüssige Futtermittel | 4 l |
| 6.4. | Futterblöcke oder Lecksteine | |
| 6.4.1. | mit einem Einzelgewicht von mehr als 1 kg | 4 kg |
| 6.4.2. | mit einem Einzelgewicht von höchstens 1 kg | Gewicht von 4 Originalblöcken oder -steinen |
| 6.5. | Raufutter/Grünfutter | 4 kg **** |
| *) Ist das beprobte Futtermittel hochwertig, kann eine kleinere Menge als Sammelprobe gewählt werden, sofern dies im Probenahmebericht beschrieben und dokumentiert wird.
**) Gemäß der Verordnung (EU) Nr. 619/2011 der Kommission vom 24. Juni 2011 zur Festlegung der Probenahme- und Analyseverfahren für die amtliche Untersuchung von Futtermitteln im Hinblick auf genetisch veränderte Ausgangserzeugnisse, für die ein Zulassungsverfahren anhängig ist oder deren Zulassung abläuft (ABl. L 166 vom 25.06.2011 S. 9) muss die Sammelprobe für die Untersuchung auf genetisch veränderte Ausgangserzeugnisse mindestens 35.000 Samen/Körner enthalten. Dies bedeutet, dass die Größe der Sammelprobe bei Mais mindestens 10,5 kg und bei Sojabohnen 7 kg betragen muss. Bei anderen Samen und Körnern wie Gerste, Hirse, Hafer, Reis, Roggen, Weizen und Raps entspricht die Größe der Sammelprobe von 4 kg mehr als 35.000 Samen/Körnern. ***) Bei verpackten Futtermitteln kann es ebenfalls vorkommen, dass - abhängig von der Größe der einzelnen Einheiten - die für die Sammelprobe vorgeschriebene Größe von 4 kg nicht erreicht werden kann. ****) Handelt es sich um Raufutter/Grünfutter mit geringer relativer Dichte (z.B. Heu, Stroh), sollte die Probengröße mindestens 1 kg betragen. | ||
7. Quantitative Anforderungen an Endproben
Endproben
Mindestens eine Endprobe muss analysiert werden. Die Menge der zur Analyse bestimmten Endproben darf nicht unter den nachstehend festgelegten Mindestmengen liegen:
| Feste Futtermittel | 500 g * ** *** **** |
| Flüssige oder halbflüssige Futtermittel | 500 ml * |
| *) Gemäß der Verordnung (EU) Nr. 619/2011 muss die Endprobe für die Untersuchung auf genetisch veränderte Ausgangserzeugnisse mindestens 10.000 Samen/Körner enthalten. Dies bedeutet, dass die Größe der Endprobe bei Mais mindestens 3.000 g und bei Sojabohnen 2.000 g betragen muss. Bei anderen Samen und Körnern wie Gerste, Hirse, Hafer, Reis, Roggen, Weizen und Raps entspricht die Größe der Sammelprobe von 500 g mehr als 10.000 Samen/Körnern.
**) Liegt die Größe der Sammelprobe erheblich unter 4 kg bzw. 4 l (siehe Fußnoten in Nummer 6), kann als Endprobe auch eine geringere Menge entnommen werden, sofern dies im Probenahmebericht beschrieben und dokumentiert wird. ***) Bei der Beprobung von Hülsenfrüchten, Getreidekörnern und Schalenfrüchten zur Bestimmung der Pflanzenschutzmittelrückstände muss gemäß der Richtlinie 2002/63/EG der Kommission vom 11. Juli 2002 zur Festlegung gemeinschaftlicher Probenahmemethoden zur amtlichen Kontrolle von Pestizidrückständen in und auf Erzeugnissen pflanzlichen und tierischen Ursprungs und zur Aufhebung der Richtlinie 79/700/EWG (ABl. L 187 vom 16.07.2002 S. 30) die Mindestgröße der Endprobe 1 kg betragen. ****) Bei Sichtprüfungen oder mikroskopischen Untersuchungen beträgt die zu untersuchende Endprobe 1 kg. | |
8. Probenahmeverfahren für sehr grosse Partien oder Partien, die so gelagert oder befördert werden, dass eine Beprobung der gesamten Partie nicht praktikabel ist
8.1. Allgemeine Grundsätze
Falls es die Art der Beförderung oder Lagerung einer Partie nicht gestattet, Einzelproben aus der gesamten Partie zu entnehmen, sollte die Beprobung solcher Partien vorzugsweise dann erfolgen, wenn sich die Partie im Fluss befindet.
Falls es sich um Großlager für Futtermittel handelt, sollten die Unternehmer dazu angehalten werden, Einrichtungen im Lager zu installieren, die eine (automatische) Beprobung der gesamten gelagerten Partie ermöglichen.
Im Fall der Anwendung der in diesem Punkt dargelegten Probenahmeverfahren wird der Futtermittelunternehmer oder sein Vertreter über das Probenahmeverfahren informiert. Wird dieses Probenahmeverfahren von dem Futtermittelunternehmer oder seinem Vertreter infrage gestellt, so muss dieser es der zuständigen Behörde auf Kosten des Unternehmers ermöglichen, die gesamte Partie zu beproben.
8.2. Große Partien, die per Schiff befördert werden
8.2.1. Dynamische Beprobung großer Partien, die per Schiff befördert werden
Die Beprobung großer Partien auf Schiffen ist vorzugsweise durchzuführen, wenn sich das Erzeugnis im Fluss befindet (dynamische Probenahme).
Die Probenahme hat je Laderaum (physisch abtrennbare Einheit) zu erfolgen. Die Laderäume werden allerdings nacheinander geleert, sodass die ursprüngliche physische Trennung nach der Weiterbeförderung in die Lagereinrichtungen nicht mehr besteht. Die Probenahme kann daher unter Bezug auf die ursprüngliche physische Trennung oder auf die Trennung nach der Beförderung in die Lagereinrichtungen erfolgen.
Das Löschen einer Schiffsladung kann mehrere Tage in Anspruch nehmen. In der Regel muss die Beprobung in regelmäßigen Abständen während der gesamten Dauer des Löschvorgangs erfolgen. Es ist jedoch nicht immer praktikabel oder sinnvoll, dass sich ein amtlicher Inspektor während des gesamten Löschvorgangs für die Probenahme vor Ort aufhält. Daher ist die Beprobung eines Teils (einer Teilpartie) der gesamten Partie zulässig Die Anzahl der Einzelproben wird unter Berücksichtigung des Umfangs der Teilpartie festgelegt.
Wird ein Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung beprobt und erfüllt diese Teilpartie nachweislich nicht die EU-Anforderungen, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
Auch wenn die amtliche Probe automatisch entnommen wird, muss ein Inspektor anwesend sein. Erfolgt die automatische Probenahme jedoch anhand voreingestellter Parameter, die während der Probenahme nicht verändert werden können, und werden die Einzelproben in einem verplombten Behälter gesammelt, was einen möglichen Betrug ausschließt, so ist die Anwesenheit eines Inspektors nur zu Beginn der Probenahme, bei jedem Wechsel des Probenbehälters und am Ende der Probenahme erforderlich.
8.2.2. Beprobung von Partien, die per Schiff befördert werden, durch statische Probenahme
Bei einer statischen Probenahme ist dasselbe Verfahren anzuwenden wie bei Lagereinrichtungen (Silos), die von oben zugänglich sind (siehe Nummer 8.4.1).
Die Probenahme muss am zugänglichen Teil der Partie/des Laderaums erfolgen (von oben). Die Anzahl der Einzelproben wird unter Berücksichtigung des Umfangs der Teilpartie festgelegt. Wird ein Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung beprobt und erfüllt diese Teilpartie nachweislich nicht die EU-Anforderungen, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
8.3. Beprobung großer Partien in Lagern
Die Probenahme muss am zugänglichen Teil der Partie erfolgen. Die Anzahl der Einzelproben wird unter Berücksichtigung des Umfangs der Teilpartie festgelegt. Wird ein Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung beprobt und erfüllt diese Teilpartie nachweislich nicht die EU-Anforderungen, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
8.4. Beprobung von Lagereinrichtungen (Silos)
8.4.1. Beprobung von Silos mit (leichtem) Zugang von oben
Die Probenahme muss am zugänglichen Teil der Partie erfolgen. Die Anzahl der Einzelproben wird unter Berücksichtigung des Umfangs der Teilpartie festgelegt. Wird ein Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung beprobt und erfüllt diese Teilpartie nachweislich nicht die EU-Anforderungen, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
8.4.2. Beprobung von Silos ohne Zugang von oben (geschlossene Silos)
8.4.2.1. Silos ohne Zugang von oben (geschlossene Silos) mit einer Größe über 100 Tonnen
In solchen Silos gelagerte Futtermittel können nicht statisch beprobt werden. Wenn das im Silo gelagerte Futtermittel beprobt werden muss und keine Möglichkeit besteht, die Sendung zu bewegen, ist eine Vereinbarung mit dem Unternehmer dahin gehend zu treffen, dass dieser den Inspektor darüber informiert, wann das Silo geleert wird, damit eine Probenahme erfolgen kann, wenn sich das Futtermittel im Fluss befindet.
8.4.2.2. Silos ohne Zugang von oben (geschlossene Silos) mit einer Größe unter 100 Tonnen
Im Rahmen des Probenahmeverfahrens ist eine Menge von 50 bis 100 kg in einen Behälter abzufüllen und anschließend zu beproben. Die Größe der Sammelprobe entspricht der gesamten Partie, und die Anzahl der Einzelproben muss im Verhältnis zu der Menge stehen, die zur Probenahme aus dem Silo in einen Behälter abgefüllt wird. Wird ein Teil einer Futtermittelpartie derselben Gruppe oder Bezeichnung beprobt und erfüllt diese Teilpartie nachweislich nicht die EU-Anforderungen, so muss davon ausgegangen werden, dass das Ergebnis der Beprobung für die gesamte Futtermittelpartie gilt, es sei denn, eine eingehende Bewertung erbringt keinen Nachweis darüber, dass die restliche Partie den EU-Anforderungen nicht genügt.
8.5. Beprobung loser Futtermittel in großen geschlossenen Containern
Solche Partien können häufig erst nach dem Entladen beprobt werden. In bestimmten Fällen ist das Entladen am Einfuhrort oder am Kontrollpunkt nicht möglich, weshalb die Probenahme erfolgen sollte, wenn die betreffenden Container entladen sind.
9. Anweisungen für die Entnahme, Vorbereitung und Verpackung der Proben
9.1. Allgemeines
Die Proben müssen so schnell wie möglich entnommen und vorbereitet werden, wobei die nötigen Vorkehrungen zu treffen sind, um sicherzustellen, dass das Erzeugnis weder verändert noch verunreinigt wird. Die für die Probenahme bestimmten Geräte, Flächen und Behälter müssen sauber und trocken sein.
9.2. Einzelproben
Die Einzelproben sind nach dem Zufallsprinzip und unter gleichmäßiger Verteilung aus der gesamten Teilpartie zu entnehmen. Ihre Größe muss ungefähr gleich sein.
Die Größe der Einzelprobe muss mindestens 100 g bzw. 25 g bei Raufutter/Grünfutter mit geringer spezifischer Dichte betragen.
Sind nach dem Probenahmeverfahren gemäß Nummer 8 weniger als 40 Einzelproben zu entnehmen, muss die Größe der Einzelprobe im Verhältnis zur erforderlichen Größe der Sammelprobe festgelegt werden (siehe Nummer 6).
Bei der Beprobung kleiner Partien verpackter Futtermittel, bei der entsprechend den quantitativen Anforderungen eine begrenzte Anzahl von Einzelproben zu entnehmen ist, umfasst eine Einzelprobe den Inhalt einer Originaleinheit, der 1 kg bzw. 1 Liter nicht überschreitet.
Bei der Beprobung verpackter Futtermittel, die aus kleinen Einheiten bestehen (z.B. < 250 g) ist die Größe der Einzelprobe von der Größe der Einheit abhängig.
Bei Proben aus dem Fernabsatz hängt der Umfang der Einzelprobe von der Größe der Einheit ab und kann im Einzelfall auch weniger als 100 g oder 100 ml enthalten.
9.2.1. Lose Futtermittel
Die Probenahme kann gegebenenfalls auch bei einer Teilpartie erfolgen, die sich in Bewegung (Einladen oder Entladen) befindet.
9.2.2. Verpackte Futtermittel
Nach Auswahl der erforderlichen Anzahl der zu beprobenden Einheiten gemäß Nummer 5 wird aus jeder dieser Einheiten ein Teil des Inhalts mit einem Probenahmestab oder einer Schaufel entnommen. Gegebenenfalls sind die Proben zu entnehmen, nachdem die Einheiten getrennt entleert worden sind.
9.2.3. Homogene oder homogenisierbare flüssige oder halbflüssige Futtermittel
Nach Auswahl der erforderlichen Anzahl der zu beprobenden Einheiten gemäß Nummer 5 wird der Inhalt falls nötig homogenisiert und aus jeder Einheit eine Menge entnommen.
Die Einzelproben können auch beim Ablassen des Inhalts entnommen werden.
9.2.4. Nicht homogenisierbare flüssige oder halbflüssige Futtermittel
Nach Auswahl der erforderlichen Anzahl der zu beprobenden Einheiten gemäß Nummer 5 werden in unterschiedlicher Höhe Proben entnommen.
Die Probenahme kann auch beim Ablassen des Inhalts erfolgen, wobei jedoch die ersten Fraktionen zu verwerfen sind.
In beiden Fällen muss das Gesamtvolumen mindestens 10 l betragen.
9.2.5. Futterblöcke und Lecksteine
Nach Auswahl der erforderlichen Anzahl der zu beprobenden Blöcke oder Steine gemäß Nummer 5 kann jedem Block oder Stein ein Teil entnommen werden. Besteht die Vermutung, dass es sich um einen nicht homogenen Block bzw. Stein handelt, so kann der ganze Block bzw. Stein als Probe genommen werden.
Bei Futterblöcken oder Lecksteinen mit einem Gewicht von jeweils maximal 1 kg gilt der Inhalt eines Futterblocks oder Lecksteins als Einzelprobe.
9.3. Vorbereitung der Sammelproben
Die Einzelproben werden gemischt und zu einer einzigen Sammelprobe zusammengestellt.
9.4. Vorbereitung der Endproben
Das Material in der Sammelprobe ist sorgfältig zu mischen. 2
Jede Probe wird in einen geeigneten Container/Behälter gefüllt. Es sind alle notwendigen Vorkehrungen zu treffen, damit jede Veränderung der Zusammensetzung bzw. jede Verunreinigung oder Verfälschung der Probe während des Transports oder der Lagerung vermieden wird.
9.4.1. Stoffe mit gleichmäßiger Verteilung
Bei der Untersuchung auf Bestandteile oder Stoffe, die im Futtermittel gleichmäßig verteilt sind, kann die Sammelprobe repräsentativ auf mindestens 2,0 kg bzw. 2,0 l reduziert werden (reduzierte Probe) 3, vorzugsweise mithilfe eines mechanischen oder automatischen Probenteilers. Bei der Beprobung von Hülsenfrüchten, Getreidekörnern und Schalenfrüchten auf Pflanzenschutzmittelrückstände beträgt die Mindestgröße der reduzierten Probe 3 kg. Falls aufgrund der Art des Futtermittels die Verwendung eines Probenteilers nicht möglich oder ein Probenteiler nicht verfügbar ist, kann die Probe nach dem Vierteilungsverfahren reduziert werden.
Dann werden aus der Sammelprobe oder den reduzierten Proben ungefähr gleich große Endproben (für Kontroll-, Verteidigungs- und etwaige Referenzzwecke) entsprechend den quantitativen Anforderungen in Nummer 7 genommen.
9.4.2. Stoffe mit ungleichmäßiger Verteilung
Bei der Untersuchung auf Bestandteile, einschließlich genetisch veränderter Ausgangserzeugnisse, oder auf Stoffe, die ungleichmäßig im Futtermittel verteilt sein können, muss die Sammelprobe folgende Anforderungen erfüllen:
Dann werden aus den reduzierten Proben ungefähr gleich große Endproben entsprechend den quantitativen Anforderungen in Nummer 7 genommen.
9.5. Verpackung der Proben
Die Behälter oder Packungen sind so zu verplomben und zu kennzeichnen, dass sie nicht ohne Beschädigung der Plombe geöffnet werden können. Hierbei muss die gesamte Kennzeichnung von der Plombe erfasst werden. Alternativ kann die Probe in einen Behälter verfüllt werden, der so verschließbar ist, dass er nicht geöffnet werden kann, ohne das Gefäß bzw. den Behälter dabei irreversibel zu beschädigen. Eine mehrmalige Verwendung des Gefäßes bzw. Behälters ist zu vermeiden.
9.6. Versendung der Proben an das Labor
Die Probe ist - zusammen mit den untersuchungsrelevanten Angaben - so schnell wie möglich an das benannte Analyselabor zu versenden.
10. Probenahmeprotokoll
Für jede Probe ist ein Probenahmeprotokoll zu erstellen, aus dem die Identität und der Umfang der Teilpartie eindeutig hervorgehen.
Im Protokoll wird außerdem jede Abweichung von den in dieser Verordnung festgelegten Probenahmeverfahren vermerkt.
Das Protokoll wird dem amtlichen Kontrolllabor sowie dem Futtermittelunternehmer und/oder dem vom Futtermittelunternehmer benannten Labor zur Verfügung gestellt.
11. Probe aus dem Fernabsatz
Aus der Sammelprobe werden dann die entsprechenden Endproben (für Durchsetzungs-, Verteidigungs- und etwaige Referenzzwecke) nach Möglichkeit entsprechend den Grundsätzen nach Nummer 9.4 entnommen, und aus dem Probenahmeprotokoll geht hervor, dass es sich bei der Probe um eine Probe aus dem Fernabsatz handelt. Die zuständige Behörde informiert danach den Futtermittelunternehmer unverzüglich über die Probenahme. Dem Futtermittelunternehmer wird ferner mitgeteilt, dass eine Probe nach Möglichkeit von der zuständigen Behörde für ihn an einem bestimmten Ort zu Verteidigungszwecken zur Verfügung gehalten oder an den Futtermittelunternehmer selbst oder an das vom Futtermittelunternehmer gemäß den geltenden nationalen Vorschriften benannte Labor geschickt wird.
Wird die Probe direkt an das amtliche Labor geschickt, so muss die Endprobe im Labor von dazu ermächtigten Personen oder im Beisein von hierzu ermächtigten Personen vorbereitet und versiegelt werden. Das Probenahmeprotokoll der Probe aus dem Fernabsatz ist unmittelbar nach der Erstellung der Endproben an die zuständige Behörde zu schicken, die den Futtermittelunternehmer über die Probenahme informiert.
Die Menge, die der Futtermittelunternehmer an die zuständige Behörde ausgeliefert hat, gilt als ein Teil einer Partie Futtermittel der gleichen Gruppe oder Bezeichnung. Erfüllt dieser Teil einer Partie nachweislich nicht die EU-Anforderungen, so ist gemäß Artikel 15 der Verordnung (EG) Nr. 178/2002 des Europäischen Parlaments und des Rates 5 auch im Fall einer Probe aus dem Fernabsatz davon auszugehen, dass sämtliche Futtermittel in dieser Partie gleichermaßen betroffen sind, es sei denn, bei einer eingehenden Prüfung (gegebenenfalls bei einer Kontrolle vor Ort) wird kein Nachweis dafür gefunden, dass der Rest der Partie die EU-Anforderungen nicht erfüllt."
2) Klumpen sind zu zerdrücken (sie werden gegebenenfalls vom übrigen Material getrennt und der Probe anschließend wieder untergemischt).
3) Außer bei Raufutter/Grünfutter mit geringer spezifischer Dichte.
4) Außer bei Raufutter/Grünfutter mit geringer spezifischer Dichte.
5) Verordnung (EG) Nr. 178/2002 des Europäischen Parlaments und des Rates vom 28. Januar 2002 zur Festlegung der allgemeinen Grundsätze und Anforderungen des Lebensmittelrechts, zur Errichtung der Europäischen Behörde für Lebensmittelsicherheit und zur Festlegung von Verfahren zur Lebensmittelsicherheit (ABl. L 31 vom 01.02.2002 S. 1).
| Anhang II |
"Anhang II
Allgemeine Bestimmungen hinsichtlich der Methoden zur Analyse von Futtermitteln
A. Vorbereitung der Proben zur Analyse
1. Zweck
Die in diesem Anhang beschriebenen Verfahren betreffen die Vorbereitung der zur Analyse bestimmten Proben, die nach der Probenahme gemäß den Bestimmungen in Anhang I an die Kontrolllabors versandt wurden.
Die Vorbereitung der Laborproben muss so erfolgen, dass die in den Analysemethoden vorgesehenen Einwaagen homogen und repräsentativ für die Endproben sind.
Über die in diesem Anhang beschriebenen Verfahren hinaus ist auch der Leitfaden für die Probenvorbereitung gemäß EN ISO 6498 zu befolgen.
2. Vorsichtsmaßnahmen
Die Wahl des Verfahrens für die Probenvorbereitung hängt von der Art der anzuwendenden Analysemethode und den zu untersuchenden Bestandteilen oder Stoffen ab. Daher ist es äußerst wichtig, dass das angewandte Probenvorbereitungsverfahren für die jeweilige Analysemethode und für die zu untersuchenden Bestandteile oder Stoffe geeignet ist.
Alle notwendigen Schritte sind so durchzuführen, dass eine Verunreinigung der Probe und eine Veränderung ihrer Zusammensetzung weitestmöglich vermieden werden.
Das Zermahlen, Mischen und Sieben muss unverzüglich erfolgen, wobei die Probe möglichst wenig Luft und Licht ausgesetzt werden darf. Die Verwendung von Mühlen oder Zerkleinerungsgeräten, die zu einer merklichen Erwärmung der Probe führen könnten, ist nicht zulässig.
Für besonders hitzeempfindliche Futtermittel wird manuelles Mahlen empfohlen. Es ist außerdem darauf zu achten, dass die verwendeten Geräte keine Kontaminationsquelle bilden.
Die Homogenisierung der Probe durch Aufschlämmen mittels Hochschermischen mit Wasser ergibt erwiesenermaßen in bestimmten Fällen homogenere Teilproben als eine trockene Homogenisierung/Trockenmahlen, insbesondere bei heterogen verteilten chemischen Stoffen. Allerdings kann auch eine Homogenisierung durch ausreichendes Trockenmahlen homogene Teilproben ergeben.
In bestimmten Fällen, z.B. bei der Bestimmung von Mutterkorn, schädlichen botanischen Verunreinigungen usw., darf die Homogenisierung der Probe nicht durch Mahlen, sondern durch ausreichendes Durchmischen der Probe erfolgen.
Kann die Probe nicht ohne eine signifikante Veränderung ihres Feuchtigkeitsgehalts vorbereitet werden, so ist dieser vor und nach der Vorbereitung gemäß der in Anhang III Teil A festgelegten Methode zu bestimmen.
3. Verfahren
3.1. Allgemeines Verfahren
Das Testaliquot ist der homogenisierten Endprobe zu entnehmen. Das Kegeln und das Vierteilungsverfahren werden nicht empfohlen, da dies mit einer hohen Teilungsfehlerquote bei den Testaliquoten einhergehen kann.
3.1.1. Futtermittel, die direkt gemahlen werden können
3.1.2. Futtermittel, die nach Trocknung gemahlen werden können
3.1.3. Flüssige oder halbflüssige Futtermittel
3.1.4. Andere Futtermittel
3.2. Besonderes Verfahren bei Sichtprüfungen oder mikroskopischen Untersuchungen oder im Fall einer Homogenisierung der vollständigen Sammelprobe
4. Lagerung der Proben
Die Proben müssen bei einer Temperatur gelagert werden, die ihre Zusammensetzung nicht beeinflusst. Proben, die zur Analyse von Vitaminen oder besonders lichtempfindlichen Stoffen bestimmt sind, sind so zu lagern, dass die Probe nicht durch Licht beeinträchtigt wird.
B. Bestimmungen über in Analyseverfahren verwendete Reagenzien und Geräte
C. Anwendung von Analysemethoden und Formulierung der Ergebnisse
1. Extraktionsverfahren
Einige Methoden geben ein spezifisches Extraktionsverfahren vor. Generell können andere Extraktionsverfahren als das in der Methode genannte Verfahren angewandt werden, und zwar unter der Bedingung, dass das angewandte Extraktionsverfahren für die analysierte Matrix eine vergleichbare Extraktionseffizienz aufweist wie das in der Methode genannte Verfahren.
2. Clean-up-Verfahren
Einige Methoden geben ein spezifisches Clean-up-Verfahren vor. Generell können andere Clean-up-Verfahren als das in der Methode genannte Verfahren angewandt werden, und zwar unter der Bedingung, dass das angewandte Clean-up-Verfahren für die analysierte Matrix zu vergleichbaren Analyseergebnissen führt wie das in der Methode genannte Verfahren.
3. Anzahl der Bestimmungen
Bei der Analyse auf unerwünschte Stoffe sind - sofern das Ergebnis der ersten Bestimmung deutlich (> 50 %) unter dem zu kontrollierenden Sollwert liegt - keine weiteren Bestimmungen erforderlich, vorausgesetzt, dass die geeigneten Qualitätsverfahren angewandt werden. In anderen Fällen ist eine Zweitanalyse (Zweitbestimmung) erforderlich, um eine interne Kreuzkontamination oder ein versehentliches Vertauschen der Proben auszuschließen. Für die weitere Bewertung wird der Mittelwert der beiden Bestimmungen herangezogen.
Bei der Kontrolle des Mindest- oder Höchstgehalts an Futtermittelzusatzstoffen sind - sofern das Ergebnis der Erstbestimmung über dem Mindestgehalt bzw. unter dem Höchstgehalt liegt - keine weiteren Bestimmungen erforderlich, vorausgesetzt, dass die geeigneten Qualitätsverfahren angewandt werden. In anderen Fällen ist eine Zweitanalyse (Zweitbestimmung) erforderlich, um eine interne Kreuzkontamination oder ein versehentliches Vertauschen der Proben auszuschließen. Für die weitere Bewertung wird der Mittelwert der beiden Bestimmungen herangezogen.
Bei der Kontrolle des angegebenen Gehalts an einem Stoff oder einer Zutat sind - sofern das Ergebnis der Erstbestimmung den angegebenen Gehalt bestätigt, d. h., wenn das Analyseergebnis innerhalb des akzeptablen Toleranzbereichs für den angegebenen Gehalt liegt - keine weiteren Bestimmungen erforderlich, vorausgesetzt, dass die geeigneten Qualitätsverfahren angewandt werden. In anderen Fällen ist eine Zweitanalyse (Zweitbestimmung) erforderlich, um eine interne Kreuzkontamination oder ein versehentliches Vertauschen der Proben auszuschließen. Der Mittelwert der beiden Bestimmungen wird für die weitere Bewertung herangezogen (das durchschnittliche Analyseergebnis liegt innerhalb des akzeptablen Toleranzbereichs für den angegebenen Gehalt oder nicht).
In einigen Fällen ist der akzeptable Toleranzbereich in Rechtsvorschriften definiert, beispielsweise in der Verordnung (EG) Nr. 767/2009 und der Verordnung (EU) 2019/4 des Europäischen Parlaments und des Rates 1.
4. Berichterstattung über die angewandte Analysemethode
Im Analysebericht ist anzugeben, welche Analysemethode angewandt wurde.
5. Bericht über die Analyseergebnisse
Das Ergebnis ist gemäß den Anweisungen in der Analysemethode mit einer angemessenen Zahl an signifikanten Ziffern anzugeben und, falls nötig, auf den Feuchtigkeitsgehalt der Endprobe vor deren Vorbereitung umzurechnen.
Die meisten in den EU-Rechtsvorschriften für Futtermittel definierten Gehalte (z.B. Höchstgehalt, Mindestgehalt) wurden in Bezug auf Futtermittel mit einem Feuchtigkeitsgehalt von 12 % festgelegt. Um das in der Probe gemessene Analyseergebnis gemäß dem vorgeschriebenen Gehalt bewerten zu können, muss das Analyseergebnis in diesen Fällen zunächst durch den Trockenmassegehalt der Probe (in %), multipliziert mit 88, dividiert werden, wie in der folgenden Formel angegeben:
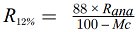
Dabei gilt:
| Mc | : | Feuchtigkeitsgehalt der Probe (in %). 100 - Mc entspricht somit dem Trockenmassegehalt der Probe (in %). |
| Rana | : | in der Probe gemessenes Analyseergebnis |
| R12 % | : | Ergebnis bei einem Futtermittel mit einem Feuchtigkeitsgehalt von 12 %; anhand des vorgeschriebenen Gehalts zu bewerten. |
Wenn darüber hinaus die folgenden Bedingungen erfüllt sind:
Wird das Analyseergebnis um den Feuchtigkeitsgehalt korrigiert, muss die entsprechende Messunsicherheit im gleichen Verfahren ebenfalls korrigiert werden.
Bei der Bestimmung von Mutterkorn oder schädlichen botanischen Verunreinigungen durch Sichtprüfung oder mikroskopischen Untersuchung ist eine Berichtigung um den Feuchtigkeitsgehalt nicht erforderlich.
6. Analysemessunsicherheit und Wiederfindungsrate bei der Analyse auf unerwünschte Stoffe
Hinsichtlich unerwünschter Stoffe im Sinne der Richtlinie 2002/32/EG erfüllt ein zur Verfütterung bestimmtes Erzeugnis die Bestimmung bezüglich des festgelegten Höchstgehalts nicht, wenn das aus einem Mittelwert aus zwei unabhängigen Bestimmungen bestehende Analyseergebnis, bezogen auf ein Futtermittel mit einem Feuchtigkeitsgehalt von 12 %, unter Berücksichtigung der erweiterten Analysemessunsicherheit bei Anwendung eines Erweiterungsfaktors von 2, der zu einem Konfidenzniveau von ca. 95 % führt, und bei Berichtigung um die Wiederfindungsrate den Höchstgehalt überschreitet. Dies bedeutet, dass zur Beurteilung der Einhaltung der Höchstgehalte die gemessene Konzentration - nach Berichtigung um die Wiederfindungsrate und nach Abzug der erweiterten Analysemessunsicherheit - herangezogen wird. Dieses Verfahren wird nur dann angewandt, wenn die Analysemethode die Schätzung der erweiterten Analysemessunsicherheit und die Berichtigung um die Wiederfindungsrate ermöglicht (z.B. nicht erforderlich bei Sichtprüfung/mikroskopischer Untersuchung).
Überschreitet das Analyseergebnis der zu Verteidigungszwecken entnommenen Probe den Höchstgehalt (ohne Berücksichtigung der erweiterten Analysemessunsicherheit), bestätigt dies die anhand der Kontrollprobe festgestellte Nichteinhaltung, sofern keine spezifischen nationalen Vorschriften diesbezüglich bestehen.
Das Analyseergebnis ist wie folgt festzuhalten (soweit die angewandte Analysemethode die Schätzung der erweiterten Analysemessunsicherheit ermöglicht):
Liegt jedoch das Analyseergebnis deutlich (> 50 %) unter dem zu kontrollierenden Sollwert - und unter der Bedingung, dass die geeigneten Qualitätsverfahren angewandt werden und die Analyse lediglich dem Zweck der Überprüfung der Einhaltung der Rechtsvorschriften dient -, können die Angabe der Wiederfindungsrate und der erweiterten Analysemessunsicherheit entfallen (etwa wenn kein Sollwert oder vorgeschriebener Gehalt besteht), sofern die Messunsicherheit nicht für die Interpretation erforderlich ist.
7. Analysemessunsicherheit und Wiederfindungsrate bei der Analyse des Gehalts an Futtermittelzusatzstoffen
Bei der Überprüfung der Einhaltung des zulässigen Mindest- und Höchstgehalts an Futtermittelzusatzstoffen gelten der festgelegte Mindest- und Höchstgehalt eines Futtermittelzusatzstoffs als nicht eingehalten, wenn das aus einem Mittelwert aus zwei unabhängigen Bestimmungen bestehende Analyseergebnis bezogen auf ein Futtermittel mit einem Feuchtigkeitsgehalt von 12 %:
Überschreitet das Analyseergebnis der zu Verteidigungszwecken entnommenen Probe den Höchstgehalt (ohne Berücksichtigung der erweiterten Analysemessunsicherheit), bestätigt dies die anhand der Kontrollprobe festgestellte Nichteinhaltung, sofern keine spezifischen nationalen Vorschriften diesbezüglich bestehen.
Das Analyseergebnis ist wie folgt festzuhalten (soweit die angewandte Analysemethode die Schätzung der erweiterten Analysemessunsicherheit ermöglicht):
2) Das Konfidenzniveau von 95 % kann durch Verwendung eines anderen Faktors, wie dem t-Faktor, erreicht werden.
3) Das Konfidenzniveau von 95 % kann durch Verwendung eines anderen Faktors, wie dem t-Faktor, erreicht werden.
| Anhang III |
"Anhang III
Analysemethoden zur Untersuchung der Zusammensetzung von Futtermittel-Ausgangserzeugnissen und Mischfuttermitteln
A. Bestimmung des Feuchtigkeitsgehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Feuchtigkeitsgehalt von Futtermitteln bestimmen. Bei Futtermitteln, die flüchtige Stoffe wie z.B. organische Säuren enthalten, ist zu beachten, dass zusammen mit dem Feuchtigkeitsgehalt auch eine bedeutende Anzahl an flüchtigen Stoffen bestimmt wird.
Sie betrifft nicht die Untersuchung von Milcherzeugnissen als Futtermittel-Ausgangserzeugnisse und von Mischfuttermitteln, die überwiegend aus Milcherzeugnissen bestehen, die Untersuchung von tierischen und pflanzlichen Fetten und Ölen oder die Untersuchung von Ölsaaten und Ölfrüchten.
Die Bestimmung des Feuchtigkeitsgehalts bei Ölsaaten muss nach dem Verfahren gemäß EN ISO 665 - Bestimmung des Feuchtegehaltes und des Gehaltes an flüchtigen Bestandteilen - erfolgen, wobei Sojabohnen vor der Bestimmung des Feuchtigkeitsgehalts zu zermahlen sind.
2. Prinzip
Die Probe wird unter definierten Bedingungen getrocknet, die von der Art des Futtermittels abhängen. Der Gewichtsverlust wird durch Wiegen bestimmt. Bei festen Futtermitteln mit einem hohen Feuchtigkeitsgehalt ist eine zusätzliche Vortrocknung erforderlich.
3. Geräte
3.1. Zerkleinerungsgerät aus einem Material, das keine Feuchtigkeit absorbiert, leicht zu reinigen ist, eine schnelle und gleichmäßige Zerkleinerung ermöglicht, ohne eine merkliche Erwärmung hervorzurufen, das so weit wie möglich den Kontakt mit der Außenluft verhindert und den unter Nummer 4.1.1 und 4.1.2 gestellten Anforderungen entspricht (z.B. Mikroschlagkreuzmühlen, Mikrozerkleinerer mit Wasserkühlung, zerlegbare Kegelmühlen, langsam laufende Kegelmühlen oder Zahnscheibenmühlen).
3.2. Analysenwaage, Genauigkeit 1 mg.
3.3. Trockene Gefäße aus korrosionsbeständigem Metall oder Glas, mit luftdicht schließenden Deckeln; die Nutzfläche muss eine Verteilung der Analysenprobe von ca. 0,3 g/cm2 ermöglichen.
3.4. Elektrisch beheizter, temperaturgeregelter Trockenschrank (± 2 °C), der eine schnelle Regelung der Temperatur gewährleistet und eine gute Lüftung besitzt 1.
3.5. Elektrisch beheizter regulierbarer Vakuumtrockenschrank mit einer Ölpumpe, der entweder mit einer Vorrichtung für die Zufuhr warmer und getrockneter Luft oder mit einem Trocknungsmittel (z.B. Calciumoxid) ausgestattet ist.
3.6. Exsikkator mit dicker, perforierter Platte aus Metall oder Porzellan, der ein wirksames Trocknungsmittel enthält.
4. Verfahren
| Anmerkung: | Die Verfahren, die in diesem Abschnitt beschrieben werden, müssen unverzüglich nach dem Öffnen der Packungen, die die Proben enthalten, durchgeführt werden. Die Analysen sind mindestens doppelt auszuführen. |
4.1. Vorbereitung
4.1.1. Futtermittel, außer den unter Nummer 4.1.2 und 4.1.3 genannten
Mindestens 50 g der Probe werden entnommen und erforderlichenfalls unter Vermeidung von Feuchtigkeitsänderungen entsprechend zerkleinert oder geteilt (siehe Nummer 6).
4.1.2. Getreide und Grütze
Mindestens 50 g der Probe werden entnommen Diese Menge wird so zermahlen, dass zumindest 50 % der Teilchen durch ein Sieb mit einer Maschenweite von 0,5 mm passiert werden können und dass beim Passieren durch ein Rundlochsieb mit einem Lochdurchmesser von 1 mm ein Rückstand von höchstens 10 % verbleibt.
4.1.3. Flüssige oder breiige Futtermittel; Futtermittel, die überwiegend aus Ölen und Fetten bestehen
Etwa 25 g der Probe, auf 10 mg genau gewogen, werden entnommen, mit einer entsprechenden, auf 10 mg genau gewogenen Menge wasserfreiem Sand vermischt, bis ein homogenes Produkt entsteht.
4.2. Trocknung
Ein Gefäß (Nummer 3.3) wird mit seinem Deckel im auf 103 °C eingestellten Trockenschrank 30 min ± 1 min lang getrocknet. Es wird aus dem Trockenschrank genommen und im Exsikkator (Nummer 3.6) auf Umgebungstemperatur abkühlen gelassen.
4.2.1. Futtermittel, außer den unter Nummer 4.2.2 und 4.2.3 genannten
Das Gefäß wird mit seinem Deckel auf 1 mg genau gewogen. Etwa 5 g der Probe werden auf 1 mg genau in das tarierte Gefäß eingewogen und gleichmäßig verteilt. Das Gefäß wird ohne Deckel in den auf 103 °C vorgeheizten Trockenschrank gestellt. Damit die Temperatur des Trockenschranks nicht zu stark abfällt, ist das Gefäß möglichst rasch hineinzustellen. Es wird 4 h lang getrocknet, wobei die Trocknungszeit von dem Zeitpunkt an gerechnet wird, an dem die Temperatur im Trockenschrank erneut 103 °C erreicht hat. Nach Öffnen des Trockenschranks wird das Gefäß sofort wieder mit dem Deckel verschlossen, aus dem Schrank genommen, zum Abkühlen 30 bis 45 min lang in den Exsikkator (Nummer 3.6) gestellt und anschließend auf 1 mg genau gewogen.
Bei Futtermitteln, die überwiegend (> 50 %) aus Ölen und Fetten tierischen und pflanzlichen Ursprungs bestehen, wird eine zusätzliche Trocknung von 30 min im Trockenschrank bei 103 °C vorgenommen. Der Unterschied zwischen den beiden Wägeergebnissen darf höchstens 0,1 % Feuchtigkeit betragen.
4.2.2. Getreide, Mehl, Grütze und Grieß
Das Gefäß wird mit seinem Deckel auf 0,5 mg genau gewogen. Etwa 5 g der zerkleinerten Probe werden auf 1 mg genau in das tarierte Gefäß eingewogen und gleichmäßig verteilt. Das Gefäß wird ohne Deckel in den auf 130 °C vorgeheizten Trockenschrank gestellt. Damit die Temperatur des Trockenschranks nicht zu stark abfällt, ist das Gefäß möglichst rasch hineinzustellen. Es wird 2 h lang getrocknet, wobei die Trocknungszeit von dem Zeitpunkt an gerechnet wird, an dem die Temperatur im Trockenschrank erneut 130 °C erreicht hat. Nach Öffnen des Trockenschranks wird das Gefäß sofort wieder mit dem Deckel verschlossen, aus dem Schrank genommen, zum Abkühlen 30 bis 45 min lang in den Exsikkator (Nummer 3.6) gestellt und anschließend auf 1 mg genau gewogen.
4.2.3. Mischfuttermittel mit einem Saccharose- oder Lactosegehalt von mehr als 4 %: Futtermittel-Ausgangserzeugnisse wie z.B. Johannisbrotschrot, hydrolysierte Getreideerzeugnisse, Malzkeime, Zuckerrübenschnitzel, Fisch- und Zuckerpresssäfte
Das Gefäß wird mit seinem Deckel auf 0,5 mg genau gewogen. Etwa 5 g der Probe werden auf 1 mg genau in das tarierte Gefäß eingewogen und gleichmäßig verteilt. Das Gefäß wird ohne Deckel in den auf 80 bis 85 °C vorgeheizten Vakuumtrockenschrank (Nummer 3.5) gestellt. Damit die Temperatur des Trockenschranks nicht zu stark abfällt, ist das Gefäß möglichst rasch hineinzustellen.
Der Druck wird auf 100 Torr eingestellt. Die Probe wird 4 h lang bei diesem Druck entweder unter Zufuhr von heißer trockener Luft oder mittels eines Trocknungsmittels (etwa 300 g für 20 Proben) getrocknet. Im letzteren Fall wird beim Erreichen des vorgeschriebenen Drucks die Verbindung zur Vakuumpumpe unterbrochen. Die Trocknungszeit wird von dem Zeitpunkt an gerechnet, an dem die Temperatur im Trockenschrank erneut 80 bis 85 °C erreicht hat. Nach Ablauf der Trocknungszeit wird der Trockenschrank vorsichtig wieder auf atmosphärischen Druck gebracht. Nach Öffnen des Trockenschranks wird das Gefäß sofort wieder mit dem Deckel verschlossen, aus dem Schrank genommen, zum Abkühlen 30 bis 45 min lang in den Exsikkator (Nummer 3.6) gestellt und anschließend auf 1 mg genau gewogen. Es wird im Vakuumtrockenschrank weitere 30 min bei 80 bis 85 °C getrocknet und erneut gewogen. Der Unterschied zwischen den beiden Wägeergebnissen darf höchstens 0,1 % Feuchtigkeit betragen.
4.3. Vortrocknung (Teiltrocknung)
"Nasse" Futtermittel mit einem Massenanteil von weniger als 85 % Trockenmasse (z.B. Grünfutter, Gesamtmischrationen, (nicht)flüssige Futtermittel) müssen vor dem Feinzermahlen teilgetrocknet werden, um ihre stabilen Stoffe untersuchen zu können; bei instabilen Stoffen ist keine Teiltrocknung möglich.
Die Teiltrocknung kann entweder mithilfe eines Trockenschranks mit Luftumwälzung oder eines Mikrowellengeräts oder durch Gefriertrocknen erfolgen. Außer beim Teiltrocknen durch Gefriertrocknen geht es darum, das Futtermittel zu trocknen und gleichzeitig die Probentemperatur unter 60 °C zu halten, damit die chemische Zusammensetzung nur minimal beeinträchtigt wird. Eine Trocknung bei Temperaturen über 60 °C führt zu chemischen Veränderungen im Futter (z.B. Proteinabbau). Das getrocknete Futtermittel wird bei Raumtemperatur 15 min lang äquilibriert, anschließend wird die teilgetrocknete Masse gemessen, um eine potenzielle Veränderung des Feuchtigkeitsgehalts, die während des Zermahlens und der Lagerung auftreten kann, so gering wie möglich zu halten. Beim Trocknen bei Temperaturen unter 60 °C wird dem Futtermittel nicht das gesamte Wasser entzogen; daher lässt sich mithilfe der (ersten) Teiltrocknung nicht die Gesamttrockenmasse des Futtermittels bestimmen. Nach dem Trocknen wird die Teilprobe zermahlen und im Rahmen der Bestimmung der anderen chemischen Bestandteile auf die (endgültige) Trockenmasse der teilgetrockneten Probe untersucht (3-15 % Restfeuchte).
Daher wird zur Bestimmung der Trockenmasse ein zweistufiges Verfahren empfohlen. Zunächst wird der Gehalt der teilgetrockneten Masse bestimmt (bei weniger als 85 % Trockenmasse), dann wird der verbleibende Trockenmassegehalt anhand einer zermahlenen Analysenprobe bestimmt und die teilgetrocknete Masse wird mit der verbleibenden Trockenmasse multipliziert, um den Gesamttrockenmassegehalt zu bestimmen.
5. Berechnung der Ergebnisse
Der Feuchtigkeitsgehalt (X) der Probe als Prozentsatz wird nach folgenden Formeln berechnet:
5.1. Trocknung ohne Vortrocknung
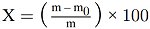
wobei:
| m = | Anfangsgewicht der Analysenprobe in g, |
| m0 = | Gewicht der trockenen Analysenprobe in g. |
5.2. Trocknung mit Vortrocknung 2
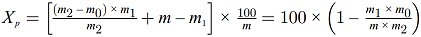
wobei:
| m = | Anfangsgewicht der Analysenprobe in g, |
| m1 = | Gewicht der Analysenprobe nach der Vortrocknung in g, |
| m2 = | Gewicht der Analysenprobe nach der Zerkleinerung oder dem Zermahlen in g, |
| m0 = | Gewicht der trockenen Analysenprobe in g. |
5.3. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 0,2 % Feuchtigkeit (absolut) nicht überschreiten, außer bei Nassfutter für Heimtiere und Kauspielzeug für Hunde, wo die Differenz 0,5 % Feuchtigkeit (absolut) nicht überschreiten darf.
6. Bemerkung
Wenn eine Zerkleinerung sich als notwendig erweist und dabei mit einer Änderung des Feuchtigkeitsgehalts des Materials gerechnet werden muss, so sind die Analyseergebnisse, die die Bestandteile des Futtermittels betreffen, auf den Feuchtigkeitsgehalt der Originalprobe umzurechnen.
B. Bestimmung des Feuchtigkeitsgehalts in tierischen und pflanzlichen Fetten und Ölen
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an Wasser und flüchtigen Stoffen in tierischen und pflanzlichen Fetten und Ölen bestimmen.
2. Prinzip
Die Probe wird bei 103 °C getrocknet, bis kein Gewichtsverlust mehr eintritt (der Gewichtsverlust zwischen 2 aufeinanderfolgenden Wägungen darf 1 mg nicht überschreiten). Der Gewichtsverlust wird durch Wiegen bestimmt.
3. Geräte
3.1. Schale mit flachem Boden, aus korrosionsbeständigem Material, Durchmesser: 8 bis 9 cm, Höhe ca. 3 cm.
3.2. Thermometer mit verstärkter Kugel und Ausdehnungsraum am oberen Ende, von ca. 80 bis mindestens 110 °C graduiert, Länge ca. 10 cm.
3.3. Sandbad oder elektrische Heizplatte.
3.4. Exsikkator, der ein wirksames Trocknungsmittel enthält.
3.5. Analysenwaage.
4. Verfahren
Etwa 20 g der homogenisierten Probe werden auf 1 mg genau in die trockene, gewogene Schale (Nummer 3.1.) eingewogen, die das Thermometer (Nummer 3.2) enthält, und auf dem Sandbad oder der elektrischen Heizplatte (Nummer 3.3) unter ständigem Rühren mit dem Thermometer so erhitzt, dass in ca. 7 min eine Temperatur von 90 °C erreicht wird
Entsprechend der Häufigkeit, mit der Gasblasen vom Boden der Schale aufsteigen, wird die Heizintensität verringert. Die Temperatur darf 105 °C nicht überschreiten. Unter ständigem Abkratzen des Bodens der Schale wird weiter umgerührt, bis sich keine Blasen mehr bilden.
Um sicherzustellen, dass keine Feuchtigkeit mehr vorhanden ist, wird mehrmals auf 103 °C ± 2 °C erhitzt und zwischen aufeinanderfolgenden Erhitzungen jeweils auf 93 °C gekühlt. Anschließend wird bis zur Raumtemperatur im Exsikkator (Nummer 3.4) abkühlen gelassen und gewogen. Dieses Verfahren ist so oft zu wiederholen, bis der Gewichtsverlust zwischen 2 aufeinanderfolgenden Wägungen 2 mg nicht mehr überschreitet.
| Anmerkung: | Eine Gewichtserhöhung der Probe nach wiederholter Erwärmung zeigt eine Oxidation des Fettes an. In diesem Fall wird der Berechnung das Ergebnis der Wägung zugrunde gelegt, die unmittelbar vor dem Auftreten der Gewichtszunahme ausgeführt wurde. |
5. Berechnung der Ergebnisse
Der Feuchtigkeitsgehalt ( X) der Probe als Prozentsatz wird nach folgender Formel berechnet:
X = (m1- m2) × 100/m
wobei:
| m = | Probeneinwaage in g, |
| m1 = | Gewicht der Schale mit Inhalt in g vor dem Erhitzen, |
| m2 = | Gewicht der Schale mit Inhalt in g nach dem Erhitzen. |
Ergebnisse unter 0,05 % sollten mit der Bezeichnung "weniger als 0,05 %" angegeben werden.
Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 0,1 % Feuchtigkeit (absolut) nicht überschreiten.
C. Bestimmung des Stickstoffgehalts und Berechnung des Rohproteingehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Rohproteingehalt von Futtermitteln anhand des nach Kjeldahl bestimmten Stickstoffgehalts 3 bestimmen.
2. Prinzip
Die Probe wird durch Schwefelsäure in Anwesenheit eines Katalysators aufgeschlossen. Der saure Aufschluss wird durch eine Natriumhydroxidlösung alkalisiert. Das Ammoniak wird durch Destillation abgetrennt und in einer definierten Menge Schwefelsäure aufgefangen, deren Überschuss durch eine Standard-Natriumhydroxidlösung titriert wird.
Alternativ wird das freigesetzte Ammoniak in überschüssiger Borsäurelösung destilliert, gefolgt von einer Titration mit Salz- oder Schwefelsäurelösung.
3. Reagenzien
3.1. Kaliumsulfat.
3.2. Katalysator: Kupfer(II)-oxid, CuO, oder Kupfer(II)-sulfatpentahydrat, CuSO4 5H2O.
3.3. Zinkgranulat.
3.4. Schwefelsäure, ρ20 = 1,84 g/ml.
3.5. Schwefelsäure, volumetrische Standardlösung, c(H2SO4) = 0,25 mol/l.
3.6. Schwefelsäure, volumetrische Standardlösung, c(H2SO4) = 0,10 mol/l.
3.7. Schwefelsäure, volumetrische Standardlösung, c(H2SO4) = 0,05 mol/l.
3.8. Methylrot-Indikator: 300 mg Methylrot werden in 100 ml Ethanol (σ = 95 bis 96 %) gelöst.
3.9. Natriumhydroxidlösung (Verwendung technischer Qualität möglich), β = 40 g/100 ml (40 %).
3.10. Natriumhydroxid, volumetrische Standardlösung, c(NaOH) = 0,25 mol/l.
3.11. Natriumhydroxid, volumetrische Standardlösung, c(NaOH) = 0,10 mol/l.
3.12. Bimssteinkörner, mit Salzsäure gewaschen und geglüht.
3.13. Acetanilid (Schmelzpunkt = 114 °C, N-Gehalt = 10,36 %).
3.14. Saccharose (stickstofffrei).
3.15. Borsäure (H3BO3).
3.16. Methylrot-Indikatorlösung: 100 mg Methylrot werden in 100 ml Ethanol oder Methanol gelöst.
3.17. Bromkresolgrünlösung: 100 mg Bromkresolgrün werden in 100 ml Ethanol oder Methanol gelöst.
3.18. Borsäurelösung (10 bis 40 g/l in Abhängigkeit vom eingesetzten Gerät)
Bei einer kolorimetrischen Endpunktbestimmung sind der Borsäurelösung Methylrot- und Bromkresolindikatoren zuzufügen. Wird 1 l Borsäurelösung zubereitet, sind vor dem Auffüllen zur Marke 7 ml Methylrot-Indikatorlösung (Nummer 3.16) und 10 ml Bromkresolgrünlösung (Nummer 3.17) zuzufügen.
In Abhängigkeit von dem verwendeten Wasser kann sich der pH-Wert von einer Borsäurelösung zur anderen unterscheiden. Der pH-Wert der Borsäurelösung muss zwischen 4,3 und 4,7 liegen. Häufig ist eine Einstellung des pH-Werts mithilfe einer geringen Menge Alkali erforderlich, um eine positive Blindprobe zu erhalten.
Anmerkung: Eine Zugabe von rund 3 ml bis 4 ml NaOH (Nummer 3.11) zu 1 l Borsäure von 10 g/l führt in der Regel zu guten Einstellungen. Die Lösung ist bei Raumtemperatur aufzubewahren und während der Aufbewahrung vor Lichteinfall und Ammoniakdämpfen zu schützen.
3.19. Salzsäure, volumetrische Standardlösung, c(HCl) = 0,10 mol/l.
| Anmerkung: | Andere Konzentrationen volumetrischer Lösungen (Nummer 3.5, 3.6, 3.7, 3.10, 3.11 und 3.19) können verwendet werden, sofern die Berechnungen entsprechend berichtigt werden. Die Konzentrationen sind stets auf 4 Dezimalstellen genau anzugeben. |
4. Geräte
Für Aufschluss, Destillation und Titration nach dem Kjeldahl-Verfahren geeignete Geräte.
5. Verfahren
5.1. Aufschluss
Von der Probe wird 1 g auf 0,001 g genau gewogen und in den Kolben des Aufschlussgeräts gegeben. Anschließend werden 15 g Kaliumsulfat (Nummer 3.1), eine geeignete Katalysatormenge (Nummer 3.2) (0,3 bis 0,4 g Kupfer(II)-oxid oder 0,9 bis 1,2 g Kupfer(II)-sulfatpentahydrat), 25 ml Schwefelsäure (Nummer 3.4) und ggf. einige Bimssteinkörnchen (Nummer 3.12) zugesetzt und vermischt.
Der Kolben wird, wenn notwendig, unter regelmäßigem Schwenken zunächst mäßig erhitzt, bis die Substanz verkohlt ist und das Schäumen aufgehört hat. Dann wird die Flüssigkeit stärker erhitzt und gleichmäßig am Sieden gehalten. Bei korrekter Erhitzung kondensiert die siedende Säure auf der Kolbenwand. Ein Überhitzen der Kolbenwände und Ansetzen organischer Partikel ist zu vermeiden.
Sobald die Lösung klar ist und sich hellgrün färbt, wird sie noch weitere 2 h am Sieden gehalten und danach abkühlen gelassen.
5.2. Destillation
Es wird vorsichtig so viel Wasser zugegeben, dass die Sulfate vollständig gelöst werden. Nach dem Abkühlen werden ggf. einige Körner Zinkgranulat (Nummer 3.3) zugesetzt. Es wird entweder gemäß Nummer 5.2.1 oder 5.2.2 weiterverfahren.
5.2.1. Destillation von Schwefelsäure
In den Auffangkolben des Destillationsapparats werden je nach dem zu erwartenden Stickstoffgehalt genau 25 ml Schwefelsäure (Nummer 3.5 oder 3.7) gebracht und einige Tropfen Methylrot-Indikator (Nummer 3.8) hinzugefügt.
Der Aufschlusskolben wird mit dem Kühler des Destillationsapparats verbunden und das Ende des Kühlers mindestens 1 cm tief in die Flüssigkeit des Auffangkolbens gesenkt (siehe Bemerkung 8.3). Dann werden 100 ml Natriumhydroxidlösung (Nummer 3.9) langsam in den Aufschlusskolben eingefüllt, wobei kein Ammoniak entweichen darf (siehe Bemerkung 8.1). Der Kolben wird so lange erhitzt, bis alles Ammoniak überdestilliert ist.
5.2.2. Destillation von Borsäure
Wird der Ammoniakgehalt des Destillats von Hand titriert, findet das im Folgenden beschriebene Verfahren Anwendung. Bei einem voll automatisierten Destilliergerät, das auch die Titration des Ammoniakgehalts des Destillats vornimmt, ist die Betriebsanleitung des Herstellers zu befolgen.
Ein Auffangkolben mit 25 bis 30 ml Borsäurelösung (Nummer 3.18) wird so unter den Ablauf des Kühlers gestellt, dass sich das Ablaufrohr unter der Oberfläche der überschüssigen Borsäurelösung befindet. Das Destilliergerät wird so eingestellt, dass es 50 ml Natriumhydroxidlösung (Nummer 3.9) abgibt. Die Bedienung des Destilliergeräts erfolgt entsprechend den Anleitungen des Herstellers. Anschließend wird das durch die Zugabe der Natriumhydroxidlösung freigesetzte Ammoniak abdestilliert. Das Destillat wird in der Borsäure (Auffangsäure) aufgefangen. Die Destillatmenge (Dauer der Dampfdestillation) hängt von der in der Probe enthaltenen Menge Stickstoff ab. Hierbei sind die Anleitungen des Herstellers zu befolgen.
| Anmerkung: | In einem halbautomatischen Destilliergerät erfolgen die Zugabe von überschüssigem Natriumhydroxid und die Dampfdestillation automatisch. |
5.3. Titration
Es wird entweder gemäß Nummer 5.3.1 oder 5.3.2 weiterverfahren.
5.3.1. Schwefelsäure
Die überschüssige Schwefelsäure im Auffangkolben wird mit Natriumhydroxidlösung (Nummer 3.10 oder 3.11) in Abhängigkeit von der Konzentration der verwendeten Schwefelsäure titriert, bis der Endpunkt erreicht ist.
5.3.2. Borsäure
Der Inhalt des Auffangkolbens wird mit der volumetrischen Standardlösung der Salzsäure (Nummer 3.19) oder mit der volumetrischen Standardlösung der Schwefelsäure (Nummer 3.6) unter Verwendung einer Bürette titriert und es wird die Menge des eingesetzten Titrationsmittels abgelesen.
Bei der kolorimetrischen Endpunktbestimmung ist der Endpunkt erreicht, wenn sich der Inhalt erstmals pink verfärbt. Die Bürette ist auf 0,05 ml genau abzulesen. Eine beleuchtete Magnetrührplatte oder ein fotometrischer Detektor können bei der Visualisierung des Endpunkts hilfreich sein.
Dies kann automatisch erfolgen bei Verwendung eines Wasserdampfdestillators mit automatischer Titration.
Hinsichtlich des Betriebs des jeweiligen Destillators bzw. des Destillier-/Titriergeräts sind die Anleitungen des Herstellers zu befolgen.
| Anmerkung: | Bei Verwendung eines automatischen Titrationssystems beginnt die Titration unmittelbar mit dem Start der Destillation, und es wird die 1%ige Borsäurelösung (Nummer 3.18) eingesetzt. |
Wird ein vollautomatisches Destilliergerät eingesetzt, kann die automatische Titration des Ammoniaks auch mittels Endpunktbestimmung unter Verwendung eines potenziometrischen pH-Systems durchgeführt werden.
In diesem Fall wird eine automatische Titriervorrichtung mit einem pH-Meter verwendet. Das pH-Meter ist nach dem üblichen Labor-pH-Kalibrierverfahren ordnungsgemäß im Bereich pH 4 bis pH 7 zu kalibrieren.
Der pH-Endpunkt der Titration ist bei einem pH-Wert von 4,6 erreicht, dem steilsten Punkt der Titrationskurve (Wendepunkt).
5.4. Blindversuch
Zur Bestätigung, dass die Reagenzien stickstofffrei sind, wird ein Blindversuch (Aufschluss, Destillation und Titration) mit 1 g Saccharose (Nummer 3.14) anstelle der Probe durchgeführt.
6. Berechnung der Ergebnisse
Die Berechnungen werden gemäß Nummer 6.1 oder 6.2 durchgeführt.
6.1. Berechnung für die Titration nach Nummer 5.3.1
Der Rohproteingehalt, ausgedrückt als Massenanteil, wird nach folgender Formel berechnet:
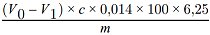
wobei:
| V0 = | Volumen NaOH (Nummer 3.10 oder 3.11), das im Blindversuch eingesetzt wurde, in ml, |
| V1 = | Volumen NaOH (Nummer 3.10 oder 3.11), das in der Titration der Probe eingesetzt wurde, in ml, |
| c = | Konzentration des Natriumhydroxids (Nummer 3.10 oder 3.11), in mol/l, |
| m = | Probeneinwaage in g. |
6.2. Berechnung für die Titration nach Nummer 5.3.2
6.2.1. Titration mit Salzsäure
Der Rohproteingehalt, ausgedrückt als Massenanteil, wird nach folgender Formel berechnet:
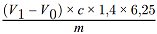
wobei:
| m = | Probeneinwaage in g, |
| c = | Konzentration der volumetrischen Standardlösung von Salzsäure (Nummer 3.19), in mol/l, |
| V0 = | Volumen der Salzsäure, die im Blindversuch eingesetzt wurde, in ml, |
| V1 = | Volumen der Salzsäure, die für die Probenmenge eingesetzt wurde, in ml. |
6.2.2. Titration mit Schwefelsäure
Der Rohproteingehalt, ausgedrückt als Massenanteil, wird nach folgender Formel berechnet:
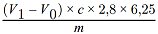
wobei:
| m = | Probeneinwaage in g, |
| c = | Konzentration der volumetrischen Standardlösung von Schwefelsäure (Nummer 3.6), in mol/l, |
| V0 = | Volumen der Schwefelsäure (Nummer 3.6), die im Blindversuch eingesetzt wurde, in ml, |
| V1 = | Volumen der Schwefelsäure (Nummer 3.6), die für die Probenmenge eingesetzt wurde, in ml. |
7. Beurteilung des Verfahrens
7.1. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf die folgenden Werte nicht überschreiten:
7.2. Vergleichbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in unterschiedlichen Laboratorien darf die folgenden Werte nicht überschreiten:
7.3. Genauigkeit
Die Analyse (Aufschluss, Destillation und Titration) wird mit einer geeigneten Menge Acetanilid (Nummer 3.13) (z.B. 0,2 bis 0,3 g) in Gegenwart von 1 g Saccharose (Nummer 3.14) durchgeführt; 1 g Acetanilid verbraucht 14,80 ml Schwefelsäure (Nummer 3.5). Die Wiederfindung muss mindestens 99 % betragen.
8. Bemerkungen
8.1. Es können manuelle, halbautomatische oder automatische Geräte verwendet werden. Bei Geräten, die ein Umfüllen zwischen Aufschluss und Destillation erfordern, ist darauf zu achten, dass dies verlustlos geschieht. Verfügt der Destillationsapparat nicht über einen Tropftrichter, so erfolgt die Zugabe der Natriumhydroxidlösung unmittelbar vor dem Anschließen des Kolbens an den Kühler; die Flüssigkeit ist in diesem Fall langsam an den Kolbenwänden entlang laufen zu lassen.
8.2. Kommt es während des Aufschlusses zur Verfestigung der Mischung, ist mit der Bestimmung von vorn zu beginnen und eine größere als die unter Nummer 5.1 genannte Menge an Schwefelsäure (Nummer 3.4) zu verwenden.
8.3. Bei stickstoffarmen Proben kann die in den Auffangkolben einzufüllende Menge Schwefelsäure (Nummer 3.7) gegebenenfalls auf 10 oder 15 ml verringert und mit Wasser auf 25 ml aufgefüllt werden.
8.4. Für Routineanalysen können auch andere Methoden zur Bestimmung des Rohproteins herangezogen werden; die in diesem Teil C beschriebene Kjeldahl-Methode ist jedoch die Referenzmethode. Die Gleichwertigkeit der Ergebnisse der alternativen Methode (z.B. DUMAS) im Vergleich zur Referenzmethode muss für jede Matrix einzeln nachgewiesen werden. Da die mit einer alternativen Methode erzielten Ergebnisse auch nach Feststellung ihrer Gleichwertigkeit leicht von den mit der Referenzmethode erzielten Ergebnissen abweichen können, muss im Analysebericht angegeben werden, welche Analysemethode zur Bestimmung des Rohproteins angewendet wurde.
D. Bestimmung des Harnstoffgehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt des als Futtermittelzusatzstoff in Futtermitteln für Wiederkäuer verwendeten Harnstoffs bestimmen.
2. Prinzip
Die Probe wird unter Zusatz eines Klärungsmittels in Wasser suspendiert. Die Suspension wird filtriert. Nach Zugabe von 4-Dimethylaminobenzaldehyd (4-DMAB) wird der Gehalt an Harnstoff im Filtrat durch Messung der Extinktion bei einer Wellenlänge von 420 nm bestimmt.
3. Reagenzien
3.1. 4-Dimethylaminobenzaldehydlösung: 1,6 g 4-DMAB werden in 100 ml 96%igen Ethanols gelöst und 10 ml Salzsäure (ρ20 = 1,19 g/ml) werden hinzugefügt. Das Reagenz ist höchstens 2 Wochen haltbar.
3.2. Carrez-Lösung I: 21,9 g Zinkacetat, Zn (CH3COO)2·2H2O, und 3 g Eisessig werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.3. Carrez-Lösung II: 10,6 g Kaliumhexacyanoferrat(II), K4Fe(CN)6·3H2O, werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.4. Aktivkohle, keinen Harnstoff adsorbierend (zu prüfen).
3.5. Harnstofflösung (Massenkonzentration = 0,1 %).
4. Geräte
4.1. Mechanisches Schüttelgerät: ca. 35 bis 40 min-1.
4.2. Reagenzgläser: 160 × 16 mm, mit Schliffstopfen.
4.3. Spektralfotometer.
5. Verfahren
5.1. Analysengang der Probe
Von der Probe werden 2 g auf 1 mg genau eingewogen und mit 1 g Aktivkohle (Nummer 3.4) in einen 500-ml-Messkolben gebracht. Hierzu werden 400 ml Wasser und 5 ml Carrez-Lösung I (Nummer 3.2) gegeben, ca. 30 s gemischt und dann 5 ml Carrez-Lösung II (Nummer 3.3) zugesetzt. Das Ganze wird 30 min lang im Schüttelgerät rotiert. Dann wird mit Wasser zur Marke aufgefüllt, geschüttelt und filtriert.
Von den klaren und farblosen Filtraten werden je 5 ml in je ein Reagenzglas mit Schliffstopfen pipettiert, 5 ml 4-DMAB-Lösung (Nummer 3.1) zugesetzt und gemischt. Die Gläser werden in einem Wasserbad bei 20 °C (+/- 4 °C) temperiert. Nach 15 min wird die Extinktion der Probenlösung im Vergleich mit der Blindprobenlösung der Reagenzien im Spektralfotometer bei 420 nm gemessen.
5.2. Kalibrationskurve
Volumen von 1, 2, 4, 5 bzw. 10 ml Harnstofflösung (Nummer 3.5) werden entnommen, in je 100-ml-Messkolben gebracht und mit Wasser zur Marke aufgefüllt. Von jeder Lösung werden 5 ml mit je 5 ml 4-DMAB-Lösung (Nummer 3.1) gemischt. Die Extinktion wird, wie oben angegeben, im Vergleich mit einer Lösung, die 5 ml 4-DMAB und 5 ml harnstofffreies Wasser enthält, gemessen. Es wird eine Kalibrationskurve aufgestellt.
6. Berechnung der Ergebnisse
Mithilfe der Kalibrationskurve ist die Menge an Harnstoff in der Probe zu bestimmen.
Das Ergebnis ist in mg Harnstoff pro kg Probe auszudrücken.
7. Beurteilung des Verfahrens
7.1. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in ein und demselben Labor und durch denselben Bearbeiter darf die folgenden Werte nicht überschreiten:
7.2. Vergleichbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in unterschiedlichen Laboratorien und/oder durch unterschiedliche Bearbeiter darf die folgenden Werte nicht überschreiten:
8. Ergebnisse eines Ringversuchs
Es wurde ein EU-Laborvergleichstest durchgeführt, an dem 18 Laboratorien teilnahmen. Es wurden 5 positive Proben eines Mischfuttermittels für Wiederkäuer (in den Tabellen 1 und 2 als "MAT" bezeichnet) als Doppelblindproben untersucht (1 Untersuchung) und eine Leerprobe eines Mischfuttermittels für Wiederkäuer wurde einmalig untersucht.
Die Wiederholgrenze (r) und die Vergleichsgrenze (R) wurden gemäß den internationalen Leitlinien berechnet, nachdem mithilfe einer Varianzanalyse der gültigen Werte Ausreißer eliminiert wurden.
Die für die Methode berechneten Leistungszahlen (Wiederholbarkeit, Vergleichbarkeit) sind in den nachstehenden Tabellen dargestellt. Bei der Untersuchung der Gesamtheit der Proben einschließlich des Blindmaterials wurden keine falsch positiven und keine falsch negativen Proben festgestellt.
Tabelle 1: Leistungseigenschaften der Methoden für Harnstoff bei λ = 420 nm in Bezug auf alle Materialien
| MAT 2 | MAT 5 | MAT 3 | MAT 4 | MAT 6 | |
| Schafe | Rinder | Schafe | Schafe | Rinder | |
| Zielmassenanteil (mg kg-1) | 3.000 | 5.000 | 7.001 | 9.036 | 11.000 |
| durchschnittlicher Massenanteil (mg kg-1) | 4.241 | 6.993 | 7.830 | 9.962 | 12.071 |
| Standardabweichung der Vergleichbarkeit sR (mg kg-1) | 1.141 | 1.303 | 985 | 994 | 1.711 |
| Standardabweichung der Wiederholbarkeit sr (mg kg-1) | 723 | 601 | 549 | 712 | 737 |
| relative Standardabweichung der Vergleichbarkeit RSDR (%) | 27 | 19 | 13 | 10 | 14 |
| relative Standardabweichung der Wiederholbarkeit RSDr (%) | 17 | 9 | 7 | 7 | 6 |
| Vergleichsgrenze, R [R = 2,8 × sR] | 3.195 | 3.649 | 2.759 | 2.784 | 4.790 |
| Wiederholgrenze, r [r = 2.8 × sr] | 2.024 | 1.684 | 1.536 | 1.994 | 2.064 |
Tabelle 2: Leistungseigenschaften der Methoden für Harnstoff bei λ = 435 nm in Bezug auf alle Materialien
| MAT 2 | MAT 5 | MAT 3 | MAT 4 | MAT 6 | |
| Schafe | Rinder | Schafe | Schafe | Rinder | |
| Zielmassenanteil (mg kg-1) | 3.000 | 5.000 | 7.001 | 9.036 | 11.000 |
| durchschnittlicher Massenanteil (mg kg-1) | 4.101 | 6.467 | 7.890 | 10.062 | 11.642 |
| Standardabweichung der Vergleichbarkeit sR (mg kg-1) | 706 | 1.194 | 675 | 745 | 1.378 |
| Standardabweichung der Wiederholbarkeit sr (mg kg-1) | 570 | 628 | 613 | 196 | 167 |
| relative Standardabweichung der Vergleichbarkeit RSDR (%) | 17 | 18 | 9 | 7 | 12 |
| relative Standardabweichung der Wiederholbarkeit RSDr (%) | 14 | 10 | 8 | 2 | 1 |
| Vergleichsgrenze, R [R = 2,8 × sR] | 1.977 | 3.344 | 1.889 | 2.087 | 3.859 |
| Wiederholgrenze, r [r = 2,8 × sr] | 1.596 | 1.759 | 1.715 | 549 | 467 |
9. Bemerkungen
9.1. Bei einem Harnstoffgehalt von mehr als 3 % ist die Einwaage auf 1 g zu reduzieren bzw. die Anfangslösung so weit zu verdünnen, dass in 500 ml höchstens 50 mg Harnstoff enthalten sind.
9.2. Bei niedrigen Harnstoffgehalten wird die Einwaage erhöht, soweit das Filtrat klar und farblos bleibt.
9.3. Aus den vorstehend aufgeführten Ergebnissen der Ringversuche ergibt sich kein nennenswerter Unterschied bei der Präzision der Messung von Harnstoff bei 420 nm im Vergleich zu 435 nm.
E. Bestimmung des Gehalts an Aminosäuren (Außer Tryptophan)
Die zur Bestimmung des Gehalts an Aminosäuren (außer Tryptophan) anzuwendenden Analysemethoden sind die folgenden:
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt der freien (synthetischen und natürlichen) sowie der gesamten (peptidgebundenen und freien) Aminosäuren in Futtermittel-Ausgangserzeugnissen, Mischfuttermitteln und Vormischungen, die weniger als 10 % 5 der einzelnen Aminosäuren enthalten, unter Verwendung eines Aminosäureanalysators bestimmen. Die Methode ist für folgende Aminosäuren anwendbar: Cyst(e)in, Methionin, Lysin, Threonin, Alanin, Arginin, Asparaginsäure, Glutaminsäure, Glycin, Histidin, Isoleucin, Leucin, Phenylalanin, Prolin, Serin, Tyrosin und Valin.
Die Methode unterscheidet nicht zwischen den verschiedenen Aminosäuresalzen und kann nicht zwischen D- und L-Formen von Aminosäuren differenzieren. Sie ist nicht zur Bestimmung des Gehalts an Tryptophan oder Hydroxyanaloga der Aminosäuren anwendbar.
2. Prinzip
2.1. Freie Aminosäuren
Die freien Aminosäuren werden mit verdünnter Salzsäure extrahiert. Mitextrahierte stickstoffhaltige Makromoleküle werden mit Sulfosalicylsäure ausgefällt und durch Filtrieren entfernt. Die filtrierte Lösung wird auf einen pH-Wert von 2,20 eingestellt. Die Aminosäuren werden durch Ionenaustauschchromatografie getrennt und nach Reaktion mit Ninhydrin durch fotometrischen Nachweis bei 570 nm bestimmt.
2.2. Gesamtaminosäuren
Die gewählte Methode hängt von den zu untersuchenden Aminosäuren ab. Cyst(e)in und Methionin müssen vor der Hydrolyse zu Cysteinsäure bzw. Methioninsulfon oxidiert werden. Tyrosin muss im Hydrolysat der nicht oxidierten Probe bestimmt werden. Alle übrigen unter Nummer 1 (Zweck und Anwendungsbereich) genannten Aminosäuren können aus dem Hydrolysat der oxidierten oder der nicht oxidierten Probe bestimmt werden.
Die Oxidation wird bei 0 °C mit einer Perameisensäure-Phenol-Mischung durchgeführt. Überschüssiges Oxidationsreagenz wird mit Natriumdisulfit zerstört. Die oxidierte bzw. die nicht oxidierte Probe wird mit Salzsäure (Nummer 3.20) 23 h lang hydrolysiert. Das Hydrolysat wird auf einen pH-Wert von 2,20 eingestellt. Die Aminosäuren werden durch Ionenaustauschchromatografie getrennt und nach Reaktion mit Ninhydrin durch fotometrischen Nachweis bei 570 nm (bei Prolin 440 nm) bestimmt.
3. Reagenzien
Es ist bidestilliertes Wasser oder Wasser gleichwertiger Qualität zu verwenden (Leitfähigkeit < 10 μ S/cm).
3.1. Wasserstoffperoxid, w (Massenanteil) = 30 %.
3.2. Ameisensäure, w (Massenanteil) = 98 bis 100 %.
3.3. Phenol.
3.4. Natriumdisulfit.
3.5. Natriumhydroxid.
3.6. 5-Sulfosalicylsäure-Dihydrat.
3.7. Salzsäure, Dichte ca. 1,18 g/ml.
3.8. Tri-Natriumcitrat-Dihydrat.
3.9. 2,2"-Thiodiethanol (Thiodiglycol).
3.10. Natriumchlorid.
3.11. Ninhydrin.
3.12. Petrolether, Siedeintervall 40 bis 60 °C.
3.13. Norleucin oder sonstige für die Verwendung als interner Standard geeignete Verbindung.
3.14. Stickstoffgas (< 10 ppm Sauerstoff).
3.15. 1-Octanol.
3.16. Aminosäuren.
3.16.1. Standardstoffe der unter Nummer 1 (Zweck und Anwendungsbereich) aufgeführten Aminosäuren. Es dürfen nur reine Verbindungen ohne Kristallwasser verwendet werden. Sie sind vor der Verwendung 1 Woche lang im Vakuum über P2O5 oder H2SO4 zu trocknen.
3.16.2. Cysteinsäure.
3.16.3. Methioninsulfon.
3.17. Natriumhydroxidlösung, c = 7,5 mol/l:
300 g NaOH (Nummer 3.5) in Wasser lösen und auf 1 l auffüllen.
3.18. Natriumhydroxidlösung, c = 1 mol/l:
40 g NaOH (Nummer 3.5) in Wasser lösen und auf 1 l auffüllen.
3.19. Phenolhaltige Ameisensäurelösung:
889 g Ameisensäure (Nummer 3.2) werden mit 111 g Wasser gemischt; anschließend werden 4,73 g Phenol (Nummer 3.3) hinzugefügt.
3.20. Hydrolysemischung, c = 6 mol HCl/l unter Zusatz von 1 g Phenol/l:
Zu 492 ml HCl (Nummer 3.7) wird 1 g Phenol (Nummer 3.3) hinzugefügt und mit Wasser auf 1 l aufgefüllt.
3.21. Extraktionslösung, c = 0,1 mol HCl/l, 2 % Thiodiglycol enthaltend: 8,2 ml HCl (Nummer 3.7) werden in ca. 900 ml Wasser gegeben, 20 ml Thiodiglycol (Nummer 3.9) werden hinzugefügt, und es wird mit Wasser auf 1 l aufgefüllt (Nummer 3.7 und 3.9 dürfen nicht unmittelbar gemischt werden).
3.22. 5-Sulfosalicylsäurelösung, β = 6 %:
60 g 5-Sulfosalicylsäure (Nummer 3.6) in Wasser lösen und mit Wasser auf 1 l auffüllen.
3.23. Oxidationsmischung (Perameisensäure-Phenol):
0,5 ml Wasserstoffperoxid (Nummer 3.1) werden mit 4,5 ml phenolhaltiger Ameisensäurelösung (Nummer 3.19) in einem kleinen Becherglas gemischt. Es wird bei 20 bis 30 °C 1 h lang stehen gelassen, um die Bildung von Perameisensäure zu bewirken. Anschließend wird die Lösung 15 min lang in ein Eisbad gestellt, bevor sie der Probe zugegeben wird.
Vorsicht: Hautkontakt vermeiden und Schutzkleidung tragen.
3.24. Citratpufferlösung, c = 0,2 mol Na+/l, pH 2,20:
19,61 g Natriumcitrat (Nummer 3.8), 5 ml Thiodiglycol (Nummer 3.9), 1 g Phenol (Nummer 3.3) und 16,50 ml HCl (Nummer 3.7) werden in ca. 800 ml Wasser gelöst. Der pH-Wert wird auf 2,20 eingestellt. Mit Wasser auf 1 l auffüllen.
3.25. Elutionspuffer entsprechend den Anforderungen des verwendeten Analysators (Nummer 4.9).
3.26. Ninhydrinreagenz entsprechend den Bedingungen des verwendeten Analysators (Nummer 4.9).
3.27. Aminosäuren-Standardlösungen: Diese Lösungen sind bei < 5 °C aufzubewahren.
3.27.1. Aminosäuren-Standard-Stammlösung (Nummer 3.16.1):
c = 2,5 μmol/ml je Aminosäure in Salzsäure.
Diese Lösung ist im Handel erhältlich.
3.27.2. Standard-Stammlösung von Cysteinsäure und Methioninsulfon, c = 1,25 μmol/ml:
0,2115 g Cysteinsäure (Nummer 3.16.2) und 0,2265 g Methioninsulfon (Nummer 3.16.3) werden in Citratpufferlösung (Nummer 3.24) in einem 1000-ml-Messkolben gelöst, und es wird mit Citratpufferlösung zur Marke aufgefüllt. Die Lösung ist bei < 5 °C höchstens 12 Monate haltbar. Sie wird nicht benötigt, falls die Standard-Stammlösung (Nummer 3.27.1) bereits Cysteinsäure und Methioninsulfon enthält.
3.27.3. Stammlösung des internen Standards, z.B. Norleucin, c = 20 μmol/ml:
0,6560 g Norleucin (Nummer 3.13) werden in Citratpufferlösung (Nummer 3.24) in einem Messkolben gelöst, und es wird mit Citratpufferlösung auf 250 ml aufgefüllt. Die Lösung ist bei < 5 °C höchstens 6 Monate haltbar.
3.27.4. Aminosäurenkalibrierlösung zur Verwendung bei Hydrolysaten, c = 5 nmol/50 μl Cysteinsäure und Methioninsulfon und c = 10 nmol/50 μl der übrigen Aminosäuren: 2,2 g Natriumchlorid (Nummer 3.10) werden in einem 100-ml-Becherglas in 30 ml Citratpufferlösung (Nummer 3.24) gelöst. Es werden 4,00 ml Standard-Stammlösung der Aminosäuren (Nummer 3.27.1), 4,00 ml Standard-Stammlösung von Cysteinsäure und Methioninsulfon (Nummer 3.27.2), und, falls verwendet, 0,50 ml Stammlösung des internen Standards (Nummer 3.27.3) hinzugefügt. Der pH-Wert wird mit Natriumhydroxid (Nummer 3.18) auf 2,20 eingestellt.
Die Lösung wird quantitativ in einen 50-ml-Messkolben überführt, und es wird mit Citratpufferlösung (Nummer 3.24) zur Marke aufgefüllt und gemischt.
Die Lösung ist bei < 5 °C höchstens 3 Monate haltbar.
Siehe auch die Bemerkungen unter 9.1.
3.27.5. Aminosäurenkalibrierlösung zur Verwendung bei Hydrolysaten gemäß Nummer 5.3.3.1 und bei Extrakten gemäß Nummer 5.2. Die Kalibrierlösung wird gemäß Nummer 3.27.4 hergestellt, jedoch ohne Zugabe von Natriumchlorid.
Die Lösung ist bei < 5 °C höchstens 3 Monate haltbar.
4. Geräte
4.1. 100- oder 250-ml-Rundkolben mit Rückflusskühler.
4.2. Ofenfeste 100-ml-Borosilikat-Glasflaschen mit Schraubverschluss mit Gummidichtung/teflonbeschichteter Dichtung (z.B. Duran, Schott).
4.3. Trockenschrank mit forcierter Umluft, auf ± 2 °C regelbar.
4.4. pH-Meter (auf drei Dezimalstellen genau).
4.5. Membranfilter, 0,22 μm Porengröße.
4.6. Zentrifuge.
4.7. Vakuum-Rotationsverdampfer.
4.8. Mechanischer Schüttler oder Magnetrührer.
4.9. Aminosäureanalysator oder HPLC-Einrichtung mit Ionenaustauschersäule, Einrichtung für Ninhydrin-Nachsäulenderivatisierung und Fotometer.
Die Säule wird mit sulfoniertem Polystyrolharz gefüllt, das die Trennung der einzelnen Aminosäuren und deren Abtrennung von sonstigen Ninhydrin-positiven Substanzen ermöglicht. Die Pumpen für die Ninhydrin- und für die Pufferlösungen müssen über den Zeitraum des Kalibrationslaufes und des Probenlaufes eine Flussstabilität von ± 0,5 % gewährleisten.
Bei einigen Aminosäureanalysatoren können auch Hydrolyseverfahren angewandt werden, wenn die Hydrolysate Natriumionenkonzentrationen von c = 0,8 mol/l aufweisen und die restliche Ameisensäure des Oxidationsschrittes enthalten. Andere Analysatoren bieten keine befriedigende Abtrennung bestimmter Aminosäuren, falls das Hydrolysat überschüssige Ameisensäure und/oder hohe Natriumionenkonzentrationen aufweist. In diesem Fall wird das Säurevolumen nach der Hydrolyse und vor der pH-Wert-Einstellung durch Einengen auf ca. 5 ml reduziert. Das Einengen ist unter Vakuum bei höchstens 40 °C vorzunehmen.
5. Verfahren
5.1. Vorbereitung der Probe
Die Probe wird so fein zermahlen, dass sie ein Sieb mit 0,5 mm Maschenweite passieren kann. Proben mit hohem Feuchtigkeitsgehalt müssen vor dem Zermahlen entweder bei einer Temperatur von höchstens 50 °C luftgetrocknet oder aber gefriergetrocknet werden. Proben mit hohem Fettgehalt sind vor dem Zermahlen mit Petrolether (Nummer 3.12) zu extrahieren.
5.2. Bestimmung des Gehalts an freien Aminosäuren
Eine geeignete Menge (1 bis 5 g) der vorbereiteten Probe (Nummer 5.1) auf 0,2 mg genau in einen Erlenmeyerkolben einwiegen und 100,0 ml Extraktionslösung (Nummer 3.21) hinzufügen. Mit einem mechanischen Schüttler 60 min lang schütteln bzw. mit einem Magnetrührer (Nummer 4.8) rühren. Absetzen lassen und 10,0 ml der überstehenden Lösung in ein 100-ml-Becherglas pipettieren.
Es werden 5,0 ml Sulfosalicylsäurelösung (Nummer 3.22) unter Rühren hinzugefügt, und mithilfe des Magnetrührers wird 5 min lang weitergerührt. Die überstehende Lösung wird filtriert oder zentrifugiert, um alle Ausfällungen zu entfernen. Von der so erhaltenen Lösung werden 10,0 ml in ein 100-ml-Becherglas gegeben, und unter Verwendung von Natriumhydroxidlösung (Nummer 3.18) wird der pH-Wert auf 2,20 eingestellt. Die Lösung wird mit Citratpufferlösung (Nummer 3.24) in einen Messkolben geeigneter Größe überführt und mit Citratpufferlösung (Nummer 3.24) zur Marke aufgefüllt.
Bei Verwendung eines internen Standards werden vor dem Auffüllen 1,00 ml der Stammlösung des internen Standards (Nummer 3.27.3) für jeweils 100 ml Endlösung hinzugefügt und mit Citratpufferlösung (Nummer 3.24) zur Marke aufgefüllt.
Anschließend wird die Chromatografie gemäß Nummer 5.4 durchgeführt.
Werden die Extrakte nicht am selben Tag chromatografiert, sind sie bei < 5 °C aufzubewahren.
5.3. Bestimmung des Gehalts an Gesamtaminosäuren
5.3.1. Oxidation
0,1 bis 1 g der vorbereiteten Probe (Nummer 5.1) werden auf 0,2 mg genau eingewogen
Die Einwaage muss einen Stickstoffgehalt von etwa 10 mg und einen Feuchtigkeitsgehalt von höchstens 100 mg haben.
Der Kolben/die Flasche wird in ein Eisbad gestellt und auf 0 °C abgekühlt. Dann werden 5 ml der Oxidationsmischung (Nummer 3.23) hinzugefügt, und es wird mithilfe eines Glasspatels mit gebogener Spitze gemischt. Der Behälter, der den Spatel enthält, wird mit einer luftdichten Folie verschlossen, das Eiswasserbad wird mit dem verschlossenen Behälter in einen Kühlschrank mit einer Temperatur von 0 °C gestellt und 16 h lang stehen gelassen. Nach 16 h wird der Behälter aus dem Kühlschrank genommen und das überschüssige Oxidationsreagenz wird durch Zusatz von 0,84 g Natriumdisulfit (Nummer 3.4) zersetzt.
Es wird gemäß Nummer 5.3.2.1 weiterverfahren.
5.3.2. Hydrolyse
5.3.2.1. Hydrolyse der oxidierten Proben
Zu der oxidierten Probe (die gemäß Nummer 5.3.1 vorbereitet wurde) werden 25 ml Hydrolysemischung (Nummer 3.20) gegeben. Dabei ist darauf zu achten, dass alle Probenrückstände, die an den Seitenwänden des Gefäßes sowie am Spatel haften, abgewaschen werden.
Je nach dem angewendeten Hydrolyseverfahren wird gemäß Nummer 5.3.2.3 oder 5.3.2.4 weiterverfahren.
5.3.2.2. Hydrolyse der nicht oxidierten Proben
In einen 100-ml- oder 250-ml-Rundkolben (Nummer 4.1) bzw. in eine 100-ml-Flasche mit Schraubverschluss (Nummer 4.2) werden 0,1 bis 1 g der vorbereiteten Probe (Nummer 5.1) auf 0,2 mg genau eingewogen. Die Einwaage muss einen Stickstoffgehalt von ca. 10 mg aufweisen. Vorsichtig 25 ml Hydrolysemischung (Nummer 3.20) hinzufügen und mit der Probe vermischen. Es wird entweder gemäß Nummer 5.3.2.3 oder gemäß Nummer 5.3.2.4 weiterverfahren.
5.3.2.3. Offene Hydrolyse (Rückflusshydrolyse)
Zu der nach Nummer 5.3.2.1 oder 5.3.2.2 hergestellten Mischung werden 3 Glasperlen hinzugegeben. Sie wird zum Sieden erhitzt und unter Rückfluss 23 h lang am Sieden gehalten. Nach Beendigung der Hydrolyse wird der Rückflusskühler mit 5 ml Citratpufferlösung (Nummer 3.24) gespült und der abgehängte Kolben im Eisbad gekühlt.
Es wird gemäß Nummer 5.3.3 weiterverfahren.
5.3.2.4. Geschlossene Hydrolyse
Die Flasche mit der nach Nummer 5.3.2.1 oder 5.3.2.2 vorbereiteten Mischung wird bei 110 °C in den Trockenschrank (Nummer 4.3) gestellt. Um einen durch Gasentwicklung hervorgerufenen Druckaufbau zu vermeiden und eine Explosion zu verhindern, wird der Schraubverschluss während der ersten Stunde nur lose auf die Flasche gelegt. Die Flasche darf nicht verschlossen werden. Nach 1 h wird die Flasche mit dem Deckel fest verschlossen und 23 h lang im Trockenschrank (Nummer 4.3) belassen. Nach Beendigung der Hydrolyse wird die Flasche aus dem Trockenschrank genommen, der Verschluss vorsichtig geöffnet, die Flasche in ein Eisbad gestellt und abkühlen gelassen.
Je nach dem Verfahren für die pH-Wert-Einstellung (Nummer 5.3.3) wird der Inhalt der Flasche quantitativ mit Citratpufferlösung (Nummer 3.24) in ein 250-ml-Becherglas oder in einen 250-ml-Rundkolben überführt.
Es wird gemäß Nummer 5.3.3 weiterverfahren.
5.3.3. pH-Wert-Einstellung
Je nach der Natriumionentoleranz des Aminosäureanalysators (Nummer 4.9) wird die pH-Wert-Einstellung gemäß Nummer 5.3.3.1 oder 5.3.3.2 vorgenommen.
5.3.3.1. Für chromatografische Systeme (Nummer 4.9), die eine niedrige Natriumionenkonzentration erfordern
Werden Aminosäureanalysatoren verwendet, bei denen eine geringe Natriumionenkonzentration erforderlich ist (wenn also das Säurevolumen reduziert werden muss), wird die Verwendung einer Stammlösung eines internen Standards (Nummer 3.27.3) empfohlen.
In diesem Fall sind dem Hydrolysat vor dem Verdampfen 2,00 ml der internen Standardlösung (Nummer 3.27.3) hinzuzufügen.
Zu dem nach Nummer 5.3.2.3 oder 5.3.2.4 erhaltenen Hydrolysat werden 2 Tropfen 1-Octanol (Nummer 3.15) gegeben.
Das Volumen wird mithilfe eines Rotationsverdampfers (Nummer 4.7) unter Vakuum bei 40 °C auf 5 bis 10 ml reduziert. Wurde das Volumen beim Einengen versehentlich auf weniger als 5 ml reduziert, wird das Hydrolysat verworfen und die Analyse wiederholt.
Der pH-Wert wird mit Natriumhydroxidlösung (Nummer 3.18) auf 2,20 eingestellt, und es wird gemäß Nummer 5.3.4 weiterverfahren.
5.3.3.2. Für alle sonstigen Aminosäureanalysatoren (Nummer 4.9)
Die nach Nummer 5.3.2.3 oder 5.3.2.4 erhaltenen Hydrolysate werden durch vorsichtige Zugabe unter Rühren von 17 ml Natriumhydroxidlösung (Nummer 3.17) teilweise neutralisiert, wobei eine Temperatur von unter 40 °C eingehalten werden muss.
Der pH-Wert wird mit Natriumhydroxidlösung (Nummer 3.17 und anschließend 3.18) bei Raumtemperatur auf 2,20 eingestellt, und es wird gemäß Nummer 5.3.4 weiterverfahren.
5.3.4. Probenlösung für die Chromatografie
Das auf pH 2,20 eingestellte Hydrolysat (Nummer 5.3.3.1 oder 5.3.3.2) wird mit Citratpufferlösung (Nummer 3.24) quantitativ in einen 200-ml-Messkolben überführt und mit Citratpufferlösung (Nummer 3.24) zur Marke aufgefüllt.
Falls bisher noch kein interner Standard hinzugefügt worden ist, werden vor dem Auffüllen 2,00 ml des internen Standards (Nummer 3.27.3) hinzugegeben und dann mit Citratpufferlösung (Nummer 3.24) zur Marke aufgefüllt. Es wird sorgfältig gemischt.
Anschließend wird die Chromatografie gemäß Nummer 5.4 durchgeführt.
Falls die Probenlösungen nicht am selben Tag chromatografiert werden, sind sie bei < 5 °C aufzubewahren.
5.4. Chromatografie
Falls erforderlich, wird der Extrakt (Nummer 5.2) oder das Hydrolysat (Nummer 5.3.4) vor der Chromatografie auf Raumtemperatur gebracht. Die Mischung wird geschüttelt und es wird eine geeignete Menge durch einen 0,22-μm-Membranfilter (Nummer 4.5) filtriert. Die so erhaltene klare Lösung wird der Ionenaustauschchromatografie unter Verwendung eines Aminosäureanalysators bzw. einer HPLC-Einrichtung (Nummer 4.9) unterzogen.
Die Einspritzung kann von Hand oder automatisch erfolgen. Wesentlich ist, dass jeweils die gleiche Menge ± 0,5 % der Standardlösung und der Probenlösung eingespritzt wird, es sei denn, es wird ein interner Standard verwendet. Das Verhältnis der Konzentrationen von Natriumionen und Aminosäuren sollte in der Standard- und der Probenlösung so ähnlich wie möglich sein.
Die Häufigkeit von Kalibrationsläufen hängt von der Stabilität des Ninhydrinreagenzes und des Analysatorsystems ab. Die Standardlösung oder die Probenlösung wird mit Citratpufferlösung (Nummer 3.24) so verdünnt, dass die Peakfläche des Standards etwa 30 bis 200 % der Peakfläche der einzelnen Aminosäuren in der Probenlösung ausmacht.
Die Chromatografie der Aminosäuren unterscheidet sich leicht je nach Art des verwendeten Analysators und des eingesetzten Harzes. Das System muss in der Lage sein, die Aminosäuren vollständig voneinander und von den sonstigen Ninhydrin-positiven Substanzen zu trennen. Im Betriebsbereich muss das chromatografische System bei Änderungen der Aminosäuremengen, die der Säule hinzugefügt werden, eine lineare Reaktion aufweisen.
Wird eine equimolare Lösung der zu bestimmenden Aminosäuren analysiert, sollten bei der Chromatografie die unten angegebenen Verhältnisse von Tal zu Peakhöhe zwischen den überlappenden Peaks erreicht werden. Diese equimolare Lösung muss mindestens 30 % der maximalen Menge jeder Aminosäure enthalten, die mit dem jeweiligen Aminosäureanalysator (Nummer 4.9) noch präzise bestimmt werden kann.
Für die Trennung von Threonin-Serin darf das Verhältnis von Tal zur Peakhöhe des niedrigeren der 2 sich überlappenden Peaks auf dem Chromatogramm nicht mehr als 2:10 betragen (wenn nur Cyst(e)in, Methionin, Threonin und Lysin bestimmt werden, beeinträchtigt eine unzureichende Trennung von angrenzenden Peaks die Bestimmung). Für alle übrigen Aminosäuren sollte die Trennung besser als 1:10 sein.
Das System muss gewährleisten, dass Lysin von "Lysinartefakten" und Omithin abgetrennt wird.
6. Berechnung der Ergebnisse
Die Flächen der Proben- und der Kalibrationsstandardpeaks werden für jede einzelne Aminosäure bestimmt und der Gehalt (X) in g Aminosäure je kg Probe berechnet:
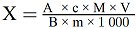
Bei Verwendung eines internen Standards ist zu multiplizieren mit D/C
| A | = | Peakfläche, Hydrolysat oder Extrakt |
| B | = | Peakfläche, Kalibrierstandardlösung |
| C | = | Peakfläche, interner Standard im Hydrolysat oder Extrakt |
| D | = | Peakfläche, interner Standard, Kalibrierstandardlösung |
| M | = | Molmasse der zu bestimmenden Aminosäure |
| c | = | Konzentration des Standards in μmol/ml |
| m | = | Probeneinwaage (auf Originalgewicht berichtigt, falls getrocknet oder entfettet), in g |
| V | = | Gesamtvolumen des Hydrolysats (Nummer 5.3.4) in ml oder errechnetes Gesamtverdünnungsvolumen des Extrakts (Nummer 6.1) in ml |
Sowohl Cystin als auch Cystein werden im Hydrolysat der oxidierten Probe als Cysteinsäure bestimmt, jedoch als Cystin (C6H12N2O4S2, M = 240,30 g/mol) unter Verwendung der Molmasse von 120,15 g/mol (0,5 × 240,30 g/mol) berechnet.
Methionin wird als Methioninsulfon in Hydrolysaten der oxidierten Probe bestimmt, aber unter Verwendung des M von Methionin (149,21 g/mol) als Methionin berechnet.
Zugesetztes freies Methionin wird nach Extraktion als Methionin bestimmt, wobei für die Berechnung das gleiche M verwendet wird.
6.1. Das Gesamtverdünnungsvolumen der Extrakte (F) für die Bestimmung des Gehalts an freien Aminosäuren (Nummer 5.2) wird wie folgt berechnet:
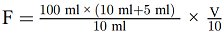
| V = Volumen des Endextrakts. |
7. Beurteilung des Verfahrens
Das Verfahren wurde in einem auf internationaler Ebene im Jahr 1990 durchgeführten Vergleichstest an 4 verschiedenen Futtermitteln (Mischfuttermittel für Schweine, Mischfuttermittel für Masthähnchen, Eiweißkonzentrat und einer Vormischung) erprobt.
| Anmerkung: | Das Verfahren wurde 2003 in einem zweiten internationalen Vergleichstest anhand von Paaren von Doppelblindproben von Finisherfutter für Masthähnchen, Starterfutter für Mastküken, Mais, Fischmehl und Geflügelfutter erprobt. Zu den Einzelheiten siehe EN ISO 13903. |
Die nach der Eliminierung von Ausreißern erhaltenen Ergebnisse des Vergleichstests aus dem Jahr 1990 (Mittelwerte und Standardabweichungen) sind in den Tabellen unter diesem Punkt dargestellt.
Mittelwerte in g/kg
| Referenzmaterial | Aminosäure | |||
| Threonin | Cyst(e)in | Methionin | Lysin | |
| Schweinemischfutter | 6,94 n = 15 | 3,01 n = 17 | 3,27 n = 17 | 9,55 n = 13 |
| Masthähnchenmischfutter | 9,31 n = 16 | 3,92 n = 18 | 5,08 n = 18 | 13,93 n = 16 |
| Eiweißkonzentrat | 22,32 n = 16 | 5,06 n = 17 | 12,01 n = 17 | 47,74 n = 15 |
| Vormischung | 58,42 n = 16 | - | 90,21 n = 16 | 98,03 n = 16 |
| n = Anzahl der beteiligten Laboratorien. | ||||
7.1. Wiederholbarkeit
Die Wiederholbarkeit wird als Standardabweichung der Wiederholbarkeit beim in der vorstehenden Tabelle dargestellten Vergleichstest ausgedrückt und ist in der folgenden Tabelle dargestellt:
Variationskoeffizient der Wiederholbarkeit (%) (VKr)
| Referenzmaterial | Aminosäure | |||
| Threonin | Cyst(e)in | Methionin | Lysin | |
| Schweinemischfutter | 1,9 n = 15 | 3,3 n = 17 | 3,4 n = 17 | 2,8 n = 13 |
| Masthähnchenmischfutter | 2,1 n = 16 | 2,8 n = 18 | 3,1 n = 18 | 2,1 n = 16 |
| Eiweißkonzentrat | 2,7 n = 16 | 2,6 n = 17 | 2,2 n = 17 | 2,4 n = 15 |
| Vormischung | 2,2 n = 16 | - | 2,4 n = 16 | 2,1 n = 16 |
| n = Anzahl der beteiligten Laboratorien. | ||||
7.2. Vergleichbarkeit
Die Ergebnisse hinsichtlich der Standardabweichung der Vergleichbarkeit, die sich aus dem oben genannten Vergleichstest ergeben, sind in der folgenden Tabelle dargestellt.
Variationskoeffizient der Vergleichbarkeit (%) (VKR)
| Referenzmaterial | Aminosäure | |||
| Threonin | Cyst(e)in | Methionin | Lysin | |
| Schweinemischfutter | 4,1 n = 15 | 9,9 n = 17 | 7,0 n = 17 | 3,2 n = 13 |
| Masthähnchenmischfutter | 5,2 n = 16 | 8,8 n = 18 | 10,9 n = 18 | 5,4 n = 16 |
| Eiweißkonzentrat | 3,8 n = 16 | 12,3 n = 17 | 13,0 n = 17 | 3,0 n = 15 |
| Vormischung | 4,3 n = 16 | -- | 6,9 n = 16 | 6,7 n = 16 |
| n = Anzahl der beteiligten Laboratorien. | ||||
8. Verwendung von Referenzmaterialien
Die korrekte Anwendung der Methode ist durch Mehrfachbestimmungen an zertifizierten Referenzmaterialien (soweit verfügbar) zu überprüfen. Für die Kalibration wird die Verwendung einer zertifizierten Aminosäurestandardlösung empfohlen.
9. Bemerkungen
9.1. Wegen der Unterschiede zwischen den Aminosäureanalysatoren sind die Endkonzentrationen der Aminosäurenkalibrierlösungen (vgl. Nummer 3.27.4 und 3.27.5) und der Hydrolysate (vgl. Nummer 5.3.4) als Richtwerte anzusehen.
Der lineare Reaktionsbereich des Geräts muss für alle Aminosäuren geprüft werden.
Die Standardlösung wird mit Citratpufferlösung verdünnt, um Peakflächen in der Mitte des Bereichs zu erhalten.
9.2. Falls Geräte für die Hochleistungsflüssigkeitschromatografie zur Analyse der Hydrolysate eingesetzt werden, sind die Versuchsbedingungen gemäß den Empfehlungen des Herstellers zu optimieren.
9.3. Wird diese Methode für Mischfuttermittel oder Vormischungen angewandt, die mehr als 1 % Chlorid enthalten (Kraftfuttermittel, Mineralfuttermittel, Ergänzungsfuttermittel), so könnte der Methioningehalt unterschätzt werden, und es ist eine modifizierte Oxidation erforderlich.
10. Leistungskriterien
Aus der Zusammenstellung der Ergebnisse (außer für Tyrosin) der 2 Ringversuche (aus dem Jahr 1990, wie unter Nummer 7 beschrieben, bzw. aus dem Jahr 2005, wie in EN/ISO 13903 beschrieben) ergeben sich die nachstehenden Kriterien für die Wiederholbarkeit und die Vergleichbarkeit. Die bei diesen 2 Laborvergleichstests erzielten Werte sind möglicherweise nicht auf andere als die genannten Konzentrationsbereiche und Matrizen anwendbar.
10.1. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in ein und demselben Labor und durch denselben Bearbeiter darf die folgenden Werte nicht überschreiten:
10.2. Vergleichbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in unterschiedlichen Laboratorien und/oder durch unterschiedliche Bearbeiter darf die folgenden Werte nicht überschreiten:
F. Bestimmung des Tryptophangehalts
Die zur Bestimmung des Gehalts an Tryptophan anzuwendenden Analysemethoden sind die folgenden:
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gesamtgehalt an Tryptophan und der Gehalt an freiem Tryptophan in Futtermitteln bestimmen. Sie differenziert nicht zwischen D- und L-Formen.
2. Prinzip
Zur Bestimmung des Gesamtgehalts an Tryptophan wird die Probe unter alkalischen Bedingungen mit gesättigter Bariumhydroxid-Lösung hydrolysiert, auf 110 °C erhitzt und 20 h lang auf dieser Temperatur gehalten. Nach der Hydrolyse wird ein interner Standard zugegeben.
Zur Bestimmung des Gehalts an freiem Tryptophan wird die Probe unter leicht sauren Bedingungen in Gegenwart eines internen Standards extrahiert.
Tryptophan und der interne Standard im Hydrolysat bzw. im Extrakt werden durch HPLC mit Fluoreszenzdetektor bestimmt.
3. Reagenzien
3.1. Es ist bidestilliertes Wasser oder Wasser gleichwertiger Qualität zu verwenden (Leitfähigkeit < 10 μS/cm).
3.2. Standardsubstanz: Tryptophan (Reinheit/Gehalt ≥ 99 %), im Vakuum über Phosphorpentoxid getrocknet.
3.3. Interner Standard: α-Methyl-Tryptophan (Reinheit/Gehalt ≥ 99 %), im Vakuum über Phosphorpentoxid getrocknet.
3.4. Bariumhydroxid-Octahydrat (das Ba(OH)2·8H2O darf nicht übermäßig der Luft ausgesetzt werden, um die Bildung von BaCO3 zu vermeiden, das die Bestimmung beeinträchtigen könnte) (siehe Bemerkung 9.3).
3.5. Natriumhydroxid.
3.6. Orthophosphorsäure, w (Massenanteil) = 85 %.
3.7. Salzsäure, ρ20 = 1,19 g/ml.
3.8. Methanol, HPLC-Qualität.
3.9. Petrolether, Siedeintervall 40 bis 60 °C.
3.10. Natriumhydroxidlösung, c = 1 mol/l:
40,0 g NaOH (Nummer 3.5) in Wasser lösen und mit Wasser (Nummer 3.1) auf 1 l auffüllen.
3.11. Salzsäure, c = 6 mol/l:
492 ml HCl (Nummer 3.7) werden mit Wasser auf 1 l aufgefüllt.
3.12. Salzsäure, c = 1 mol/l:
82 ml HCl (Nummer 3.7) werden mit Wasser auf 1 l aufgefüllt.
3.13. Salzsäure, c = 0,1 mol/l:
8,2 ml HCl (Nummer 3.7) werden mit Wasser auf 1 l aufgefüllt.
3.14. Orthophosphorsäure, c = 0,5 mol/l:
34 ml Orthophosphorsäure (Nummer 3.6) werden mit Wasser (Nummer 3.1) auf 1 l aufgefüllt.
3.15. Konzentrierte Tryptophanlösung (Nummer 3.2), c = 2,50 μmol/ml:
0,2553 g Tryptophan (Nummer 3.2) werden in einem 500-ml-Messkolben in Salzsäure (Nummer 3.13) gelöst und mit Salzsäure (Nummer 3.13) zur Marke aufgefüllt. Bei -18 °C höchstens 4 Wochen aufbewahren.
3.16. Konzentrierte interne Standardlösung, c = 2,50 μmol/ml:
0,2728 g α-Methyl-Tryptophan (Nummer 3.3) werden in einem 500-ml-Messkolben in Salzsäure (Nummer 3.13) gelöst und mit Salzsäure (Nummer 3.13) zur Marke aufgefüllt. Bei -18 °C höchstens 4 Wochen aufbewahren.
3.17. Kalibrierstandardlösung von Tryptophan und internem Standard:
2,00 ml konzentrierte Tryptophanlösung (Nummer 3.15) und 2,00 ml konzentrierte interne Standardlösung (α-Methyl-Tryptophan) (Nummer 3.16) werden mit Wasser (Nummer 3.1) und Methanol (Nummer 3.8) auf etwa dasselbe Volumen und etwa dieselbe Methanolkonzentration (10 bis 30 %) wie das fertige Hydrolysat verdünnt.
Diese Lösung muss vor Gebrauch frisch hergestellt werden.
Während der Zubereitung vor direktem Sonnenlicht schützen.
3.18. Essigsäure.
3.19. 1,1,1-Trichlor-2-methyl-2-propanol.
3.20. Ethanolamin, w (Massenanteil) > 98 %.
3.21. Lösung von 1 g 1,1,1-Trichlor-2-methyl-2-propanol (Nummer 3.19) in 100 ml Methanol (Nummer 3.8).
3.22. Mobile Phase für die HPLC: 3,00 g Essigsäure (Nummer 3.18) + 900 ml Wasser (Nummer 3.1) + 50,0 ml Lösung (Nummer 3.21) von 1,1,1-Trichlor-2-methyl-2-propanol (Nummer 3.19) in Methanol (Nummer 3.8) (1 g/100 ml). Den pH-Wert mit Ethanolamin (Nummer 3.20) auf 5,0 einstellen. Mit Wasser (Nummer 3.1) auf 1 l auffüllen.
4. Geräte
4.1. HPLC-Einrichtung mit Fluoreszenzdetektor.
4.2. HPLC-Trennsäule, 125 × 4 mm, C18, 3 μm Korngröße, oder vergleichbare Säule.
4.3. pH-Meter.
4.4. Polypropylen-Kolben, 125 ml, Weithals mit Schraubverschluss.
4.5. Membranfilter, 0,45 μm Porengröße.
4.6. Autoklav, 110 (± 2) °C, 1,4 (± 0,1) bar.
4.7. Mechanisches Schüttelgerät oder Magnetrührer.
4.8. Vortex-Schüttelgerät.
5. Verfahren
5.1. Vorbereitung der Proben
Die Probe wird so fein zermahlen, dass sie ein Sieb mit 0,5 mm Maschenweite passieren kann. Proben mit hohem Feuchtigkeitsgehalt müssen vor dem Zermahlen entweder bei einer Temperatur von höchstens 50 °C luftgetrocknet oder aber gefriergetrocknet werden. Proben mit hohem Fettgehalt sind vor dem Zermahlen mit Petrolether (Nummer 3.9) zu extrahieren.
5.2. Bestimmung des Gehalts an freiem Tryptophan (Extrakt)
Eine geeignete Menge (1 bis 5 g) der vorbereiteten Probe (Nummer 5.1) auf 1 mg genau in einen Erlenmeyerkolben einwiegen. 100,0 ml Salzsäure (Nummer 3.13) und 5,00 ml konzentrierte interne Standardlösung (Nummer 3.16) zugeben. Mit einem mechanischen Schüttler oder einem Magnetrührer (Nummer 4.7) 60 min lang schütteln bzw. mischen. Absetzen lassen und 10,0 ml der überstehenden Lösung in ein Becherglas pipettieren. 5 ml Orthophosphorsäure (Nummer 3.14) zugeben. Der pH-Wert wird mit Natriumhydroxidlösung (Nummer 3.10) auf 3 eingestellt. Ausreichend Methanol (Nummer 3.8) für eine Methanolkonzentration von 10 bis 30 % im Endvolumen zugeben. In einen Messkolben mit ausreichendem Volumen überführen und mit Wasser auf das für die Chromatografie notwendige Volumen verdünnen (entspricht etwa dem Volumen der Kalibrierstandardlösung (Nummer 3.17)).
Einige ml der Lösung werden vor der Einspritzung in die HPLC-Säule durch einen 0,45-μm-Membranfilter (Nummer 4.5) filtriert. Die Chromatografie gemäß Nummer 5.4 durchführen.
Standardlösung und Extrakte sind vor direktem Sonnenlicht zu schützen. Falls es nicht möglich ist, die Extrakte am selben Tag zu analysieren, können sie bei 5 °C maximal 3 Tage aufbewahrt werden.
5.3. Bestimmung des Gehalts an Gesamttryptophan (Hydrolysat)
0,1 bis 1 g der vorbereiteten Probe (Nummer 5.1) werden auf 0,2 mg genau in den Polypropylenkolben (Nummer 4.4) eingewogen. Die Einwaage muss einen Stickstoffgehalt von ca. 10 mg aufweisen. 8,4 g Bariumhydroxid-Octahydrat (Nummer 3.4) und 10 ml Wasser zugeben. Mithilfe eines Vortex-Schüttelgeräts (Nummer 4.8) oder Magnetrührgeräts (Nummer 4.7) mischen. Den teflonbeschichteten Magneten in der Mischung lassen. Die Gefäßwände mit 4 ml Wasser abspülen. Schraubkappe aufsetzen und Kolben locker verschließen. In einen Autoklaven (Nummer 4.6) mit kochendem Wasser überführen und 30 bis 60 min lang dämpfen lassen. Den Autoklaven schließen und 20 h lang bei 110 (± 2) °C autoklavieren.
Vor dem Öffnen des Autoklaven ist die Temperatur auf knapp unter 100 °C zu senken. Um eine Kristallisation des Ba(OH)2·8H2O zu vermeiden, sind der warmen Mischung 30 ml Wasser mit Zimmertemperatur zuzugeben. Leicht schütteln oder rühren. 2,00 ml konzentrierte interne Standardlösung (α-Methyl-Tryptophan) (Nummer 3.16) zugeben. Die Gefäße im Wasser-/Eisbad 15 min lang kühlen.
Anschließend 5 ml Orthophosphorsäure (Nummer 3.14) zugeben. Das Gefäß im Kühlbad belassen und unter Rühren mit HCl (Nummer 3.11) neutralisieren; der pH-Wert wird mit HCl (Nummer 3.12) auf 3,0 eingestellt. Ausreichend Methanol für eine Methanolkonzentration von 10 bis 30 % im Endvolumen zugeben. In einen Messkolben mit ausreichendem Volumen überführen und mit Wasser auf das für die Chromatografie notwendige Volumen verdünnen (z.B. 100 ml). Die Zugabe von Methanol darf keine Präzipitation verursachen.
Einige ml der Lösung werden vor der Einspritzung in die HPLC-Säule durch einen 0,45-μm-Membranfilter (Nummer 4.5) filtriert. Die Chromatografie gemäß Nummer 5.4 durchführen.
Standardlösung und Extrakte sind vor direktem Sonnenlicht zu schützen. Falls es nicht möglich ist, die Hydrolysate am selben Tag zu analysieren, können sie bei 5 °C höchstens 3 Tage aufbewahrt werden.
5.4. HPLC-Bestimmung
Die folgenden Angaben für eine isokratische Trennung sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen (siehe auch Bemerkungen 9.1 und 9.2):
| HPLC-Trennsäule (Nummer 4.2): | 125 × 4 mm, C18, 3 μm Korngröße, oder vergleichbare Säule |
| Säulentemperatur: | Raumtemperatur |
| Mobile Phase (Nummer 3.22): | 3,00 g Essigsäure (Nummer 3.18) + 900 ml Wasser (Nummer 3.1) + 50,0 ml Lösung (Nummer 3.21) von 1,1,1-Trichlor-2-methyl-2-propanol (Nummer 3.19) in Methanol (Nummer 3.8) (1 g/100 ml). Den pH-Wert mit Ethanolamin (Nummer 3.20) auf 5,0 einstellen. Mit Wasser (Nummer 3.1) auf 1 l auffüllen. |
| Durchflussrate: | 1 ml/min |
| Gesamtlaufzeit: | ca. 34 min |
| Detektionswellenlänge: | Anregung: 280 nm, Emission: 356 nm |
| Einspritzvolumen: | 20 μl |
6. Berechnung der Ergebnisse
Die Menge von Tryptophan (X) in g je 100 g Probe wird wie folgt berechnet:
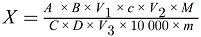
| A | = | Peakfläche des internen Standards; Kalibrierstandardlösung (Nummer 3.17) |
| B | = | Peakfläche von Tryptophan, Extrakt (Nummer 5.2) oder Hydrolysat (Nummer 5.3) |
| V1 | = | Volumen der konzentrierten Tryptophanlösung (Nummer 3.15), das der Kalibrierlösung (Nummer 3.17) zugegeben wurde, in ml (2 ml) |
| c | = | Konzentration der konzentrierten Tryptophanlösung (Nummer 3.15), die der Kalibrierlösung (Nummer 3.17) zugegeben wurde, in μmol/ml (= 2,50) |
| V2 | = | Volumen der konzentrierten internen Standardlösung (Nummer 3.16), das bei der Extraktion (Nummer 5.2) (= 5,00 ml) oder dem Hydrolysat (Nummer 5.3) (= 2,00 ml) zugegeben wurde, in ml |
| C | = | Peakfläche des internen Standards, Extrakt (Nummer 5.2) oder Hydrolysat (Nummer 5.3) |
| D | = | Peakfläche von Tryptophan, Kalibrierstandardlösung (Nummer 3.17) |
| V3 | = | Volumen der konzentrierten internen Standardlösung (Nummer 3.16), das der Kalibrierstandardlösung (Nummer 3.17) zugegeben wurde, in ml (2,00 ml) |
| m | = | Probeneinwaage (korrigiert auf Originalgewicht, falls getrocknet und/oder entfettet), in g |
| M | = | Molmasse von Tryptophan (= 204,23 g/mol) |
7. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 10 % des höheren Werts nicht überschreiten.
8. Ergebnisse eines Ringversuchs
Es wurde ein EU-Ringversuch (4. Vergleichstest) durchgeführt, bei dem 3 Proben von bis zu 12 Laboratorien analysiert wurden, um die Hydrolysemethode zu zertifizieren. Jede Probe wurde mehrfach (5-mal) analysiert. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst.
| Probe 1 Schweinefutter | Probe 2 Schweinefutter mit Zusatz von L-Tryptophan | Probe 3 Kraftfutter für Schweine | |||||||||||||||||
| L | 12 | 12 | 12 | ||||||||||||||||
| n Mittelwert [g/kg] | 50 2,42 | 55 3,40 | 50 4,22 | ||||||||||||||||
| sr [g/kg] | 0,05 | 0,05 | 0,08 | ||||||||||||||||
| r [g/kg] | 0,14 | 0,14 | 0,22 | ||||||||||||||||
| VKr [%] | 1,9 | 1,6 | 1,9 | ||||||||||||||||
| SR [g/kg] | 0,15 | 0,20 | 0,09 | ||||||||||||||||
| R [g/kg] | 0,42 | 0,56 | 0,25 | ||||||||||||||||
| VKR [%] | 6,3 | 6,0 | 2,2 | ||||||||||||||||
| |||||||||||||||||||
Es wurde ein weiterer EU-Ringversuch (3. Vergleichstest) durchgeführt, bei dem 2 Proben von bis zu 13 Laboratorien analysiert wurden, um die Methode zur Extraktion von freiem Tryptophan zu zertifizieren. Jede Probe wurde mehrfach (5-mal) analysiert. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst.
| Probe 4 Mischung aus Weizen und Soja | Probe 5 Mischung aus Weizen und Soja (= Probe 4) mit Tryptophan-Zusatz (0,457 g/kg) | |||||||||||||||||
| L n | 12 55 | 12 60 | ||||||||||||||||
| Mittelwert [g/kg] | 0,391 | 0,931 | ||||||||||||||||
| sr [g/kg] | 0,005 | 0,012 | ||||||||||||||||
| r [g/kg] | 0,014 | 0,034 | ||||||||||||||||
| VKr [%] | 1,34 | 1,34 | ||||||||||||||||
| SR [g/kg] | 0,018 | 0,048 | ||||||||||||||||
| R [g/kg] | 0,050 | 0,134 | ||||||||||||||||
| VKR [%] | 4,71 | 5,11 | ||||||||||||||||
| ||||||||||||||||||
Es wurde ein weiterer EU-Vergleichstest durchgeführt, bei dem 4 Proben von bis zu 7 Laboratorien analysiert wurden, um die Tryptophan-Hydrolyse zu zertifizieren. Die Ergebnisse sind nachstehend zusammengefasst. Jede Probe wurde mehrfach (5-mal) analysiert.
| Probe 1 Schweinemisch- futtermittel (CRM 117) | Probe 2 Fischmehl mit geringem Fettgehalt (CRM 118) | Probe 3 Sojamehl (CRM 119) | Probe 4 Magermilchpulver (CRM 120) | |||||||||||||||||
| L | 7 | 7 | 7 | 7 | ||||||||||||||||
| n | 25 | 30 | 30 | 30 | ||||||||||||||||
| Mittelwert [g/kg] | 2,064 | 8,801 | 6,882 | 5,236 | ||||||||||||||||
| sr [g/kg] | 0,021 | 0,101 | 0,089 | 0,040 | ||||||||||||||||
| r [g/kg] | 0,059 | 0,283 | 0,249 | 0,112 | ||||||||||||||||
| VKr [%] | 1,04 | 1,15 | 1,30 | 0,76 | ||||||||||||||||
| SR [g/kg] | 0,031 | 0,413 | 0,283 | 0,221 | ||||||||||||||||
| R [g/kg] | 0,087 | 1,156 | 0,792 | 0,619 | ||||||||||||||||
| VKR [%] | 1,48 | 4,69 | 4,11 | 4,22 | ||||||||||||||||
| ||||||||||||||||||||
9. Bemerkungen
9.1. Mit den folgenden besonderen Chromatografiebedingungen kann eine bessere Trennung von Tryptophan und α-Methyl-Tryptophan erreicht werden.
Isokratische Trennung, gefolgt von der Reinigung der Gradientensäule:
| HPLC-Trennsäule: | 125 × 4 mm, C18, 5 μm Korngröße, oder vergleichbare Säule | |
| Säulentemperatur: | 32 °C | |
| Mobile Phase: | A: 0,01 mol/l KH2PO4/Methanol, 95 + 5 (V+V). | |
| B: Methanol. | ||
| Gradientenprogramm: | 0 min 100 % A | 0 % B |
| 15 min 100 % A | 0 % B | |
| 17 min 60 % A | 40 % B | |
| 19 min 60 % A | 40 % B | |
| 21 min 100 % A | 0 % B | |
| 33 min 100 % A | 0 % B | |
| Durchflussrate: | 1,2 ml/min | |
| Gesamtlaufzeit: | ca. 33 min | |
9.2. Die Durchführung der Chromatografie variiert je nach Art der HPLC und der verwendeten Säulenpackung. Das System muss so gewählt werden, dass eine Grundlinientrennung zwischen Tryptophan und dem internen Standard möglich ist. Die Abbauprodukte müssen deutlich von Tryptophan und dem internen Standard getrennt werden. Zur Untersuchung der Grundlinie unter dem internen Standard auf Verunreinigungen sind Hydrolysate ohne internen Standard zu analysieren. Die Laufzeit muss lang genug sein, dass alle Abbauprodukte eluiert werden, andernfalls können späte Elutionspeaks anschließende Chromatografiedurchgänge beeinträchtigen.
Im Betriebsbereich muss das Chromatografiesystem eine lineare Reaktion ergeben. Die lineare Reaktion ist bei einer konstanten (der normalen) Konzentration des internen Standards und unterschiedlichen Tryptophankonzentrationen zu messen. Die Größe des Tryptophan- und des internen Standardpeaks müssen sich innerhalb des linearen Bereichs des HPLC-/Fluoreszenzsystems befinden. Sollten der Tryptophan- und/oder der interne Standardpeak/die internen Standardpeaks zu klein oder zu hoch sein, ist die Analyse mit einer anderen Probengröße und/oder einem anderen Endvolumen zu wiederholen.
9.3. Bariumhydroxid
Älteres Bariumhydroxid ist schwerer löslich. Dies kann zur Folge haben, dass die Lösung für die HPLC-Bestimmung nicht klar ist und zu niedrigen Tryptophan-Werten führen kann.
G. Bestimmung des Gehalts an Rohölen und -Fetten
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Rohöl- und Rohfettgehalt von Futtermitteln bestimmen.
Je nach Art und Zusammensetzung des Futtermittels sowie in Abhängigkeit vom Zweck der Untersuchung ist eines der beiden nachstehend beschriebenen Verfahren anzuwenden.
Zur Bestimmung des Rohöl- und Rohfettgehalts von Ölsaaten und Ölfrüchten sowie von Futtermitteln, bei denen der Rohöl-/Rohfettgehalt 15 % übersteigt, sollte die Extraktion mithilfe des Verfahrens A und die erneute Extraktion mithilfe des Verfahrens B (Nummer 5.3) durchgeführt werden.
1.1. Verfahren A - Direkt extrahierbare Rohöle und Rohfette
Das Verfahren ist anzuwenden bei Futtermittel-Ausgangserzeugnissen pflanzlichen Ursprungs mit Ausnahme derjenigen, die in den Anwendungsbereich des Verfahrens B fallen.
1.2. Verfahren B - Gesamtgehalt an Rohölen und Rohfetten
Das Verfahren ist anzuwenden bei Futtermittel-Ausgangserzeugnissen tierischen Ursprungs und bei allen Mischfuttermitteln. Es ist außerdem bei allen Erzeugnissen anzuwenden, aus denen Öle und Fette ohne vorherige Hydrolyse nicht vollständig extrahiert werden können (z.B. Kleber, Hefen, Kartoffeleiweiß und Erzeugnisse, die Verfahren unterzogen wurden wie Extrudieren, Flockieren und Erhitzen).
1.3. Auswertung der Ergebnisse
In allen Fällen, in denen mit Verfahren B ein höheres Ergebnis erzielt wird als mit Verfahren A, gilt das mit Verfahren B erhaltene Ergebnis als der richtige Wert.
2. Prinzip
2.1. Verfahren A
Die Probe wird mit Petrolether extrahiert. Das Lösungsmittel wird abdestilliert und der Rückstand getrocknet und gewogen.
2.2. Verfahren B
Die Probe wird unter Erhitzen mit Salzsäure behandelt. Die Mischung wird abgekühlt und filtriert. Der gewaschene und getrocknete Rückstand wird nach Verfahren A weiterbehandelt.
3. Reagenzien
3.1. Petrolether, Siedeintervall: 40 bis 60 °C. Die Bromzahl muss weniger als 1 und der Abdampfrückstand weniger als 2 mg/100 ml betragen.
3.2. Natriumsulfat, wasserfrei.
3.3. Salzsäure, c = 3 mol/l.
3.4. Filterhilfsmittel, z.B. Kieselgur, Hyflo-Supercel.
4. Geräte
4.1. Extraktionsapparat: Sofern das Gerät mit einem Siphon (Soxhletapparat) ausgestattet ist, muss die Rückflussmenge so bemessen sein, dass das Lösungsmittel mindestens 10-mal in der Stunde abläuft. Wenn es sich um ein Gerät ohne Siphon handelt, muss die Rückflussmenge etwa 10 ml/min betragen.
4.2. Extraktionshülsen: Diese müssen frei sein von petroletherlöslichen Stoffen und eine Porosität besitzen, die den Anforderungen nach Nummer 4.1 genügt.
4.3. Trockenschrank: Vakuumtrockenschrank, eingestellt auf 75 °C (± 3 °C,) oder Lufttrockenschrank, eingestellt auf 100 °C (± 3 °C).
5. Verfahren
5.1. Verfahren A (siehe Bemerkung 8.1)
Von der Probe werden 5 g auf 1 mg genau abgewogen, dann in eine Extraktionshülse (Nummer 4.2) überführt und mit einem fettfreien Wattebausch abgedeckt.
Die Hülse wird in einen Extraktionsapparat (Nummer 4.1) eingesetzt und 6 h lang mit Petrolether (Nummer 3.1) extrahiert. Der Petroletherextrakt wird in einem trockenen, mit einigen Körnern Bimsstein 6 versehenen, tarierten Kolben aufgefangen.
Nach beendeter Extraktion wird das Lösungsmittel abdestilliert. Anschließend wird der Rückstand mit Kolben 1,5 h im Trockenschrank (Nummer 4.3) getrocknet und nach dem Abkühlen in einem Exsikkator gewogen. Durch eine zweite Trocknung von 30 min Dauer ist zu prüfen, ob das Gewicht der Öle und Fette konstant geblieben ist (der Gewichtsverlust zwischen 2 aufeinanderfolgenden Wägungen darf 1 mg nicht überschreiten).
5.2. Verfahren B
Von der Probe werden 2,5 g auf 1 mg genau abgewogen (siehe Bemerkung 8.2) und in ein 400-ml-Becherglas oder einen 300-ml-Erlenmeyerkolben gebracht. Anschließend werden 100 ml Salzsäure (Nummer 3.3) und einige Körner Bimsstein hinzugefügt. Das Becherglas wird mit einem Uhrglas abgedeckt, bzw. dem Erlenmeyerkolben wird ein Rückflusskühler aufgesetzt. Das Gemisch wird auf kleiner Flamme oder auf einer Heizplatte bis zum Siedepunkt erhitzt und 1 h lang schwach sieden gelassen. Es ist zu verhindern, dass das Material sich an den Wänden des Gefäßes festsetzt.
Dann wird abgekühlt und so viel vom Filterhilfsmittel (Nummer 3.4) zugesetzt, dass beim Filtrieren kein Öl- bzw. Fettverlust eintritt. Filtriert wird unter Verwendung eines feuchten, fettfreien doppelten Filterpapiers. Der Rückstand wird bis zur neutralen Reaktion mit kaltem Wasser gewaschen. Danach ist zu überprüfen, dass das Filtrat keine Öle und Fette mehr enthält. Bei Vorhandensein von Ölen oder Fetten muss vor der Hydrolyse eine Extraktion der Probe mit Petrolether nach Verfahren A vorgenommen werden.
Das doppelte Filterpapier mit dem Rückstand ist auf ein Uhrglas zu legen und ca. 1,5 h lang bei 100 °C (± 3 °C) im Lufttrockenschrank (Nummer 4.3) zu trocknen.
Das doppelte Filterpapier mit dem trockenen Rückstand wird in eine Extraktionshülse (Nummer 4.2) überführt und mit einem fettfreien Wattebausch abgedeckt. Die Hülse wird in einen Extraktionsapparat (Nummer 4.1) eingesetzt. Dann wird, wie unter Nummer 5.1 Absätze 2 und 3 beschrieben, weiterverfahren.
5.3. Verfahren A und erneute Extraktion mithilfe des Verfahrens B
Zur Bestimmung des Rohöl- und Rohfettgehalts von Ölsaaten und Ölfrüchten sowie von Futtermitteln, bei denen der Rohöl-/Rohfettgehalt 15 % übersteigt, sollte die Extraktion mithilfe des Verfahrens A und die erneute Extraktion mithilfe des Verfahrens B durchgeführt werden.
Dies bedeutet, dass nach der Extraktion mit Petrolether (Verfahren A) der Rückstand oder ein Teil des Rückstands mit Salzsäure erneut extrahiert wird (Verfahren B). Der Rohöl- und Rohfettgehalt ist die Summe der Ergebnisse der Verfahren A und B.
6. Angabe der Ergebnisse
Das Gewicht des Rückstands wird als Prozentsatz der Probe ausgedrückt.
7. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen eines Analytikers bei ein und derselben Probe darf die folgenden Werte nicht überschreiten:
8. Bemerkungen
8.1. Bei Erzeugnissen mit hohem Öl- und Fettgehalt, die schwer zu zerkleinern sind oder sich zur Entnahme einer reduzierten homogenen Analysenprobe nicht eignen, ist folgendermaßen zu verfahren:
Von der Probe werden 20 g auf 1 mg genau abgewogen und mit 10 g oder mehr wasserfreiem Natriumsulfat (Nummer 3.2) gemischt. Dann wird mit Petrolether (Nummer 3.1) extrahiert, wie unter Nummer 5.1 beschrieben. Der dabei aufgefangene Extrakt wird mit Petrolether (Nummer 3.1) auf 500 ml aufgefüllt und gemischt. Von der Lösung werden 50 ml entnommen und in einen kleinen, trockenen, mit Bimssteinkörnchen versehenen und tarierten Kolben gebracht. Das Lösungsmittel wird abdestilliert und dann wird, wie unter Nummer 5.1 letzter Absatz beschrieben, getrocknet und weiterverfahren.
Der Extraktionsrückstand in der Hülse wird vom Lösungsmittel befreit, auf 1 mm zerkleinert und wieder zurück in die Extraktionshülse gebracht (ohne Zugabe von Natriumsulfat). Dann wird, wie unter Nummer 5.1 Absätze 2 und 3 beschrieben, weiterverfahren.
Der Gehalt an Ölen und Fetten, ausgedrückt als Prozentsatz der Probe, wird nach folgender Formel berechnet:
(10 m1 + m2) × 5
wobei:
| m1 = | Gewicht des Rückstands in g nach der ersten Extraktion (aliquoter Teil des Extrakts), |
| m2 = | Gewicht des Rückstands in g nach der zweiten Extraktion. |
8.2. Bei einigen Erzeugnissen (z.B. öl- und fettarmen Erzeugnissen) kann die Einwaage erhöht werden.
8.3. Heimtierfutter mit hohem Wassergehalt muss vor der Hydrolyse und Extraktion nach Verfahren B möglicherweise mit wasserfreiem Natriumsulfat gemischt werden.
8.4. Bei dem Verfahren nach Nummer 5.2 kann die Verwendung von heißem statt kaltem Wasser zum Waschen des Rückstands nach der Filtration möglicherweise wirksamer sein.
8.5. Die Trocknungszeit von 1,5 h muss bei einigen Futtermitteln möglicherweise verlängert werden. Übermäßiges Trocknen ist zu vermeiden, da dies zu niedrigen Ergebnissen führen kann. Es kann auch ein Mikrowellengerät verwendet werden.
H. Bestimmung des Rohfasergehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an säure- und alkaliunlöslichen, fettfreien organischen Bestandteilen, herkömmlicherweise als Rohfaser bezeichnet, in Futtermitteln bestimmen.
Die Methode ist nicht anwendbar in Bezug auf Lignozellulose und Pflanzenkohle (zu feine Partikel).
2. Prinzip
Die gegebenenfalls entfettete Probe wird nacheinander mit kochender Schwefelsäurelösung und kochender Kaliumhydroxidlösung definierter Konzentrationen behandelt. Der Rückstand wird durch Filtration auf einem gesinterten Glasfilter getrennt, gewaschen, getrocknet, gewogen und bei 475 bis 500 °C verascht. Der Gewichtsverlust bei dieser Veraschung entspricht der Rohfaser der Einwaage.
3. Reagenzien
3.1. Schwefelsäure, c = 0,13 mol/l.
3.2. Antischaummittel (z.B. n-Oktanol).
3.3. Filterhilfsmittel (Celite 545 oder gleichwertiges Mittel), 4 h lang auf 500 °C erhitzt (8.6).
3.4. Aceton.
3.5. Petrolether, Siedeintervall: 40 bis 60 °C.
3.6. Salzsäure, c = 0,5 mol/l.
3.7. Kaliumhydroxidlösung, c = 0,23 mol/l.
4. Geräte
4.1. Heizvorrichtung für den Aufschluss mit Schwefelsäure und Kaliumhydroxidlösung, ausgestattet mit einer Halterung für den Glasfiltertiegel (Nummer 4.2) und einem Abflussrohr mit Hahn zum Flüssigkeitsablauf, für den Vakuumanschluss und, sofern möglich, auch mit einem Anschluss für die Zufuhr von Druckluft. Vor der täglichen Inbetriebnahme muss die gesamte Apparatur mit Wasser 5 min erhitzt werden.
4.2. Glasfiltertiegel mit eingeschmolzenem gesintertem Glasfilter (Porengröße 40 bis 90 μm). Vor dem erstmaligen Gebrauch wird der Tiegel einige Minuten bei 500 °C geglüht und dann abkühlen gelassen (Nummer 8.6).
4.3. Siedezylinder (mindestens 270 ml) mit einem Rückflusskühler.
4.4. Trockenschrank mit Thermostat.
4.5. Muffelofen mit Thermostat.
4.6. Extraktionsvorrichtung mit einer Halterung für den Glasfiltertiegel (Nummer 4.2) und einem Abflussrohr mit Hahn für den Flüssigkeitsablauf und den Vakuumanschluss.
4.7. Verbindungsringe zur Verbindung von Heizvorrichtung (Nummer 4.1), Filtertiegel (Nummer 4.2) und Siedezylinder (Nummer 4.3), Verbindungsringe zur Verbindung von Kaltextraktionsvorrichtung (Nummer 4.6) und Filtertiegel.
5. Verfahren
Von der vorbereiteten Probe werden 1 g auf 1 mg genau in den Glasfiltertiegel (Nummer 4.2) eingewogen (siehe Bemerkungen 9.1, 9.2 und 9.3), und es wird 1 g Filterhilfsmittel (Nummer 3.3) hinzugefügt.
Der Glasfiltertiegel (Nummer 4.2) wird in die Heizvorrichtung (Nummer 4.1) eingesetzt und mit dem Siedezylinder (Nummer 4.3) verbunden. 150 ml auf Siedetemperatur erhitzte Schwefelsäure (Nummer 3.1) werden in den mit dem Tiegel verbundenen Siedezylinder überführt, und es werden erforderlichenfalls einige Tropfen Antischaummittel (Nummer 3.2) hinzugefügt.
Die Flüssigkeit wird innerhalb von 5 ± 2 min zum Sieden erhitzt und genau 30 min lang im kräftigen Sieden gehalten.
Der Hahn im Abflussrohr (Nummer 4.1) wird geöffnet und die Schwefelsäure mithilfe von Vakuum durch den Glasfiltertiegel abgesaugt. Der Filterrückstand wird 3-mal mit je 30 ml kochendem Wasser gewaschen. Nach jedem Waschvorgang ist der Rückstand trocken zu saugen.
Der Auslaufhahn wird geschlossen, und es werden 150 ml siedende Kaliumhydroxidlösung (Nummer 3.7) und einige Tropfen Antischaummittel (Nummer 3.2) in den mit dem Siedezylinder verbundenen Glasfiltertiegel gegeben. Die Flüssigkeit wird innerhalb von 5 ± 2 min zum Sieden erhitzt und genau 30 min lang im kräftigen Sieden gehalten. Nach dem Filtern wird das Waschen des Rückstands in der gleichen Weise durchgeführt wie nach der Behandlung mit Schwefelsäure.
Nach dem letzten Waschen wird der Rückstand trocken gesaugt und der Tiegel mit Inhalt vom Siedezylinder gelöst und an die Kaltextraktionsvorrichtung (Nummer 4.6) angeschlossen. Unter Anlegen von Vakuum wird der Rückstand im Tiegel 3-mal mit je 25 ml Aceton (Nummer 3.4) gewaschen, wobei der Rückstand nach jedem Waschvorgang trocken zu saugen ist.
Der Filtertiegel mit Inhalt wird im Trockenschrank bei 130 °C bis zur Massekonstanz getrocknet, in einem Exsikkator abgekühlt und anschließend rasch gewogen. Danach wird der Filtertiegel mit Inhalt in einen Muffelofen gebracht und mindestens 30 min lang bei einer Temperatur von 475 bis 500 °C bis zur Massekonstanz verascht (der Gewichtsverlust bei 2 aufeinanderfolgenden Wägungen darf 2 mg nicht überschreiten).
Nach dem Erhitzen wird der Tiegel zunächst im Muffelofen und dann im Exsikkator abgekühlt und anschließend gewogen.
Es wird ein Blindversuch ohne Probe durchgeführt. Der beim Veraschen auftretende Gewichtsverlust darf 4 mg nicht überschreiten.
6. Berechnung der Ergebnisse
Der Gehalt an Rohfaser als Prozentsatz der Probe wird nach folgender Formel berechnet:
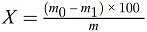
wobei:
| m = | Einwaage in g, |
| m0 = | Gewichtsverlust nach dem Veraschen während der Bestimmung, in g, |
| m1 = | Gewichtsverlust nach dem Veraschen während des Blindversuchs, in g. |
7. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf die folgenden Werte nicht überschreiten:
8. Vergleichbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe in unterschiedlichen Laboratorien darf die folgenden Werte nicht überschreiten:
9. Bemerkungen
9.1. Futtermittel, die mehr als 10 % Rohfett enthalten, müssen vor der Analyse mit Petrolether (Nummer 3.5) entfettet werden. Dazu wird der Glasfiltertiegel (Nummer 4.2) mit Inhalt an die Kaltextraktionsvorrichtung (Nummer 4.6) angeschlossen und unter Anlegen von Vakuum 3-mal mit je 30 ml Petrolether gewaschen, wobei sichergestellt wird, dass der Rückstand trocken ist. Der Tiegel mit Inhalt wird an die Heizvorrichtung (Nummer 4.1) angeschlossen. Danach ist gemäß Nummer 5 weiterzuverfahren.
9.2. Futtermittel, die Fette enthalten, welche nicht direkt mit Petrolether (Nummer 3.5) extrahiert werden können, müssen, wie unter Nummer 8.1 angegeben, entfettet werden und nach dem Sieden mit Säure ein weiteres Mal entfettet werden. Nach dem Sieden mit Säure und dem anschließenden Waschvorgang wird der Tiegel mit Inhalt an die Kaltextraktionsvorrichtung (Nummer 4.6) angeschlossen und 3-mal mit je 30 ml Aceton und danach weitere 3-mal mit je 30 ml Petrolether entfettet. Der Filtertiegel wird mithilfe von Vakuum trocken gesaugt und die Analyse wird, wie unter Nummer 5 beschrieben, fortgesetzt, beginnend mit der Behandlung mit Kaliumhydroxidlösung.
9.3. Bei Futtermitteln, die mehr als 5 % Carbonate, ausgedrückt als Calciumcarbonat, enthalten, wird der Tiegel (Nummer 4.2) mit der eingewogenen Probemenge an die Heizvorrichtung (Nummer 4.1) angeschlossen. Die Probe wird 3-mal mit je 30 ml Salzsäure (Nummer 3.6) gewaschen. Nach jeder Zugabe wird die Probe vor dem Absaugen etwa 1 min lang stehen gelassen. Anschließend wird 1-mal mit 30 ml Wasser gewaschen. Danach ist wie unter Nummer 5 angegeben weiterzuverfahren.
9.4. Wenn ein Gerät benutzt wird, bei dem mehrere Glasfiltertiegel an derselben Heizvorrichtung gleichzeitig befestigt sind, dürfen in derselben Untersuchungsreihe keine 2 Einzelbestimmungen an ein und derselben Probe vorgenommen werden.
9.5. Wenn nach dem Sieden mit Säure bzw. Lauge Schwierigkeiten bei der Filtration auftreten, wird der Heizvorrichtung durch das Auslassrohr Druckluft zugeführt und anschließend die Filtration fortgesetzt.
9.6. Die Veraschungstemperatur darf 500 °C nicht überschreiten, um die Haltbarkeit der Glasfiltertiegel zu verlängern. Beim Erhitzen und Abkühlen sind vor allem übermäßige Temperatursprüngezu vermeiden.
I. Bestimmung des Zuckergehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an reduzierenden Zuckern und an Gesamtzucker nach Inversion, ausgedrückt als Glucose oder gegebenenfalls nach Multiplikation mit dem Faktor 0,95 als Saccharose, bestimmen. Sie wird bei Mischfuttermitteln angewendet. Für andere Futtermittel sind besondere Verfahren vorgesehen. Gegebenenfalls muss der Gehalt an Lactose getrennt bestimmt und dieses Ergebnis bei der Berechnung berücksichtigt werden.
Die Methode ist anzuwenden, um den Zuckergehalt für die Berechnung des Energiegehalts des Futtermittels zu bestimmen.
Ist der Zuckergehalt für andere Zwecke zu bestimmen, können andere Analysemethoden angewendet werden.
2. Prinzip
Die Zucker werden in verdünntem Ethanol gelöst; die Lösung wird mit den Lösungen Carrez I und II geklärt. Nach dem Verdunsten des Ethanols werden vor und nach der Inversion die Bestimmungen nach der Luff-Schoorl-Methode durchgeführt.
3. Reagenzien
3.1. Ethanollösung (Volumenkonzentration = 40 %), Dichte: 0,948 g/ml bei 20 °C, auf den Umschlagspunkt von Phenolphthalein eingestellt.
3.2. Carrez-Lösung I: 21,9 g Zinkacetat, Zn (CH3COO)2·2H2O, und 3 g Eisessig werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.3. Carrez-Lösung II: 10,6 g Kaliumhexacyanoferrat(II), K4Fe(CN)6·3H2O, werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.4. Methylorangelösung (Massenkonzentration = 0,1 %).
3.5. Salzsäure 4 mol/l.
3.6. Salzsäure 0,1 mol/l.
3.7. Natriumhydroxidlösung 0,1 mol/l.
3.8. Reagenz nach Luff-Schoorl:
Die Zitronensäurelösung (Nummer 3.8.2) unter vorsichtigem Rühren in die Natriumcarbonatlösung (Nummer 3.8.3) gießen. Nach Zugabe der Kupfersulfatlösung (Nummer 3.8.1) mit Wasser auf 1 l auffüllen. Über Nacht absetzen lassen und dann filtrieren.
Die Konzentration des so erhaltenen Reagenz (Cu 0,05 mol/l; Na2CO3 1 mol/l) prüfen, siehe Nummer 5.4 letzter Absatz. Der pH-Wert der Lösung muss bei etwa 9,4 liegen.
3.8.1. Kupfersulfatlösung: 25 g Kupfersulfat, CuSO4·5H2O, eisenfrei, werden in 100 ml Wasser gelöst.
3.8.2. Zitronensäurelösung: 50 g Zitronensäure, C6H8O7·Η2O werden in 50 ml Wasser gelöst.
3.8.3. Natriumcarbonatlösung: 143,8 g Natriumcarbonat, wasserfrei, werden in ca. 300 ml warmem Wasser gelöst. Abkühlen lassen.
3.9. Natriumthiosulfatlösung 0,1 mol/l.
3.10. Stärkelösung: Eine Aufschlämmung von 5 g löslicher Stärke in 30 ml Wasser wird zu 1 l siedendem Wasser hinzugefügt und 3 min lang im Sieden halten; dann wird abgekühlt und es werden gegebenenfalls 10 mg Quecksilberiodid als Konservierungsmittel hinzugefügt.
3.11. Schwefelsäure 3 mol/l.
3.12. Kaliumiodidlösung (Massenkonzentration = 30 %).
3.13. Bimssteinkörner, mit Salzsäure ausgekocht, mit Wasser gewaschen und getrocknet.
3.14. 3-Methylbutan-1-ol.
4. Geräte
Mechanisches Schüttelgerät: ca. 35 bis 40 min-1.
5. Verfahren
5.1. Extraktion der Probe
Von der Probe werden 2,5 g auf 1 mg genau in einen 250-ml-Messkolben eingewogen. Nach Zugabe von 200 ml Ethanol (Nummer 3.1) wird der Kolben 1 h lang im Schüttelgerät gemischt. Anschließend werden 5 ml Carrez-Lösung I (Nummer 3.2) hinzugefügt, und es wird ca. 30 s lang gerührt. Dann werden 5 ml Carrez-Lösung II (Nummer 3.3) hinzugefügt, und es wird nochmals 1 min lang gerührt; nun wird mit Ethanol (Nummer 3.1) zur Marke aufgefüllt, homogenisiert und filtriert. Vom Filtrat werden 200 ml abpipettiert und auf ungefähr die Hälfte des Volumens eingeengt, um den größten Teil des Ethanols zur Verdunstung zu bringen. Der Abdampfrückstand wird mit warmem Wasser in einen 200-ml-Messkolben übergespült, abgekühlt, mit Wasser zur Marke aufgefüllt, homogenisiert und, falls erforderlich, filtriert. Diese Lösung wird für die Bestimmung des Gehalts an reduzierenden Zuckern und nach Inversion zur Bestimmung des Gesamtzuckers verwendet.
5.2. Bestimmung des Gehalts an reduzierenden Zuckern
Eine Menge von höchstens 25 ml der Lösung, die weniger als 60 mg reduzierende Zucker, ausgedrückt als Glucose, enthält, wird abpipettiert, falls erforderlich mit destilliertem Wasser auf 25 ml aufgefüllt, und es wird der Gehalt an reduzierendem Zucker nach der Luff-Schoorl-Methode bestimmt. Das Ergebnis wird als Prozentsatz Glucose in der Probe ausgedrückt.
5.3. Bestimmung des Gehalts an Gesamtzucker nach Inversion
Von der Lösung werden 50 ml in einen 100-ml-Messkolben pipettiert. Es werden einige Tropfen Methylorangelösung (Nummer 3.4) hinzugefügt und dann wird vorsichtig unter ständigem Rühren Salzsäure (Nummer 3.5) bis zum eindeutigen Umschlag nach Rot hinzugegeben. Dann werden 15 ml Salzsäure (Nummer 3.6) hinzugefügt, und der Kolben wird 30 min lang in ein Bad mit kräftig siedendem Wasser gestellt. Es wird schnell auf etwa 20 °C abgekühlt und es werden 15 ml Natriumhydroxidlösung (Nummer 3.7) hinzugegeben. Nun wird mit Wasser auf 100 ml aufgefüllt und homogenisiert. Es wird eine Menge von höchstens 25 ml entnommen, die weniger als 60 mg reduzierende Zucker, ausgedrückt als Glucose, enthält. Falls erforderlich, wird mit destilliertem Wasser auf 25 ml aufgefüllt und der Gehalt an reduzierenden Zuckern nach der Luff-Schoorl-Methode bestimmt. Das Ergebnis wird als Prozentsatz Glucose oder gegebenenfalls nach Multiplikation mit dem Faktor 0,95 als Saccharose ausgedrückt.
5.4. Titration nach Luff-Schoorl
In einen 300-ml-Erlenmeyerkolben werden 25 ml Reagenz nach Luff-Schoorl (Nummer 3.8) pipettiert und anschließend genau 25 ml der geklärten Zuckerlösung hinzugefügt. Nach Zugabe von 2 Körnchen Bimsstein (Nummer 3.13) wird unter Schütteln mit der Hand über freier Flamme von mittlerer Höhe erhitzt, sodass die Flüssigkeit in etwa 2 min zum Sieden kommt. Anschließend wird der Erlenmeyerkolben sofort auf ein Drahtnetz mit einer Asbestscheibe, in die ein Loch von etwa 6 cm Durchmesser gestanzt wurde, gestellt; vorher wird unter dem Drahtnetz eine Flamme entzündet und so eingestellt, dass der Kolben nur am Boden erhitzt wird. Dann wird der Kolben mit einem Rückflusskühler verbunden. Von diesem Augenblick an wird der Kolben genau 10 min lang sieden gelassen. Anschließend wird er sofort in kaltem Wasser abgekühlt und nach etwa 5 min wird wie folgt titriert:
Der Flüssigkeit werden 10 ml Kaliumiodidlösung (Nummer 3.12) und unmittelbar danach, aber vorsichtig (wegen der Gefahr des übermäßigen Schäumens), 25 ml Schwefelsäure (Nummer 3.11) zugegeben. Dann wird mit Natriumthiosulfatlösung (Nummer 3.9) zunächst bis zum Auftreten einer mattgelben Farbe titriert und nach Zugabe von Stärkelösung (Nummer 3.10) als Indikator die Titration zu Ende geführt.
Die gleiche Titration wird in einer Mischung aus genau 25 ml Reagenz nach Luff-Schoorl (Nummer 3.8) und 25 ml Wasser nach Zugabe von 10 ml Kaliumiodidlösung (Nummer 3.12) und 25 ml Schwefelsäure (Nummer 3.11) durchgeführt, jedoch ohne vorheriges Erhitzen.
6. Berechnung der Ergebnisse
Aus der unten angeführten Tabelle wird die Menge Glucose in mg abgelesen, die der Differenz der Ergebnisse beider Titrationen, ausgedrückt in ml Natriumthiosulfatlösung (0,1 mol/l), entspricht. Das Ergebnis wird als Prozentsatz der Probe angegeben.
7. Sonderverfahren
7.1. Bei sehr stark melassehaltigen Futtermitteln und anderen wenig homogenen Futtermitteln werden 20 g in einen 1-l-Messkolben eingewogen, es werden 500 ml Wasser hinzugefügt und dann wird 1 h lang im Schüttelgerät gemischt. Danach wird - jedoch mit jeweils der 4-fachen Menge der Carrez-Lösungen I (Nummer 3.2) und II (Nummer 3.3) - wie unter Nummer 5.1 beschrieben geklärt. Anschließend wird mit Ethanol (Volumenkonzentration = 80 %) zur Marke aufgefüllt.
Die Lösung wird homogenisiert und filtriert. Das Ethanol wird, wie unter Nummer 5.1 beschrieben, entfernt. Bei Abwesenheit verkleisterter Stärke wird mit destilliertem Wasser zur Marke aufgefüllt.
7.2. Bei Melasse und Futtermittel-Ausgangserzeugnissen, die reich an Zucker, aber praktisch stärkefrei sind (Johannisbrot, Zuckerrübentrockenschnitzel usw.), werden 5 g in einen 250-ml-Messkolben eingewogen und 200 ml destilliertes Wasser hinzugefügt. Dann wird 1 h lang oder, falls erforderlich, länger im Schüttelgerät gemischt. Danach wird mit den Carrez-Lösungen I (Nummer 3.2) und II (Nummer 3.3), wie unter Nummer 5.1 beschrieben, geklärt und anschließend mit kaltem Wasser zur Marke aufgefüllt, homogenisiert und filtriert. Zur Bestimmung des Gesamtzuckergehalts wird, wie unter Nummer 5.3 beschrieben, weiterverfahren.
8. Bemerkungen
8.1. Es wird empfohlen, vor dem Erhitzen mit dem Luff-Schoorl-Reagenz (unabhängig vom Volumen) etwa 1 ml 3-Methylbutan-1-ol (Nummer 3.14) hinzuzufügen, um die Schaumbildung zu vermeiden.
8.2. Die Differenz zwischen dem Gehalt an Gesamtzucker nach Inversion, ausgedrückt als Glucose, und dem Gehalt an reduzierenden Zuckern, ausgedrückt als Glucose, ergibt nach Multiplikation mit dem Faktor 0,95 das Ergebnis als Prozentsatz Saccharose.
8.3. Zur Bestimmung des Gehalts an reduzierenden Zuckern, mit Ausnahme von Milchzucker (Lactose), gibt es 2 Möglichkeiten:
8.3.1. Für eine annähernde Berechnung wird der aus einer getrennten Bestimmung ermittelte Lactosegehalt mit 0,675 multipliziert und das Ergebnis von dem Gehalt an reduzierenden Zuckern abgezogen.
8.3.2. Für eine genaue Berechnung der reduzierenden Zucker (mit Ausnahme von Lactose) ist es notwendig, dass beiden endgültigen Bestimmungen die gleiche Menge der Einwaage zugrunde liegt. Die eine Bestimmung wird in einem Teil der nach Nummer 5.1. hergestellten Lösung durchgeführt, die zweite Bestimmung in einem Teil der Lösung, die bei der Bestimmung des Lactosegehalts mittels der für diesen Zweck vorgesehenen Methode (nach Vergärung der anderen Zuckerarten und Klärung) hergestellt wird.
In beiden Fällen wird der anwesende Zucker nach der Luff-Schoorl-Methode bestimmt und in mg Glucose berechnet. Diese beiden Werte werden voneinander subtrahiert und die Differenz wird als Prozentsatz der Probe ausgedrückt.
Beispiel
Die beiden abpipettierten Mengen entsprechen bei jeder Bestimmung einer Probeneinwaage von 250 mg.
Im ersten Fall werden 17 ml Natriumthiosulfatlösung 0,1 mol/l, entsprechend 44,2 mg Glucose, verbraucht; im zweiten Fall werden 11 ml, entsprechend 27,6 mg Glucose, verbraucht.
Die Differenz beträgt also 16,6 mg Glucose.
Der Gehalt an reduzierenden Zuckern (mit Ausnahme von Lactose), berechnet als Glucose, ist demnach
(4 × 16;6) / 10 = 6,64 %
Tabelle für 25 ml Reagenz nach Luff-Schoorl
ml Na2S2O3 0,1 mol/l, 2 min lang erhitzen, 10 min lang sieden
| Na2S2O3 0,1 mol/l | Glucose, Fructose, Invertzucker C6H12O6 | Lactose C12H22O11 | Na2S2O3 0,1 mol/l | ||
| ml | mg | Differenz | mg | Differenz | ml |
| 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 | 2,4 4,8 7,2 9,7 12,2 14,7 17,2 19,8 22,4 25,0 27,6 30,3 33,0 35,7 38,5 41,3 44,2 47,1 50,0 53,0 56,0 59,1 62,2 | 2,4 2,4 2,5 2,5 2,5 2,5 2,6 2,6 2,6 2,6 2,7 2,7 2,7 2,8 2,8 2,9 2,9 2,9 3,0 3,0 3,1 3,1 | 3,6 7,3 11,0 14,7 18,4 22,1 25,8 29,5 33,2 37,0 40,8 44,6 48,4 52,2 56,0 59,9 63,8 67,7 71,7 75,7 79,8 83,9 88,0 | 3,7 3,7 3,7 3,7 3,7 3,7 3,7 3,7 3,8 3,8 3,8 3,8 3,8 3,8 3,9 3,9 3,9 4,0 4,0 4,1 4,1 4,1 | 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |
J. Bestimmung des Lactosegehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Lactosegehalt von Futtermitteln bestimmen, die mehr als 0,5 % Lactose enthalten.
2. Prinzip
Die Zucker werden in Wasser gelöst. Die Lösung wird mit Hefe - Saccharomyces cerevisiae - vergoren, wobei die Lactose nicht angegriffen wird. Nach Klärung und Filtration wird der Gehalt an Lactose im Filtrat nach der Luff-Schoorl-Methode bestimmt.
3. Reagenzien
3.1. Saccharomyces-cerevisiae-Suspension: 25 g frische Hefe werden in 100 ml Wasser suspendiert. Im Kühlschrank ist die Suspension höchstens 1 Woche haltbar.
3.2. Carrez-Lösung I: 21,9 g Zinkacetat, Zn (CH3COO)2·2H2O, und 3 g Eisessig werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.3. Carrez-Lösung II: 10,6 g Kaliumhexacyanoferrat(II), K4Fe(CN)6·3H2O, werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.4. Reagenz nach Luff-Schoorl:
Die Zitronensäurelösung (Nummer 3.4.2) wird unter vorsichtigem Rühren in die Natriumcarbonatlösung (Nummer 3.4.3) gegossen. Nach Zugabe der Kupfersulfatlösung (Nummer 3.4.1) wird mit Wasser auf 1 l aufgefüllt. Über Nacht absetzen lassen und dann filtrieren. Die Konzentration des so erhaltenen Reagenz (Cu 0,05 mol/l; Na2CO3 1 mol/l) muss geprüft werden. Der pH-Wert der Lösung muss bei etwa 9,4 liegen.
3.4.1. Kupfersulfatlösung: 25 g Kupfersulfat, CuSO4·5H2O, eisenfrei, werden in 100 ml Wasser gelöst.
3.4.2. Zitronensäurelösung: 50 g Zitronensäure, C6H8O7· Η2O werden in 50 ml Wasser gelöst.
3.4.3. Natriumcarbonatlösung: 143,8 g Natriumcarbonat, wasserfrei, werden in ca. 300 ml warmem Wasser gelöst. Die Lösung wird abkühlen gelassen.
3.5. Bimssteinkörner, mit Salzsäure ausgekocht, mit Wasser gewaschen und getrocknet.
3.6. Kaliumiodidlösung (Massenkonzentration = 30 %).
3.7. Schwefelsäure 3 mol/l.
3.8. Natriumthiosulfatlösung 0,1 mol/l.
3.9. Stärkelösung: Eine Aufschlämmung von 5 g löslicher Stärke in 30 ml Wasser wird zu 1 l siedendem Wasser hinzugefügt und 3 min lang im Sieden halten; dann wird abgekühlt und es werden gegebenenfalls 10 mg Quecksilberiodid als Konservierungsmittel hinzugefügt.
4. Geräte
Wasserbad mit Thermostat, auf 38 bis 40 °C eingestellt.
5. Verfahren
Von der Probe wird 1 g auf 1 mg genau eingewogen und mit 25 bis 30 ml Wasser in einen 100-ml-Messkolben gebracht. Der Messkolben wird 30 min lang in ein Bad mit siedendem Wasser gestellt und dann auf etwa 35 °C abgekühlt. Anschließend werden 5 ml Hefesuspension (Nummer 3.1) zugefügt und es wird homogenisiert. Der Kolben wird 2 h lang in einem Wasserbad bei 38 bis 40 °C stehen gelassen und auf etwa 20 °C abgekühlt.
Danach werden 2,5 ml Carrez-Lösung I (Nummer 3.2) hinzugefügt, und es wird 30 s lang gerührt. Dann werden 2,5 ml Carrez-Lösung II (Nummer 3.3) hinzugefügt, und es wird nochmals 30 s lang gerührt. Nun wird mit Wasser auf 100 ml aufgefüllt, gemischt und filtriert. Vom Filtrat wird eine Menge von höchstens 25 ml, die möglichst 40 bis 80 mg Lactose enthält, in einen 300-ml-Erlenmeyerkolben abpipettiert. Gegebenenfalls wird mit Wasser auf 25 ml aufgefüllt.
Auf dieselbe Weise wird ein Blindversuch mit 5 ml Hefesuspension (Nummer 3.1) ausgeführt. Dann wird der Gehalt an Lactose nach der Luff-Schoorl-Methode wie folgt bestimmt: Nach Zugabe von genau 25 ml des Reagenz nach Luff-Schoorl (Nummer 3.4) und von 2 Körnchen Bimsstein (Nummer 3.5) wird unter Schütteln mit der Hand über freier Flamme von mittlerer Höhe erhitzt, sodass die Flüssigkeit in etwa 2 min zum Sieden kommt. Anschließend wird der Erlenmeyerkolben sofort auf ein Drahtnetz mit einer Asbestscheibe, in die ein Loch von etwa 6 cm Durchmesser gestanzt wurde, gestellt; vorher wird unter dem Drahtnetz eine Flamme entzündet und so eingestellt, dass der Kolben nur am Boden erhitzt wird. Dann wird der Kolben mit einem Rückflusskühler verbunden. Von diesem Augenblick an wird der Kolben genau 10 min lang sieden gelassen. Anschließend wird er sofort in kaltem Wasser abgekühlt und nach etwa 5 min wird wie folgt titriert:
Zu der Flüssigkeit werden 10 ml Kaliumiodidlösung (Nummer 3.6) und unmittelbar danach, aber vorsichtig (wegen der Gefahr des übermäßigen Schäumens), 25 ml Schwefelsäure (Nummer 3.7) hinzugegeben. Dann wird mit Natriumthiosulfatlösung (Nummer 3.8) zunächst bis zum Auftreten einer mattgelben Farbe titriert und nach Zugabe von Stärkelösung (Nummer 3.9) als Indikator die Titration zu Ende geführt.
Die gleiche Titration wird in einer Mischung aus genau 25 ml Reagenz nach Luff-Schoorl (Nummer 3.4) und 25 ml Wasser nach Zugabe von 10 ml Kaliumiodidlösung (Nummer 3.6) und 25 ml Schwefelsäure (Nummer 3.7) durchgeführt, jedoch ohne vorheriges Erhitzen.
6. Berechnung der Ergebnisse
Aus der zugehörigen Tabelle wird die Menge Lactose in mg abgelesen, die der Differenz der Ergebnisse beider Titrationen, ausgedrückt in ml Natriumthiosulfatlösung (0,1 mol/l), entspricht.
Das Ergebnis entspricht dem Gehalt an wasserfreier Lactose und wird als Prozentsatz der Probe ausgedrückt.
7. Bemerkung
Tabelle für 25 ml Reagenz nach Luff-Schoorl
ml Na2S2O3 0,1 mol/l, 2 min lang erhitzen, 10 min lang sieden
| Na2S2O3 0,1 mol/l | Glucose, Fructose, Invertzucker C6H12O6 | Lactose C12H22O11 | Na2S2O3 0,1 mol/l | ||
| ml | mg | Differenz | mg | Differenz | ml |
| 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 | 2,4 4,8 7,2 9,7 12,2 14,7 17,2 19,8 22,4 25,0 27,6 30,3 33,0 35,7 38,5 41,3 44,2 47,1 50,0 53,0 56,0 59,1 62,2 | 2,4 2,4 2,5 2,5 2,5 2,5 2,6 2,6 2,6 2,6 2,7 2,7 2,7 2,8 2,8 2,9 2,9 2,9 3,0 3,0 3,1 3,1 | 3,6 7,3 11,0 14,7 18,4 22,1 25,8 29,5 33,2 37,0 40,8 44,6 48,4 52,2 56,0 59,9 63,8 67,7 71,7 75,7 79,8 83,9 88,0 | 3,7 3,7 3,7 3,7 3,7 3,7 3,7 3,7 3,8 3,8 3,8 3,8 3,8 3,8 3,9 3,9 3,9 4,0 4,0 4,1 4,1 4,1 | 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |
K. Bestimmung des Stärkegehalts
Polarimetrisches Verfahren
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an Stärke und ihrer Abbauprodukte mit hoher Molmasse in Futtermitteln zum Zweck der Prüfung ihrer Übereinstimmung mit dem angegebenen Energiegehalt (Anhang VII) und mit der Verordnung (EG) Nr. 767/2009 bestimmen.
Die Methode ist anzuwenden, um den Stärkegehalt für die Berechnung des Energiegehalts des Futtermittels zu bestimmen.
Ist der Stärkegehalt für andere Zwecke zu bestimmen, können andere Analysemethoden angewendet werden.
2. Prinzip
Die Methode basiert auf einer doppelten Bestimmung. Bei der ersten Bestimmung wird die Probe mit verdünnter Salzsäure behandelt. Nach Klärung und Filtration wird die optische Drehung der Lösung polarimetrisch gemessen.
Bei der zweiten Bestimmung wird die Probe mit 40 %igem Ethanol extrahiert. Nach Behandlung des Filtrats mit Salzsäure wird geklärt, filtriert und die optische Drehung unter den gleichen Bedingungen wie bei der ersten Bestimmung gemessen.
Der Unterschied zwischen den beiden Messungen, multipliziert mit einem bekannten Faktor, ergibt den Stärkegehalt der Probe.
3. Reagenzien
3.1. Salzsäure, Lösung (Massenanteil = 25 %) Dichte: 1,126 g/ml.
3.2. Salzsäure, Lösung (Massenkonzentration = 1,13 %).
Die Konzentration muss durch Titration mit Natriumhydroxidlösung (0,1 mol/l) in Gegenwart von Methylrot (Massenkonzentration = 0,1 %) in Ethanol (Volumenkonzentration = 94 %) geprüft werden. Zur Neutralisierung von 10 ml werden 30,94 ml NaOH (0,1 mol/l) benötigt.
3.3. Carrez-Lösung I: 21,9 g Zinkacetat, Zn (CH3COO)2·2H2O, und 3 g Eisessig werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.4. Carrez-Lösung II: 10,6 g Kaliumhexacyanoferrat(II), K4Fe(CN)6·3H2O, werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.5. Ethanol, Lösung (Volumenkonzentration = 40 %), Dichte: 0,948 g/ml bei 20 °C.
4. Geräte
4.1. 250-ml-Erlenmeyerkolben mit Schliffstopfen und Rückflusskühler.
4.2. Polarimeter oder Saccharimeter.
5. Verfahren
5.1. Vorbereitung der Probe
Die Probe muss so fein zermahlen werden, dass sie vollständig durch ein Rundlochsieb mit einem Lochdurchmesser von 0,5 mm passiert werden kann.
5.2. Bestimmung der gesamten optischen Drehung (P oder S) (siehe Bemerkung 7.1)
Von der zermahlenen Probe werden 2,5 g auf 1 mg genau in einen 100-ml-Messkolben eingewogen. Es werden 25 ml Salzsäure (Nummer 3.2) hinzugefügt und der Kolben wird geschüttelt, bis sich der Stoff gleichmäßig verteilt hat; dann werden weitere 25 ml Salzsäure (Nummer 3.2) hinzugegeben. Der Kolben wird in ein Bad mit kochendem Wasser gestellt und während der ersten 3 min kräftig und regelmäßig geschüttelt, um die Bildung von Klumpen zu verhindern. Die in dem Wasserbad enthaltene Wassermenge muss ausreichen, um das Wasser auch dann noch über dem Siedepunkt zu halten, wenn der Kolben eingetaucht wird. Während des Schüttelns darf der Kolben nicht aus dem Wasser herausgenommen werden. Nach genau 15 min wird der Kolben aus dem Wasserbad entfernt, es werden 30 ml kaltes Wasser hinzugefügt und es wird unverzüglich auf 20 °C abgekühlt.
Danach werden 5 ml Carrez-Lösung I (Nummer 3.3) hinzugefügt, und es wird ca. 30 s lang geschüttelt. Anschließend werden 5 ml Carrez-Lösung II (Nummer 3.4) hinzugefügt, und es wird nochmals ca. 30 s lang geschüttelt. Dann wird mit Wasser zur Marke aufgefüllt, gemischt und filtriert. Ist das Filtrat nicht vollständig klar (was selten vorkommt), muss die Bestimmung mit größeren Mengen Carrez-Lösungen I und II, z.B. 10 ml, wiederholt werden.
Anschließend wird die optische Drehung der Lösung in einem 200-mm-Rohr mit einem Polarimeter oder einem Saccharimeter gemessen.
5.3. Bestimmung der optischen Drehung (P" oder S") der in 40 %igem Ethanol löslichen Substanzen
Von der Probe werden 5 g auf 1 mg genau in einen 100-ml-Messkolben eingewogen und es werden etwa 80 ml Ethanol (Nummer 3.5) hinzugefügt (siehe Bemerkung 7.2). Anschließend wird der Kolben 1 h lang bei Raumtemperatur stehen gelassen; währenddessen wird er 6-mal kräftig geschüttelt, damit sich die Analysenprobe gründlich mit dem Ethanol vermischt. Dann wird mit Ethanol (Nummer 3.5) zur Marke aufgefüllt, gemischt und filtriert.
Von dem Filtrat werden 50 ml (= 2,5 g der Probe) in einen 250-ml-Erlenmeyerkolben abpipettiert und es werden 2,1 ml Salzsäure (Nummer 3.1) hinzugefügt; der Kolben wird kräftig geschüttelt, an einen Rückflusskühler angeschlossen und in ein Bad mit siedendem Wasser gestellt. Nach genau 15 min wird der Erlenmeyerkolben aus dem Wasserbad herausgenommen und der Inhalt in einen 100-ml-Messkolben mit einer kleinen Menge von kaltem Wasser überspült; anschließend wird auf 20 °C abgekühlt.
Danach wird mit den Carrez-Lösungen I (Nummer 3.3) und II (Nummer 3.4) geklärt, mit Wasser zur Marke aufgefüllt, gemischt und filtriert und die optische Drehung gemessen, wie unter Nummer 5.2 Absätze 2 und 3 beschrieben.
6. Berechnung der Ergebnisse
Der Stärkegehalt (%) wird wie folgt berechnet:
6.1. Polarimetrische Messung
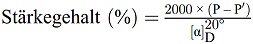
| P | = | Optische Drehung insgesamt in Winkelgrad |
| P" | = | Optische Drehung in Winkelgrad der in 40 %igem Ethanol löslichen Substanzen |
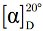 | = | Spezifische optische Drehung von reiner Stärke. Für diesen Faktor werden die nachstehenden, allgemein anerkannten Werte angewendet: |
| + 185,9°: | Reisstärke, | |
| + 185,7°: | Kartoffelstärke, | |
| + 184,6°: | Maisstärke, | |
| + 182,7°: | Weizenstärke, | |
| + 181,5°: | Gerstenstärke, | |
| + 181,3°: | Haferstärke, | |
| + 184,0°: | sonstige Stärkearten sowie Stärkegemische in Mischfuttermitteln. |
6.2. Saccharimetrische Messung
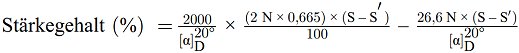
| S | = | Optische Drehung insgesamt in Saccharimeter-Grad |
| S" | = | Optische Drehung in Saccharimeter-Grad der in 40 %igem Ethanol löslichen Substanzen |
| N | = | Gewicht (g) von Saccharose in 100 ml Wasser, das bei Messung mit einem 200-mm-Rohr eine optische Drehung von 100 Saccharimeter-Grad bewirkt:
16,29 g für die französischen Saccharimeter, 26,00 g für die deutschen Saccharimeter, |
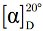 | = | Spezifische optische Drehung von reiner Stärke (siehe Nummer 6.1). |
6.3. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 0,4 (absolut) bei Stärkegehalten von weniger als 40 % und 1 % (relativ) bei Stärkegehalten von 40 % und mehr nicht überschreiten.
7. Bemerkungen
7.1. Enthält die Probe mehr als 6 % Carbonate, berechnet als Calciumcarbonat, so müssen diese vor der Bestimmung der gesamten optischen Drehung durch Behandlung mit der genau notwendigen Menge verdünnter Schwefelsäure zerstört werden.
7.2. Bei Erzeugnissen mit hohem Lactosegehalt, z.B. bei Molkenpulver oder Magermilchpulver, wird nach Zusatz von 80 ml Ethanol (Nummer 3.5) wie folgt verfahren: Der Messkolben wird an einen Rückflusskühler angeschlossen und 30 min lang in ein Wasserbad von 50 °C gestellt. Nach dem Abkühlen wird das Verfahren, wie unter Nummer 5.3 beschrieben, fortgeführt.
7.3. Folgende Futtermittel-Ausgangserzeugnisse führen, sofern sie in größeren Mengen in Futtermitteln vorhanden sind, erwiesenermaßen zu Interferenzen bei der Bestimmung des Stärkegehalts mithilfe des polarimetrischen Verfahrens und könnten so falsche Ergebnisse zur Folge haben:
L. Bestimmung des Rohaschegehalts
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Rohaschegehalt von Futtermitteln bestimmen.
2. Prinzip
Die Probe wird bei 550 °C verascht; der Rückstand wird gewogen.
3. Reagenzien
Ammoniumnitrat, Lösung (Massenkonzentration = 20 %).
4. Geräte
4.1. Heizplatte.
4.2. Elektrischer Muffelofen mit Thermostat.
4.3. Veraschungsschalen aus Quarzglas, Porzellan oder Platin, entweder rechteckig (ca. 60 × 40 × 25 mm) oder rund (Durchmesser: 60 bis 75 mm, Höhe: 20 bis 40 mm).
5. Verfahren
Etwa 5 g (2,5 g bei Stoffen, die zur Blasenbildung neigen) der Probe werden auf 1 mg genau in eine vorher bei 550 °C geglühte, abgekühlte und tarierte Veraschungsschale eingewogen. Die Schale wird auf der Heizplatte allmählich bis zum Verkohlen des Stoffes erhitzt. Die Veraschung erfolgt gemäß Nummer 5.1 oder 5.2.
5.1. Die Schale wird in den auf 550 °C eingestellten kalibrierten Muffelofen gebracht und darin bei dieser Temperatur so lange gehalten, bis sich eine weiße, hellgraue oder rötliche Asche bildet, die offensichtlich frei von Kohlepartikeln ist. Dann wird die Schale in einen Exsikkator gestellt und unmittelbar nach dem Abkühlen gewogen.
5.2. Die Schale wird 3 h lang in den auf 550 °C eingestellten kalibrierten Muffelofen gebracht. Dann wird die Schale in einen Exsikkator gestellt und unmittelbar nach dem Abkühlen gewogen. Anhand einer zweiten Veraschung von 30 min Dauer ist sicherzustellen, dass das Gewicht der Asche konstant bleibt (der Gewichtsverlust zwischen 2 aufeinanderfolgenden Wägungen darf 1 mg nicht überschreiten).
6. Berechnung der Ergebnisse
Das Gewicht des Rückstands wird berechnet, indem das Leergewicht abgezogen wird.
Das Ergebnis ist als Prozentsatz der Probe auszudrücken.
7. Bemerkungen
7.1. Bei schwer zerstörbaren Stoffen werden der abgekühlten Rohasche nach einer ersten Veraschung von mindestens 3 h einige Tropfen 20%iger Ammoniumnitratlösung oder Wasser zugefügt (jedoch vorsichtig, um ein Zerstäuben oder Verkleben der Asche zu vermeiden). Nach Trocknung im Trockenschrank wird die Veraschung weitergeführt. Der Vorgang wird gegebenenfalls bis zur vollständigen Veraschung wiederholt.
7.2. Bei Stoffen, die der unter Nummer 7.1 beschriebenen Behandlung widerstehen, ist wie folgt vorzugehen: Nach einer Veraschung von 3 h Dauer wird die Asche mit warmem Wasser aufgenommen und durch einen kleinen aschefreien Filter abfiltriert. In der ursprünglichen Schale werden Filter und dessen Inhalt verascht. Das Filtrat wird in die abgekühlte Schale gebracht, bis zur Trockne eingedampft, verascht und gewogen.
7.3. Bei Ölen und Fetten wird eine Probe von 25 g in eine Schale entsprechender Abmessung genau eingewogen. Es wird dann durch Anzünden des Stoffes mit einem Streifen aus aschefreiem Filterpapier verkohlt. Nach der Verkohlung wird mit möglichst geringer Menge Wasser angefeuchtet. Anschließend wird getrocknet und die Veraschung, wie unter Nummer 5 beschrieben, zu Ende geführt.
M. Bestimmung des Gehalts an in Salzsäure unlöslicher Asche
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an in Salzsäure unlöslichen, mineralischen Bestandteilen des Futtermittels bestimmen. Abhängig von der Art der Probe können 2 Verfahren angewandt werden.
1.1. Verfahren A: anzuwenden bei organischen Futtermittel-Ausgangserzeugnissen und bei den meisten Mischfuttermitteln.
1.2. Verfahren B: anzuwenden bei Mineralstoffen und Mineralstoffmischungen sowie bei allen Mischfuttermitteln, deren Gehalt an in Salzsäure unlöslichen Bestandteilen bei der Bestimmung nach Verfahren A mehr als 1 % beträgt.
2. Prinzip
2.1. Verfahren A: Die Probe wird verascht. Die Asche wird in Salzsäure zum Sieden gebracht und der unlösliche Rückstand abfiltriert und gewogen.
2.2. Verfahren B: Die Probe wird mit Salzsäure behandelt. Die Lösung wird abfiltriert, der Rückstand wird verascht, und die so erhaltene Asche nach Verfahren A weiterbehandelt.
3. Reagenzien
3.1. Salzsäure 3 mol/l.
3.2. Trichloressigsäure, Lösung (Massenkonzentration = 20 %).
3.3. Trichloressigsäure, Lösung (Massenkonzentration = 1 %).
4. Geräte
4.1. Heizplatte.
4.2. Elektrischer Muffelofen mit Thermostat.
4.3. Veraschungsschalen aus Quarzglas, Porzellan oder Platin, entweder rechteckig (ca. 60 × 40 × 25 mm) oder rund (Durchmesser: 60 bis 75 mm, Höhe: 20 bis 40 mm).
4.4. Aschefreie Filter.
5. Verfahren
5.1. Verfahren A:
Die Einwaage wird unter den Bedingungen, die für die Bestimmung des Rohaschegehalts beschrieben sind, verascht. Es kann auch die bei dieser Analyse erhaltene Asche verwendet werden.
Die Asche wird zusammen mit 75 ml Salzsäure (Nummer 3.1) in ein Becherglas von 250 bis 400 ml Inhalt überführt. Es wird vorsichtig zum Sieden erhitzt und 15 min lang weiter in schwachem Sieden gehalten. Die warme Lösung wird durch einen aschefreien Papierfilter filtriert und der Rückstand wird mit warmem Wasser bis zum Ausbleiben der sauren Reaktion ausgewaschen. Der Filter mit dem Rückstand wird nach dem Trocknen bei einer Temperatur von mindestens 550 °C und höchstens 700 °C in einer tarierten Veraschungsschale verascht und anschließend im Exsikkator gekühlt und gewogen.
5.2. Verfahren B
Von der Probe werden 5 g auf 1 mg genau in ein Becherglas von 250 bis 400 ml Fassungsvermögen eingewogen. Dann werden nacheinander 25 ml Wasser und 25 ml Salzsäure (Nummer 3.1) zugegeben, gemischt, und es wird bis zum Nachlassen des Aufbrausens gewartet. Zuletzt werden weitere 50 ml Salzsäure (Nummer 3.1) zugegeben. Nach dem Nachlassen der eventuell erneut auftretenden Gasentwicklung wird das Becherglas 30 min lang oder, wenn notwendig, länger in ein siedendes Wasserbad gestellt, bis die vollständige Hydrolyse eventuell vorhandener Stärke eingetreten ist. Es wird warm durch einen aschefreien Filter filtriert. Der Filter wird mit etwa 50 ml warmem Wasser ausgewaschen (siehe Bemerkung 7). Anschließend wird der Filter mit Rückstand in eine Veraschungsschale gestellt, getrocknet und bei einer Temperatur von mindestens 550 °C und höchstens 700 °C verascht. Die Asche wird mit 75 ml Salzsäure (Nummer 3.1) in ein Becherglas von 250 bis 400 ml Fassungsvermögen überführt und anschließend, wie unter Nummer 5.1 Absatz beschrieben, weiterbehandelt.
6. Berechnung der Ergebnisse
Das Gewicht des Rückstands wird berechnet, indem das Leergewicht abgezogen wird. Das Ergebnis ist als Prozentsatz der Probe auszudrücken.
7. Bemerkung
Treten bei der Filtration Schwierigkeiten auf, so wird die Bestimmung wiederholt. Hierbei werden anstelle von 50 ml Salzsäure (Nummer 3.1) 50 ml Trichloressigsäure, Lösung (Massenkonzentration = 20 %) (Nummer 3.2), zugegeben; der Filter wird mit einer warmen 1%igen Trichloressigsäurelösung (Nummer 3.3) ausgewaschen.
N. Bestimmung des Gesamtphosphorgehalts
Der Gesamtphosphorgehalt wird anhand folgender Methode bestimmt:
Fotometrische Methode
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Gehalt an Gesamtphosphor in Futtermitteln bestimmen. Sie ist besonders für die Untersuchung von Futtermitteln mit einem geringen Phosphorgehalt geeignet. In bestimmten Fällen (phosphorreiche Erzeugnisse) kann eine gravimetrische Methode angewandt werden.
2. Prinzip
Die Probe wird entweder auf trockenem Wege (bei organischen Futtermitteln) oder auf nassem Wege (bei Mineralstoffen und flüssigen Futtermitteln) aufgeschlossen und in Säure gelöst. Die Lösung wird mit dem Vanadat-Molybdat-Reagenz behandelt. Die Extinktion der gelb gefärbten Lösung wird bei 430 nm im Spektralfotometer gemessen.
3. Reagenzien
3.1. Calciumcarbonat.
3.2. Salzsäure, ρ20 = 1,10 g/ml (ca. 6 mol/l).
3.3. Salpetersäure, ρ20 = 1,045 g/ml.
3.4. Salpetersäure, ρ20 = 1,38 bis 1,42 g/ml.
3.5. Schwefelsäure, ρ20 = 1,84 g/ml.
3.6. Vanadat-Molybdat-Reagenz: 200 ml Ammoniumheptamolybdatlösung (Nummer 3.6.1) werden mit 200 ml Ammoniummonovanadatlösung (Nummer 3.6.2) und 134 ml Salpetersäure (Nummer 3.4) in einem 1-l-Messkolben gemischt und mit Wasser zur Marke aufgefüllt.
3.6.1. Ammoniumheptamolybdatlösung: 100 g Ammoniumheptamolybdat, (NH4) 6Mo7O24·4H2O, werden in heißem Wasser gelöst. 10 ml Ammoniakwasser (D: 0,91 g/ml) werden hinzugefügt, und das Volumen wird mit Wasser auf 1 l aufgefüllt.
3.6.2. Ammoniummonovanadatlösung: 2,35 g Ammoniummonovanadat, NH4VO3, werden in 400 ml heißem Wasser gelöst. 20 ml verdünnte Salpetersäure (7 ml HNO3 (Nummer 3.4) + 13 ml H2O) werden unter ständigem Rühren langsam hinzugefügt, und das Volumen wird mit Wasser auf 1 l aufgefüllt.
3.7. Phosphor-Standardlösung 1 mg je ml: 4,387 g Kaliumdihydrogenphosphat, KH2PO4, werden in Wasser gelöst. Das Volumen wird mit Wasser auf 1 l aufgefüllt..
4. Geräte
4.1. Veraschungsschalen aus Quarzglas, Platin oder Porzellan.
4.2. Elektrischer Muffelofen mit Thermostat auf 550 °C eingestellt.
4.3. Kjeldahl-Kolben, 250 ml.
4.4. Messkolben und Präzisions-Pipetten.
4.5. Spektralfotometer.
4.6. Reagenzgläser, ca. 16 mm Durchmesser, mit Stopfen graduiert bis zu 14,5 mm Durchmesser; Fassungsvermögen: 25 bis 30 ml.
5. Verfahren
5.1. Vorbereitung der Lösung
Je nach der Art der Probe wird die Lösung gemäß Nummer 5.1.1 oder 5.1.2 vorbereitet.
5.1.1. Allgemeines Verfahren
Von der Probe werden 1 g oder mehr auf 1 mg genau in einen Kjeldahl-Kolben eingewogen und mit 20 ml Schwefelsäure (Nummer 3.5) versetzt; dann wird geschüttelt, um das Material vollständig mit der Säure zu benetzen und um zu verhindern, dass es an den Wandungen des Kolbens anhaftet; anschließend wird der Kolben erhitzt und 10 min lang im Sieden gehalten. Nach geringem Abkühlen werden 2 ml Salpetersäure (Nummer 3.4) hinzugefügt; es wird schwach erhitzt und wieder etwas abgekühlt. Dann wird noch ein wenig Salpetersäure (Nummer 3.4) hinzugegeben und erneut zum Sieden erhitzt. Das Verfahren wird so oft wiederholt, bis die Lösung farblos geworden ist. Hierauf wird abgekühlt, etwas Wasser zugesetzt und die Flüssigkeit in einen 500-ml-Messkolben überführt, wobei der Kjeldahl-Kolben mit heißem Wasser ausgespült wird. Nach Abkühlen wird mit Wasser zur Marke aufgefüllt, homogenisiert und filtriert.
5.1.2. Verfahren für Proben, die organische Stoffe enthalten, aber frei sind von Calcium- bzw. Magnesiumdihydrogenphosphaten
Von der Probe werden 2,5 g auf 1 mg genau in eine Veraschungsschale eingewogen und mit 1 g Calciumcarbonat (Nummer 3.1) vollständig vermischt. Im Muffelofen wird bei 550 °C verascht, bis die Asche weiß oder grau ist (kleine Mengen Kohle stören nicht). Die Asche wird in ein 250-ml-Becherglas gebracht. Es werden 20 ml Wasser und so viel Salzsäure (Nummer 3.2) zugefügt, bis das Aufbrausen ausbleibt. Zuletzt werden weitere 10 ml Salzsäure (Nummer 3.2) zugegeben. Dann wird das Becherglas auf ein Sandbad gestellt und bis zur Trockne eingedampft, um die Kieselsäure unlöslich zu machen. Der Rückstand wird in 10 ml Salpetersäure (Nummer 3.3) aufgenommen und 5 min lang auf dem Sandbad oder der Heizplatte zum Sieden erhitzt, wobei der Rückstand nicht ganz trocken werden darf. Die Flüssigkeit wird in einen 500-ml-Messkolben übergespült, wobei das Becherglas mehrmals mit heißem Wasser ausgewaschen wird. Nach Abkühlen wird mit Wasser zur Marke aufgefüllt, homogenisiert und filtriert.
5.2. Entwicklung der Färbung und Messung der Extinktion
Ein aliquoter Teil des nach Nummer 5.1.1 oder 5.1.2 erhaltenen Filtrats wird verdünnt, um eine Konzentration an Phosphor von höchstens 40 μg/ml zu erhalten. Von dieser Lösung werden 10 ml in ein Reagenzglas (Nummer 4.6) pipettiert und es werden 10 ml Vanadat-Molybdat-Reagenz (Nummer 3.6) hinzugefügt. Das Reagenzglas wird geschüttelt und dann mindestens 10 min lang bei einer Temperatur von 20 °C stehen gelassen. Anschließend wird die Extinktion im Spektralfotometer bei 430 nm gegen eine Lösung von 10 ml Wasser und 10 ml Vanadat-Molybdat-Reagenz (Nummer 3.6) gemessen.
5.3. Kalibrationskurve
Aus der Standardlösung (Nummer 3.7) werden Lösungen hergestellt, die 5, 10, 20, 30 bzw. 40 μg Phosphor je ml enthalten. Zu jeweils 10 ml dieser Lösungen werden 10 ml Vanadat-Molybdat-Reagenz (Nummer 3.6) hinzugefügt. Das Reagenzglas wird geschüttelt und dann mindestens 10 min lang bei einer Temperatur von 20 °C stehen gelassen. Dann wird die Extinktion entsprechend den unter Nummer 5.2 genannten Bedingungen gemessen. Die Kalibrationskurve wird aufgestellt, indem die Extinktionswerte auf der Ordinate und die entsprechende Phosphormenge auf der Abszisse aufgetragen werden. Bei Phosphorkonzentrationen von 0 bis 40 μg/ml ist die Kurve linear.
6. Berechnung der Ergebnisse
Der Phosphorgehalt der Analysenprobe wird mithilfe der Kalibrationskurve bestimmt.
Das Ergebnis ist als Prozentsatz der Probe auszudrücken.
Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf die folgenden Werte nicht überschreiten:
O. Bestimmung des Chlorgehalts aus Chloriden
1. Zweck und Anwendungsbereich
Mit der Methode lässt sich der Chlorgehalt aus wasserlöslichen Chloriden, herkömmlicherweise als Natriumchlorid bezeichnet, bestimmen. Sie ist bei allen Futtermitteln anwendbar.
2. Prinzip
Die Chloride werden in Wasser gelöst. Handelt es sich um Erzeugnisse, die organische Stoffe enthalten, wird eine Klärung vorgenommen. Die Lösung wird mittels Salpetersäure schwach angesäuert, und die Chloride werden mit einer Silbernitratlösung als Silberchlorid gefällt. Der Silbernitratüberschuss wird mit einer Ammoniumthiocyanatlösung nach der Volhard-Methode zurücktitriert.
3. Reagenzien
3.1. Ammoniumthiocyanatlösung 0,1 mol/l.
3.2. Silbernitratlösung 0,1 mol/l.
3.3. Gesättigte Ammonium-Eisen(III)-Sulfatlösung (NH4)Fe(SO4)2.
3.4. Salpetersäure, Dichte: 1,38 g/ml.
3.5. Diethylether.
3.6. Aceton.
3.7. Carrez-Lösung I: 21,9 g Zinkacetat, Zn (CH3COO)2·2H2O, und 3 g Eisessig werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.8. Carrez-Lösung II: 10,6 g Kaliumhexacyanoferrat(II), K4Fe(CN)6·3H2O, werden in Wasser gelöst und mit Wasser auf 100 ml aufgefüllt.
3.9. Aktivkohle, chloridfrei und keine Chloride adsorbierend.
4. Geräte
Mechanisches Schüttelgerät: ca. 35 bis 40 min-1.
5. Verfahren
5.1. Vorbereitung der Lösung
Je nach der Art der Probe wird die Lösung gemäß Nummer 5.1.1, 5.1.2 oder 5.1.3 hergestellt.
Gleichzeitig ist ein Blindversuch ohne die zu analysierende Probe durchzuführen.
5.1.1. Proben, die frei von organischen Stoffen sind
Eine Menge von höchstens 10 g der Probe mit einem Gehalt von höchstens 3 g Chlor in Form von Chloriden wird auf 1 mg genau abgewogen und in einen 500-ml-Messkolben mit 400 ml Wasser von etwa 20 °C gebracht. Dann wird 30 min lang in dem Schüttelgerät rotiert, zur Marke aufgefüllt, homogenisiert und filtriert.
5.1.2. Proben, die organische Stoffe enthalten (mit Ausnahme der unter 5.1.3 angeführten Erzeugnisse)
Etwa 5 g der Probe werden auf 1 mg genau eingewogen und mit 1 g Aktivkohle in einen 500-ml-Messkolben gebracht. Hierzu werden 400 ml Wasser von etwa 20 °C und 5 ml Carrez-Lösung I (Nummer 3.7) gegeben, es wird 30 s lang gerührt und anschließend werden 5 ml Carrez-Lösung II (Nummer 3.8) zugesetzt. Dann wird 30 min lang in dem Schüttelgerät rotiert, zur Marke aufgefüllt, homogenisiert und filtriert.
5.1.3. Backfutter, Leinkuchen und Leinmehl, Erzeugnisse mit einem hohen Leinmehlgehalt oder sonstige Erzeugnisse mit einem hohen Gehalt an Pflanzenschleim oder kolloidalen Stoffen (z.B. verkleisterte Stärke)
Die Lösung wird, wie unter 5.1.2 beschrieben, zubereitet, jedoch nicht filtriert. Es wird dekantiert (falls erforderlich, zentrifugiert); dann werden 100 ml der überstehenden Lösung in einen 200-ml-Messkolben pipettiert. Es wird mit Aceton (Nummer 3.6) gemischt und mit demselben Lösungsmittel zur Marke aufgefüllt, homogenisiert und filtriert.
5.2. Titration
Von dem Filtrat, das nach Nummer 5.1.1, 5.1.2 oder 5.1.3 erhalten wurde, werden (je nach dem zu erwartenden Chlorgehalt) 25 bis 100 ml in einen Erlenmeyerkolben pipettiert. Die aliquote Menge darf höchstens 150 mg Chlor (Cl) enthalten. Falls erforderlich, wird mit Wasser auf mindestens 50 ml verdünnt. Dann werden 5 ml Salpetersäure (Nummer 3.4), 2 ml der gesättigten Ammonium-Eisen(III)-Sulfatlösung (Nummer 3.3) und 2 Tropfen Ammoniumthiocyanatlösung (Nummer 3.1) aus einer bis zum Nullpunkt gefüllten Bürette hinzugesetzt. Anschließend wird aus einer Bürette Silbernitratlösung (Nummer 3.2) zugegeben, bis ein Überschuss von 5 ml vorhanden ist. Dann werden 5 ml Diethylether (Nummer 3.5) zugegeben, und es wird kräftig geschüttelt, um den Niederschlag zum Ausflocken zu bringen. Der Überschuss an Silbernitrat wird mit Ammoniumthiocyanatlösung (Nummer 3.1) titriert, bis eine rotbraune Farbe auftritt, die 1 min lang beständig ist.
6. Berechnung der Ergebnisse
Die Menge Chlor (X), ausgedrückt als % Natriumchlorid, wird nach folgender Formel berechnet:
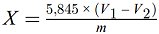
wobei:
| V1 = | zugegebene Silbernitratlösung 0,1 mol/l, in ml, |
| V2 = | Ammoniumthiocyanatlösung 0,1 mol/l, die für die Titration verbraucht werden, in ml, |
| m = | Probeneinwaage (aliquoter Teil) in g. |
Falls der Blindversuch einen Verbrauch an Silbernitratlösung 0,1 mol/l anzeigt, wird dieser Wert von dem Volumen (V1 - V2) abgezogen.
7. Bemerkungen
7.1. Die Titration kann auch potenziometrisch oder amperometrisch erfolgen.
7.2. Bei sehr öl- und fettreichen Erzeugnissen ist eine vorherige Entfettung mit Diethylether oder Petrolether durchzuführen.
7.3. Bei Fischmehl kann die Titration nach der Mohr-Methode durchgeführt werden. "
2) Zur Berechnung im Einzelnen wird verwiesen auf EN ISO 6498 - Futtermittel - Leitfaden für die Probenvorbereitung.
3) Der Gehalt an N lässt sich in allen Futtermitteln bestimmen, nur lässt sich der Umrechnungsfaktor 6,25 zur Berechnung des Rohproteingehalts möglicherweise nicht auf Futtermittel-Ausgangserzeugnisse aus Insekten (niedrigerer Umrechnungsfaktor) und bestimmtes Heimtierfutter und bestimmte Blutplasmaproteine (höherer Umrechnungsfaktor) anwenden.
4) Die Analysemethode gemäß EN 17180 ist als alternative Methode für die Zwecke amtlicher Kontrollen zur Bestimmung des Gehalts an Aminosäuren in Futtermitteln mit mehr als 10 % Aminosäuren genannt.
5) Diese Methode wurde nicht durch einen Ringversuch für Vormischungen validiert, die mehr als 10 % Futtermittelzusatzstoffe enthalten. Sie kann jedoch mit entsprechenden leichten Änderungen auch auf diese Matrizen angewendet werden, sofern sie anschließend intern validiert wird. Nähere Informationen unter https://ec.europa.eu/jrc/en/eurl/feed-additives/authorisation.
6) Soll das Öl oder Fett später einer Qualitätsprüfung unterzogen werden, sind die Bimssteinkörner durch Glasperlen zu ersetzen.
7) Verordnung (EG) Nr. 121/2008 der Kommission vom 11. Februar 2008 zur Festlegung der Analysemethode zur Bestimmung des Stärkegehalts in Zubereitungen von der zur Fütterung verwendeten Art (KN-Code 2309) (ABl. L 37 vom 12.02.2008 S. 3).
| Anhang IV |
"Anhang IV
Analysemethoden zur Untersuchung von Futtermitteln auf ihren Gehalt an zugelassenen Zusatzstoffen
A. Bestimmung des Vitamin-A-Gehalts
Der Vitamin-A-Gehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Vitamin-A-(Retinol-)Gehalts in Futtermitteln. Unter Vitamin A wird der nach dieser Methode ermittelte Gehalt an all-trans-Vitamin-A-Alkohol und seinen cis-Isomeren verstanden. Der Vitamin-A-Gehalt wird in Internationalen Einheiten (IE) je kg angegeben. Eine IE entspricht der Aktivität von 0,300 μg all-trans-Vitamin-A-Alkohol oder 0,344 μg all-trans-Vitamin-A-Acetat oder 0,550 μg all-trans-Vitamin-A-Palmitat.
Die Bestimmungsgrenze beträgt 2.000 IE Vitamin A/kg.
2. Prinzip
Die Probe wird mit ethanolischer Kaliumhydroxidlösung hydrolysiert, und das Vitamin A wird mit Petrolether extrahiert. Das Lösungsmittel wird eingedampft; der Rückstand wird in Methanol gelöst und, falls notwendig, auf die erforderliche Konzentration verdünnt. Der Vitamin-A-Gehalt wird mittels Umkehrphasen-Hochleistungsflüssigkeitschromatografie (RP-HPLC) unter Verwendung eines UV- oder Fluoreszenzdetektors bestimmt. Die chromatografischen Bedingungen werden so gewählt, dass keine Ruftrennung zwischen all-trans-Vitamin-A-Alkohol und seinen cis-Isomeren erfolgt.
3. Reagenzien
3.1. Ethanol, σ = 96 %.
3.2. Petrolether, Siedeintervall 40 bis 60 °C.
3.3. Methanol
3.4. Kaliumhydroxid-Lösung, c = 50 g/100 ml.
3.5. Natriumascorbat-Lösung, c = 10 g/100 ml (siehe Bemerkung 7.7).
3.6. Natriumsulfid, Na2S · x H2O (x = 7 bis 9).
3.6.1. Natriumsulfid-Lösung, c = 0,5 mol/l in Glycerin, β = 120 g/l (für x = 9) (siehe Bemerkung 7.8).
3.7. Phenolphthalein-Lösung, c = 2 g/100 ml in Ethanol (Nummer 3.1).
3.8. 2-Propanol.
3.9. Mobile Phase für die HPLC: Mischung von Methanol (Nummer 3.3) und Wasser z.B. 980 + 20 (V+V) Das Mischungsverhältnis ist der jeweils verwendeten Säule anzupassen.
3.10. Stickstoff, sauerstofffrei.
3.11. All-trans-Vitamin-A-Acetat, reinst, mit zertifizierter Aktivität, z.B. 2,80 × 106 IE/g
3.11.1. Stammlösung von all-trans-Vitamin-A-Acetat: 50 mg Vitamin-A-Acetat (Nummer 3.11) auf 0,1 mg genau in einen 100-ml-Messkolben einwiegen. In 2-Propanol (Nummer 3.8) lösen und mit demselben Lösungsmittel zur Marke auffüllen. Der Sollgehalt dieser Lösung beträgt 1.400 IE Vitamin A je ml. Der genaue Gehalt ist gemäß Nummer 5.6.3.1 zu bestimmen.
3.12. All-trans-Vitamin-A-Palmitat, reinst, mit zertifizierter Aktivität, z.B. 1,80 × 106 IE/g
3.12.1. Stammlösung von all-trans-Vitamin-A-Palmitat: 80 mg Vitamin-A-Palmitat (Nummer 3.12) auf 0,1 mg genau in einen 100-ml-Messkolben einwiegen. In 2-Propanol (Nummer 3.8) lösen und mit demselben Lösungsmittel zur Marke auffüllen. Der Sollgehalt dieser Lösung beträgt 1.400 IE Vitamin A je ml. Der genaue Gehalt ist gemäß Nummer 5.6.3.2 zu bestimmen.
3.13. 2,6-Di-tert-butyl-4-methylphenol (BHT) (siehe Bemerkung 7.5).
4. Geräte
4.1. Vakuum-Rotationsverdampfer.
4.2. Braunglasgeräte
4.2.1. Stehkolben oder Erlenmeyerkolben, 500 ml, mit Schliffhülse.
4.2.2. Messkolben mit Schliffstopfen, enghalsig, 10, 25, 100 und 500 ml.
4.2.3. Scheidetrichter, konische Form, 1.000 ml, mit Schliffstopfen.
4.2.4. Spitzkolben, 250 ml, mit Schliffhülsen.
4.3. Allihn-Rückflusskühler, Mantellänge 300 mm, Kernschliff mit Adapter für Gaseinleitung.
4.4. Phasentrennungsfaltenfilter, DurchmesS.r.1.5 mm (z.B. Schleicher & Schuell 597 HY 1/2).
4.5. HPLC-Einrichtung mit Injektionssystem
4.5.1. HPLC-Trennsäule, 250 mm × 4 mm, C18, 5 oder 10 μm Korngröße, oder vergleichbare Säule (Leistungskriterium: nur ein Peak für alle Retinol-Isomeren unter diesen HPLC-Bedingungen).
4.5.2. UV- oder Fluoreszenzdetektor mit variabler Wellenlängeneinstellung.
4.6. Spektralfotometer mit Quarz-Küvetten von 10 mm Schichtdicke.
4.7. Wasserbad mit Magnetrührer.
4.8. Extraktionsapparat (Abbildung 1) bestehend aus:
4.8.1. 1-l-Standzylinder mit Schliff und Schliffstopfen,
4.8.2. Schliffeinsatz mit Seitenarm und einem in der Höhe verschiebbaren Rohr in der Mitte. Das verschiebbare Rohr muss ein U-förmiges unteres Ende und eine Düse am entgegengesetzten Ende haben, sodass die obere Flüssigkeitsphase aus dem Zylinder in den Scheidetrichter überführt werden kann.
5. Verfahren
| Anmerkung: | Vitamin A ist empfindlich gegenüber Licht (UV-Strahlung) und Oxidation. Daher muss unter Ausschluss von Licht (Verwendung von Braunglasgeräten oder von mit Aluminiumfolie umhüllten Glasgeräten) und Sauerstoff (Stickstoffspülung) gearbeitet werden. Während der Extraktion muss das Luftpolster über der Flüssigkeit durch Stickstoff ersetzt werden (zur Vermeidung von Überdruck Stopfen immer wieder lüften). |
5.1. Vorbereitung der Probe
Die Probe wird unter Vermeidung von Erwärmung so fein vermahlen, dass sie ein Sieb mit 1 mm Maschenweite passieren kann. Das Mahlen darf erst unmittelbar vor dem Einwiegen und Verseifen erfolgen, da sonst Vitamin-A-Verluste auftreten können. Wenn die Größenverteilung der Partikel geeignet ist, darf die Probe (dürfen die Proben) nicht gemahlen werden (z.B. bei Vormischungen und Futtermittelzusatzstoffen).
5.2. Verseifung
Je nach Vitamin-A-Gehalt 2 bis 25 g der Probe auf 1 mg genau in einen 500-ml-Steh- oder Erlenmeyerkolben (Nummer 4.2.1) einwiegen. Bei niedrigen Konzentrationen kann das Probengewicht erhöht werden, um genügend Partikel in der Testmenge zu erhalten. Nacheinander unter Schwenken 130 ml Ethanol (Nummer 3.1), etwa 100 mg BHT (Nummer 3.13), 2 ml Natriumascorbat-Lösung (Nummer 3.5) und 2 ml Natriumsulfid-Lösung (Nummer 3.6) zusetzen. Den Kolben mit einem Rückflusskühler (Nummer 4.3) verbinden und in ein Wasserbad mit Magnetrührer (Nummer 4.7) geben. Bis zum Sieden erhitzen und 5 min am Rückflusskühler kochen. Anschließend 25 ml Kaliumhydroxidlösung (Nummer 3.4) durch den Rückflusskühler (Nummer 4.3) zugeben, und unter ständigem Rühren und schwachem Stickstoffstrom 25 min weiterkochen. Den Kühler mit etwa 20 ml Wasser ausspülen und den Kolbeninhalt auf Zimmertemperatur abkühlen.
5.3. Extraktion
Die Verseifungslösung wird mit insgesamt 250 ml Wasser quantitativ in einen 1.000-ml-Scheidetrichter (Nummer 4.2.3) oder in den Extraktionsapparat (Nummer 4.8) überspült. Der Verseifungskolben wird mit 25 ml Ethanol (Nummer 3.1) und anschließend mit 100 ml Petrolether (Nummer 3.2) nachgewaschen, und die Spülflüssigkeiten werden ebenfalls in den Scheidetrichter oder den Extraktionsapparat überführt. Das Wasser/Ethanol-Verhältnis in den vereinigten Lösungen muss etwa 2:1 betragen. 2 min kräftig schütteln und dann 2 min absetzen lassen.
5.3.1. Extraktion mithilfe eines Scheidetrichters (Nummer 4.2.3)
Nach Phasentrennung (siehe Bemerkung 7.3) wird die Petroletherphase in einen anderen Scheidetrichter (Nummer 4.2.3) überführt. Diese Extraktion 2-mal mit je 100 ml Petrolether (Nummer 3.2) und 2-mal mit je 50 ml Petrolether (Nummer 3.2) wiederholen.
Die vereinigten Extrakte werden im Scheidetrichter unter leichtem Schwenken (Vermeidung von Emulsionsbildung) 2-mal mit jeweils 100 ml Wasser gespült und dann durch mehrmaliges Schütteln mit weiteren Portionen von 100 ml Wasser so oft gewaschen, bis das Waschwasser bei Zugabe von Phenolphthalein-Lösung (Nummer 3.7) farblos bleibt (4-maliges Waschen ist normalerweise ausreichend). Zur Entfernung eventuell suspendierten Wassers wird der gewaschene Extrakt durch einen trockenen Phasentrennungsfaltenfilter (Nummer 4.4) in einen 500-ml-Messkolben (Nummer 4.2.2) filtriert. Scheidetrichter und Filter mit 50 ml Petrolether (Nummer 3.2) nachwaschen, mit Petrolether (Nummer 3.2) zur Marke auffüllen und gut schütteln.
5.3.2. Extraktion mithilfe eines Extraktionsapparats (Nummer 4.8)
Nach Phasentrennung (siehe Bemerkung 7.3) wird der Stopfen des Standzylinders (Nummer 4.8.1) durch den Schliffeinsatz (Nummer 4.8.2) ersetzt und das verschiebbare Rohr so eingestellt, dass sich das U-förmige untere Ende gerade über dem Niveau der Grenzfläche befindet. Durch Druckausübung von einer am Seitenarm angebrachten Stickstoffleitung wird die obere Petroletherphase in einen 1.000-ml-Scheidetrichter (Nummer 4.2.3) überführt. 100 ml Petrolether (Nummer 3.2) werden in den Standzylinder gegeben, der mit einem Stopfen verschlossen und gründlich geschüttelt wird. Nach der Phasentrennung wird die obere Phase wie zuvor in den Scheidetrichter überführt. Diese Extraktion wird noch 1-mal mit 100 ml Petrolether (Nummer 3.2) und 2-mal mit je 50 ml Petrolether (Nummer 3.2) wiederholt, und die Petroletherphasen werden in den Scheidetrichter überführt.
Die vereinigten Petroletherextrakte, wie unter 5.3.1 erläutert, waschen und wie dort beschrieben weiterverfahren.
5.4. Vorbereitung der Probenlösung für die HPLC
Ein aliquoter Teil der Petrolether-Lösung (gemäß Nummer 5.3.1 oder 5.3.2) wird in einen 250-ml-Spitzkolben (Nummer 4.2.4) pipettiert. Das Lösungsmittel wird unter vermindertem Druck und bei einer Badtemperatur von höchstens 40 °C am Rotationsverdampfer (Nummer 4.1) fast bis zur Trockne eingedampft. Danach wird unter Stickstoff (Nummer 3.10) Druckausgleich geschaffen und der Kolben vom Rotationsverdampfer abgenommen. Das restliche Lösungsmittel wird im Stickstoffstrom (Nummer 3.10) abgeblasen, und der Rückstand wird sofort in einer definierten Menge (10 bis 100 ml) Methanol (Nummer 3.3) aufgenommen (die Konzentration von Vitamin A muss etwa 5 bis 30 IE/ml betragen).
5.5. Bestimmung durch HPLC
Die Abtrennung von Vitamin A erfolgt mithilfe einer Umkehrphasen-C18-Säule (Nummer 4.5.1), und die Konzentration wird mithilfe eines UV-Detektors (325 nm) oder eines Fluoreszenzdetektors (Anregung: 325 nm, Emission: 475 nm) (Nummer 4.5.2) gemessen.
Hierzu wird ein aliquoter Teil (z.B. 20 μl) der nach Nummer 5.4 erhaltenen methanolischen Lösung auf die Trennsäule gegeben und mit der mobilen Phase (Nummer 3.9) eluiert. Die mittlere Peakhöhe (-fläche) von mehreren Einspritzungen derselben Probenlösung wird ermittelt. In gleicher Weise werden auch die mittleren Peakhöhen (-flächen) von mehreren Einspritzungen der Kalibrierlösungen (Nummer 5.6.2) bestimmt.
HPLC-Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen:
| HPLC-Trennsäule (Nummer 4.5.1): | 250 × 4 mm, C18, 5 oder 10 μm Korngröße, oder vergleichbare Säule |
| Mobile Phase (Nummer 3.9): | Mischung von Methanol (Nummer 3.3) und Wasser z.B. 980 + 20 (V+V) |
| Durchflussrate: | 1 bis 2 ml/min |
| Detektor (Nummer 4.5.2): | UV-Detektor (325 nm) oder Fluoreszenzdetektor (Anregung: 325 nm, Emission: 475 nm |
5.6. Kalibrierung
5.6.1. Herstellen der Gebrauchsstandardlösungen
20 ml der Vitamin-A-Acetat-Stammlösung (Nummer 3.11.1) oder 20 ml der Vitamin-A-Palmitat-Stammlösung (Nummer 3.12.1) in einen 500-ml-Steh- oder Erlenmeyerkolben (Nummer 4.2.1) pipettieren und, wie unter 5.2 beschrieben, aber ohne Zugabe von BHT, hydrolysieren. Anschließend mit Petrolether (Nummer 3.2) gemäß Nummer 5.3 extrahieren und mit Petrolether (Nummer 3.2) auf 500 ml auffüllen. 100 ml dieses Extrakts werden am Rotationsverdampfer (siehe 5.4) fast bis zur Trockne eingedampft. Das verbleibende Lösungsmittel wird im Stickstoffstrom (Nummer 3.10) abgeblasen, und der Rückstand wird in 10,0 ml Methanol (Nummer 3.3) aufgenommen. Der Sollgehalt dieser Lösung beträgt 560 IE Vitamin A je ml. Der genaue Gehalt ist nach Nummer 5.6.3.3 zu bestimmen. Die Gebrauchsstandardlösung muss vor Gebrauch frisch hergestellt werden.
Von dieser Gebrauchsstandardlösung werden 2,0 ml in einen 20-ml-Messkolben pipettiert. Es wird mit Methanol (Nummer 3.3) zur Marke aufgefüllt und gemischt. Der Sollgehalt dieser verdünnten Gebrauchsstandardlösung beträgt 56 IE Vitamin A je ml.
5.6.2. Herstellen der Kalibrierlösungen und Erstellung der Kalibrationskurve
Von der verdünnten Gebrauchsstandardlösung werden 1,0 ml, 2,0 ml, 5,0 ml bzw. 10,0 ml in jeweils einen 20-ml-Messkolben pipettiert. Es wird mit Methanol (Nummer 3.3) zur Marke aufgefüllt und gemischt. Der Sollgehalt dieser Lösungen beträgt 2,8 IE, 5,6 IE, 14,0 IE bzw. 28,0 IE Vitamin A je ml.
Von jeder Kalibrierlösung werden mehrmals 20 μl eingespritzt, und die mittleren Peakhöhen (-flächen) werden gemessen. Anhand der so ermittelten mittleren Peakhöhen (-flächen) und unter Berücksichtigung der Ergebnisse der UV-Kontrolle (Nummer 5.6.3.3) wird eine Kalibrationskurve erstellt.
5.6.3. UV-Kontrolle der Standardlösungen
5.6.3.1. Vitamin-A-Acetat-Stammlösung
Von der Vitamin-A-Acetat-Stammlösung (Nummer 3.11.1) werden 2,0 ml in einen 50-ml-Messkolben (Nummer 4.2.2) pipettiert, und es wird mit 2-Propanol (Nummer 3.8) zur Marke aufgefüllt. Der Sollgehalt dieser Lösung beträgt 56 IE Vitamin A je ml. Von dieser verdünnten Vitamin-A-Acetat-Lösung werden 3,0 ml in einen 25-ml-Messkolben pipettiert; es wird mit 2-Propanol (Nummer 3.8) zur Marke aufgefüllt. Der Sollgehalt dieser Lösung beträgt 6,72 IE Vitamin A je ml. Das UV-Spektrum dieser Lösung wird gegen 2-Propanol (Nummer 3.8) im Spektralfotometer (Nummer 4.6) zwischen 300 und 400 nm gemessen. Das Extinktionsmaximum muss zwischen 325 und 327 nm liegen.
Berechnung des Vitamin-A-Gehalts:
IE Vitamin A/ml = E326 × 19,0
(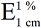 für Vitamin - A - Acetat = 1 530 bei 326 nm in 2-Propanol)
für Vitamin - A - Acetat = 1 530 bei 326 nm in 2-Propanol)
5.6.3.2. Vitamin-A-Palmitat-Stammlösung
Von der Vitamin-A-Palmitat-Stammlösung (Nummer 3.12.1) werden 2,0 ml in einen 50-ml-Messkolben (Nummer 4.2.2) pipettiert, und es wird mit 2-Propanol (Nummer 3.8) zur Marke aufgefüllt. Der Sollgehalt dieser Lösung beträgt 56 IE Vitamin A je ml. Von dieser verdünnten Vitamin-A-Palmitat-Lösung werden 3,0 ml in einen 25-ml-Messkolben pipettiert; es wird zur Marke mit 2-Propanol (Nummer 3.8) aufgefüllt. Der Sollgehalt dieser Lösung beträgt 6,72 IE Vitamin A je ml. Das UV-Spektrum dieser Lösung wird gegen 2-Propanol (Nummer 3.8) im Spektralfotometer (Nummer 4.6) zwischen 300 und 400 nm gemessen. Das Extinktionsmaximum muss zwischen 325 und 327 nm liegen.
Berechnung des Vitamin-A-Gehalts:
IE Vitamin A/ml = E326 × 19,0
(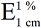 für Vitamin - A - Palmitat = 957 bei 326 nm in 2-Propanol)
für Vitamin - A - Palmitat = 957 bei 326 nm in 2-Propanol)
5.6.3.3. Vitamin-A-Gebrauchsstandardlösung
Von der gemäß Nummer 5.6.1 hergestellten, unverdünnten Vitamin-A-Gebrauchsstandardlösung werden 3,0 ml in einen 50-ml-Messkolben (Nummer 4.2.2) pipettiert, und es wird mit 2-Propanol (Nummer 3.8) zur Marke aufgefüllt. 5,0 ml dieser Lösung werden in einen 25-ml-Messkolben pipettiert; es wird mit 2-Propanol (Nummer 3.8) zur Marke aufgefüllt. Der Sollgehalt dieser Lösung beträgt 6,72 IE Vitamin A je ml. Das UV-Spektrum dieser Lösung wird gegen 2-Propanol (Nummer 3.8) im Spektralfotometer (Nummer 4.6) zwischen 300 und 400 nm gemessen. Das Extinktionsmaximum muss zwischen 325 und 327 nm liegen.
Berechnung des Vitamin-A-Gehalts:
IE Vitamin A/ml = E325 × 18,30
(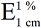 für Vitamin - A - Alkohol = 1 821 bei 325 nm in 2-Propanol)
für Vitamin - A - Alkohol = 1 821 bei 325 nm in 2-Propanol)
6. Berechnung der Ergebnisse
Aus der mittleren Höhe (Fläche) der Vitamin-A-Peaks der Probenlösung wird anhand der Kalibrationskurve (Nummer 5.6.2) die Konzentration der Probenlösung in IE/ml bestimmt.
Der Vitamin-A-Gehalt w (in IE/kg) der Probe wird nach folgender Formel berechnet:
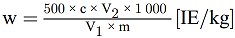
wobei:
| c = | Vitamin-A-Konzentration der Probenlösung (Nummer 5.4) in IE/ml, |
| V1 = | Volumen der Probenlösung (Nummer 5.4) in ml, |
| V2 = | Volumen des unter 5.4 entnommenen aliquoten Teils in ml, |
| m = | Probeneinwaage in g. |
7. Bemerkungen
7.1. Bei Proben mit niedriger Vitamin-A-Konzentration kann es zweckmäßig sein, die Petroletherextrakte von zwei Verseifungsansätzen (Einwaage 25 g) zu einer Probenlösung für die HPLC-Bestimmung zu vereinigen.
7.2. Die Einwaage für die Analyse darf höchstens 2 g Fett enthalten.
7.3. Bei schlechter Phasentrennung können etwa 10 ml Ethanol (Nummer 3.1) zur Zerstörung der Emulsion zugegeben werden.
7.4. Bei Lebertran oder anderen reinen Fetten ist die Verseifungsdauer auf 45 bis 60 min zu erhöhen.
7.5. Statt BHT kann Hydrochinon verwendet werden.
7.6. Bei Verwendung einer Normalphasensäule ist die Trennung der Retinolisomeren möglich. Allerdings müssen in diesem Fall für die Berechnungen die Peakhöhen (-flächen) aller cis- und trans-Isomeren addiert werden.
7.7. Statt Natriumascorbat-Lösung können etwa 150 mg Ascorbinsäure verwendet werden.
7.8. Statt Natriumsulfid-Lösung können etwa 50 mg EDTA verwendet werden.
7.9. Bei der Bestimmung des Gehalts an Vitamin A in Milchaustausch-Futtermitteln sind folgende Aspekte zu berücksichtigen:
Um festzustellen, ob die angewandte Analysemethode zuverlässige Ergebnisse für diese spezifische Matrix (Milchaustausch-Futtermittel) liefert, ist ein Wiederfindungstest an einer weiteren Probeneinwaage durchzuführen. Ist die Wiederfindungsrate kleiner als 80 %, muss das Analyseergebnis um die Wiederfindung korrigiert werden.
8. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 15 % des höheren Werts nicht überschreiten.
9.Ergebnisse eines Ringversuchs 2
| Vormischungen | Fertigfutter-vormischungen | Mineralfutter | Eiweißkonzentrat | Ferkelaufzuchtfutter | |||||||||||||||||
| L | 13 | 12 | 13 | 12 | 13 | ||||||||||||||||
| n | 48 | 45 | 47 | 46 | 49 | ||||||||||||||||
| Mittelwert [IE/kg] | 17,02 × 106 | 1,21 × 106 | 537.100 | 151.800 | 18.070 | ||||||||||||||||
| sr [IE/kg] | 0,51 × 106 | 0,039 × 106 | 22.080 | 12.280 | 682 | ||||||||||||||||
| r [IE/kg] | 1,43 × 106 | 0,109 × 106 | 61.824 | 34.384 | 1.910 | ||||||||||||||||
| VKr [%] | 3,0 | 3,5 | 4,1 | 8,1 | 3,8 | ||||||||||||||||
| sR [IE/kg] | 1,36 × 106 | 0,069 × 106 | 46.300 | 23.060 | 3.614 | ||||||||||||||||
| R [IE/kg] | 3,81 × 106 | 0,193 × 106 | 129.640 | 64.568 | 10.119 | ||||||||||||||||
| VKR [%] | 8,0 | 6,2 | 8,6 | 15 | 20 | ||||||||||||||||
| |||||||||||||||||||||
Abbildung 1:
Extraktionsapparat (4.8)
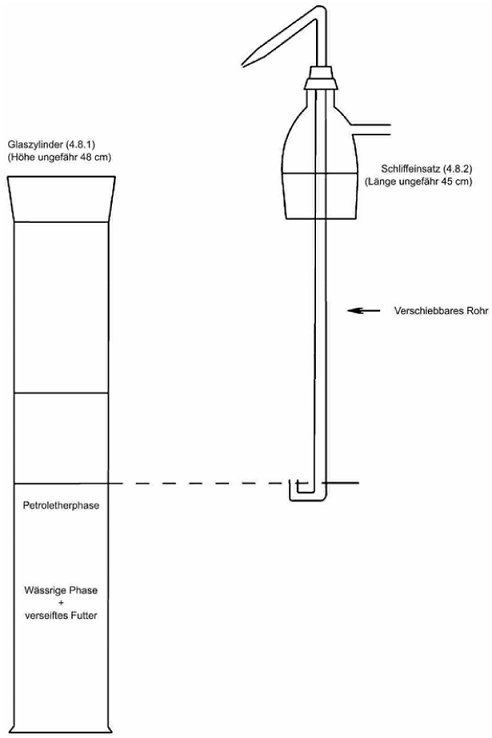
B. Bestimmung des Vitamin-E-Gehalts
Der Vitamin-E-Gehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Vitamin-E-Gehalts in Futtermitteln. Der Vitamin-E-Gehalt wird in mg DL-α-Tocopherol-Acetat je kg angegeben. 1 mg DL-α-Tocopherol-Acetat entspricht 0,91 mg DL-α-Tocopherol (Vitamin E).
Die Bestimmungsgrenze beträgt 2 mg Vitamin E/kg. Diese Grenze wird nur mit dem Fluoreszenzdetektor erreicht. Bei einem UV-Detektor beträgt die Bestimmungsgrenze 10 mg/kg.
2. Prinzip
Die Probe wird mit ethanolischer Kaliumhydroxidlösung hydrolysiert, und das Vitamin E wird mit Petrolether extrahiert. Das Lösungsmittel wird eingedampft; der Rückstand wird in Methanol gelöst und, falls notwendig, auf die erforderliche Konzentration verdünnt. Der Vitamin-E-Gehalt wird mittels Umkehrphasen-Hochleistungsflüssigkeitschromatografie (RP-HPLC) unter Verwendung eines UV- oder Fluoreszenzdetektors bestimmt.
3. Reagenzien
3.1. Ethanol, σ = 96 %.
3.2. Petrolether, Siedeintervall 40 bis 60 °C.
3.3. Methanol
3.4. Kaliumhydroxid-Lösung, c = 50 g/100 ml.
3.5. Natriumascorbat-Lösung, c = 10 g/100 ml (siehe Bemerkung 7.7).
3.6. Natriumsulfid, Na2S · x H2O (x = 7 bis 9).
3.6.1. Natriumsulfid-Lösung, c = 0,5 mol/l in Glycerin, β = 120 g/l (für x = 9) (siehe Bemerkung 7.8).
3.7. Phenolphthalein-Lösung, c = 2 g/100 ml in Ethanol (Nummer 3.1).
3.8. Mobile Phase für die HPLC: Mischung von Methanol (Nummer 3.3) und Wasser z.B. 980 + 20 (V+V) Das Mischungsverhältnis ist der jeweils verwendeten Säule anzupassen.
3.9. Stickstoff, sauerstofffrei.
3.10. DL-α-Tocopherol-Acetat, reinst, mit zertifizierter Aktivität
3.10.1. DL-α-Tocopherol-Acetat-Stammlösung: 100 mg DL-α-Tocopherol-Acetat (Nummer 3.10) auf 0,1 mg genau in einen 100-ml-Messkolben einwiegen. In Ethanol (Nummer 3.1) lösen und mit demselben Lösungsmittel zur Marke auffüllen. 1 ml dieser Lösung enthält 1 mg DL-α-Tocopherol-Acetat. (UV-Kontrolle siehe 5.6.1.3; Stabilisierung siehe Bemerkung 7.4).
3.11. DL-α-Tocopherol, reinst, mit zertifizierter Aktivität
3.11.1. DL-α-Tocopherol-Stammlösung: Von DL-α-Tocopherol (Nummer 3.11) werden 100 mg auf 0,1 mg genau in einen 100-ml Messkolben eingewogen. In Ethanol (Nummer 3.1) lösen und mit demselben Lösungsmittel zur Marke auffüllen. 1 ml dieser Lösung enthält 1 mg DL-α-Tocopherol. (UV-Kontrolle siehe 5.6.2.3; Stabilisierung siehe Bemerkung 7.4).
3.12. 2,6-Di-tert-butyl-4-methylphenol (BHT) (siehe Bemerkung 7.5).
4. Geräte
4.1. Rotationsfilmverdampfer.
4.2. Braunglasgeräte
4.2.1. Stehkolben oder Erlenmeyerkolben, 500 ml, mit Schliffhülse.
4.2.2. Messkolben mit Schliffstopfen, enghalsig, 10, 25, 100 und 500 ml.
4.2.3. Scheidetrichter, konische Form, 1.000 ml, mit Schliffstopfen.
4.2.4. Spitzkolben, 250 ml, mit Schliffhülsen.
4.3. Allihn-Rückflusskühler, Mantellänge 300 mm, Kernschliff mit Adapter für Gaseinleitung.
4.4. Phasentrennungsfaltenfilter, DurchmesS.r.1.5 mm (z.B. Schleicher & Schuell 597 HY 1/2).
4.5. HPLC-Einrichtung mit Injektionssystem
4.5.1. HPLC-Trennsäule, 250 mm × 4 mm, C18, 5 oder 10 μm Korngröße, oder vergleichbare Säule,
4.5.2. UV- oder Fluoreszenzdetektor mit variabler Wellenlängeneinstellung.
4.6. Spektralfotometer mit Quarz-Küvetten von 10 mm Schichtdicke.
4.7. Wasserbad mit Magnetrührer.
4.8. Extraktionsapparat (Abbildung 1) bestehend aus:
4.8.1. 1-l-Standzylinder mit Schliff und Schliffstopfen,
4.8.2. Schliffeinsatz mit Seitenarm und einem in der Höhe verschiebbaren Rohr in der Mitte. Das verschiebbare Rohr muss ein U-förmiges unteres Ende und eine Düse am entgegengesetzten Ende haben, sodass die obere Flüssigkeitsphase aus dem Zylinder in den Scheidetrichter überführt werden kann.
5. Verfahren
| Anmerkung: | Vitamin E ist empfindlich gegenüber Licht (UV-Strahlung) und Oxidation. Daher muss unter Ausschluss von Licht (Verwendung von Braunglasgeräten oder von mit Aluminiumfolie umhüllten Glasgeräten) und Sauerstoff (Stickstoffspülung) gearbeitet werden. Während der Extraktion muss das Luftpolster über der Flüssigkeit durch Stickstoff ersetzt werden (zur Vermeidung von Überdruck Stopfen immer wieder lüften). |
5.1. Vorbereitung der Probe
Die Probe wird unter Vermeidung von Erwärmung so fein vermahlen, dass sie ein Sieb mit 1 mm Maschenweite passieren kann. Das Mahlen darf erst unmittelbar vor dem Einwiegen und Verseifen erfolgen, da sonst Vitamin-E-Verluste auftreten können.
5.2. Verseifung
Je nach Vitamin-E-Gehalt 2 bis 25 g der Probe auf 0,01 g genau in einen 500-ml-Steh- oder Erlenmeyerkolben (Nummer 4.2.1) einwiegen. Nacheinander unter Schwenken 130 ml Ethanol (Nummer 3.1), etwa 100 mg BHT (Nummer 3.12), 2 ml Natriumascorbat-Lösung (Nummer 3.5) und 2 ml Natriumsulfid-Lösung (Nummer 3.6) zusetzen. Den Kolben mit dem Rückflusskühler (Nummer 4.3) verbinden und in ein Wasserbad mit Magnetrührer (Nummer 4.7) geben. Bis zum Sieden erhitzen und 5 min am Rückflusskühler kochen. Anschließend 25 ml Kaliumhydroxidlösung (Nummer 3.4) durch den Rückflusskühler (Nummer 4.3) zugeben, und unter ständigem Rühren und schwachem Stickstoffstrom 25 min weiterkochen. Den Kühler mit etwa 20 ml Wasser ausspülen und den Kolbeninhalt auf Zimmertemperatur abkühlen.
5.3. Extraktion
Die Verseifungslösung wird mit insgesamt 250 ml Wasser quantitativ in einen 1.000-ml-Scheidetrichter (Nummer 4.2.3) oder in den Extraktionsapparat (Nummer 4.8) überspült. Der Verseifungskolben wird mit 25 ml Ethanol (Nummer 3.1) und anschließend mit 100 ml Petrolether (Nummer 3.2) nachgewaschen, und die Spülflüssigkeiten werden ebenfalls in den Scheidetrichter oder den Extraktionsapparat überführt. Das Wasser/Ethanol-Verhältnis in den vereinigten Lösungen muss etwa 2:1 betragen. 2 min kräftig schütteln und dann 2 min absetzen lassen.
5.3.1. Extraktion mithilfe eines Scheidetrichters (Nummer 4.2.3)
Nach Phasentrennung (siehe Bemerkung 7.3) wird die Petroletherphase in einen anderen Scheidetrichter (Nummer 4.2.3) überführt. Diese Extraktion 2-mal mit je 100 ml Petrolether (Nummer 3.2) und 2-mal mit je 50 ml Petrolether (Nummer 3.2) wiederholen.
Die vereinigten Extrakte werden im Scheidetrichter unter leichtem Schwenken (Vermeidung von Emulsionsbildung) 2-mal mit jeweils 100 ml Wasser gespült und dann durch mehrmaliges Schütteln mit weiteren Portionen von 100 ml Wasser so oft gewaschen, bis das Waschwasser bei Zugabe von Phenolphthalein-Lösung (Nummer 3.7) farblos bleibt (4-maliges Waschen ist normalerweise ausreichend). Zur Entfernung eventuell suspendierten Wassers wird der gewaschene Extrakt durch einen trockenen Phasentrennungsfaltenfilter (Nummer 4.4) in einen 500-ml-Messkolben (Nummer 4.2.2) filtriert. Scheidetrichter und Filter mit 50 ml Petrolether (Nummer 3.2) nachwaschen, mit Petrolether (Nummer 3.2) zur Marke auffüllen und gut schütteln.
5.3.2. Extraktion mithilfe eines Extraktionsapparats (Nummer 4.8)
Nach Phasentrennung (siehe Bemerkung 7.3) wird der Stopfen des Standzylinders (Nummer 4.8.1) durch den Schliffeinsatz (Nummer 4.8.2) ersetzt und das verschiebbare Rohr so eingestellt, dass sich das U-förmige untere Ende gerade über dem Niveau der Grenzfläche befindet. Durch Druckausübung von einer am Seitenarm angebrachten Stickstoffleitung wird die obere Petroletherphase in einen 1.000-ml-Scheidetrichter (Nummer 4.2.3) überführt. 100 ml Petrolether (Nummer 3.2) werden in den Standzylinder gegeben, der mit einem Stopfen verschlossen und gründlich geschüttelt wird. Nach der Phasentrennung wird die obere Phase wie zuvor in den Scheidetrichter überführt. Diese Extraktion wird noch 1-mal mit 100 ml Petrolether (Nummer 3.2) und 2-mal mit je 50 ml Petrolether (Nummer 3.2) wiederholt, und die Petroletherphasen werden in den Scheidetrichter überführt.
Die vereinigten Petroletherextrakte, wie unter Nummer 5.3.1 erläutert, waschen und wie dort beschrieben weiterverfahren.
5.4. Vorbereitung der Probenlösung für die HPLC
Ein aliquoter Teil der Petrolether-Lösung (gemäß Nummer 5.3.1 oder 5.3.2) wird in einen 250-ml-Spitzkolben (Nummer 4.2.4) pipettiert. Das Lösungsmittel wird unter vermindertem Druck und bei einer Badtemperatur von höchstens 40 °C am Rotationsverdampfer (Nummer 4.1) fast bis zur Trockne eingedampft. Danach wird unter Stickstoff (Nummer 3.9) Druckausgleich geschaffen und der Kolben vom Rotationsverdampfer abgenommen. Das restliche Lösungsmittel wird im Stickstoffstrom (Nummer 3.9) abgeblasen, und der Rückstand wird sofort in einer definierten Menge (10 bis 100 ml) Methanol (Nummer 3.3) aufgenommen (die Konzentration von DL-α-Tocopherol muss etwa 5 bis 30 μg/ml betragen).
5.5. Bestimmung durch HPLC
Die Abtrennung von Vitamin E erfolgt mithilfe einer Umkehrphasen-C18-Säule (Nummer 4.5.1), und die Konzentration wird mithilfe eines Fluoreszenzdetektors (Anregung: 295 nm, Emission: 330 nm) oder eines UV-Detektors (292 nm) (Nummer 4.5.2) gemessen.
Hierzu wird ein aliquoter Teil (z.B. 20 μl) der nach Nummer 5.4 erhaltenen methanolischen Lösung auf die Trennsäule gegeben und mit der mobilen Phase (Nummer 3.8) eluiert. Die mittlere Peakhöhe (-fläche) von mehreren Einspritzungen derselben Probenlösung wird ermittelt. In gleicher Weise werden auch die mittleren Peakhöhen (-flächen) von mehreren Einspritzungen der Kalibrierlösungen (Nummer 5.6.2) bestimmt.
HPLC-Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen:
| HPLC-Trennsäule (Nummer 4.5.1): | 250 mm × 4 mm, C18, 5 oder 10 μm Korngröße, oder vergleichbare Säule |
| Mobile Phase (Nummer 3.8): | Mischung von Methanol (Nummer 3.3) und Wasser z.B. 980 + 20 (V+V). |
| Durchflussrate: | 1 bis 2 ml/min |
| Detektor (Nummer 4.5.2) | Fluoreszenzdetektor (Anregung: 295 nm; Emission: 330 nm) oder UV-Detektor (292 nm) |
5.6. Kalibrierung (DL-α-Tocopherol-Acetat oder DL-α-Tocopherol)
5.6.1. DL-α-Tocopherol-Acetat-Standard
5.6.1.1. Herstellen der Gebrauchsstandardlösung
Von der DL-α-Tocopherol-Acetat-Stammlösung (Nummer 3.10.1) werden 25 ml in einen 500-ml-Steh- oder Erlenmeyerkolben (Nummer 4.2.1) pipettiert und, wie unter 5.2 beschrieben, hydrolysiert. Anschließend mit Petrolether (Nummer 3.2) gemäß Nummer 5.3 extrahieren und mit Petrolether auf 500 ml auffüllen. Von diesem Extrakt werden 25 ml am Rotationsverdampfer (siehe 5.4) fast bis zur Trockne eingedampft. Das verbleibende Lösungsmittel wird im Stickstoffstrom (Nummer 3.9) abgeblasen, und der Rückstand wird in 25,0 ml Methanol (Nummer 3.3) aufgenommen. Der Sollgehalt dieser Lösung beträgt 45,5 μg DL-α-Tocopherol je ml; das entspricht 50,0 μg DL-α-Tocopherol-Acetat je ml. Die Gebrauchsstandardlösung muss vor Gebrauch frisch hergestellt werden.
5.6.1.2. Herstellen der Kalibrierlösungen und Erstellung der Kalibrationskurve
Von der Gebrauchsstandardlösung werden 1,0 ml, 2,0 ml, 4,0 ml bzw. 10,0 ml in jeweils einen 20-ml-Messkolben pipettiert; es wird mit Methanol (Nummer 3.3) zur Marke aufgefüllt und gemischt. Der Sollgehalt dieser Lösungen beträgt 2,5 μg/ml, 5,0 μg/ml, 10,0 μg/ml bzw. 25,0 μg/ml DL-α-Tocopherol-Acetat, d. h. 2,28 μg/ml, 4,55 μg/ml, 9,10 μg/ml bzw. 22,8 μg/ml DL-α-Tocopherol.
Von jeder Kalibrierlösung werden mehrmals 20 μl eingespritzt, und die mittleren Peakhöhen (-flächen) werden gemessen. Anhand der so ermittelten mittleren Peakhöhen (-flächen) wird eine Kalibrationskurve erstellt.
5.6.1.3. UV-Kontrolle der DL-α-Tocopherol-Acetat-Stammlösung (Nummer 3.10.1)
Von der DL-α-Tocopherol-Acetat-Stammlösung (Nummer 3.10.1) werden 5,0 ml mit Ethanol auf 25,0 ml aufgefüllt. Das UV-Spektrum dieser Lösung wird gegen Ethanol (Nummer 3.1) im Spektralfotometer (Nummer 4.6) zwischen 250 und 320 nm gemessen.
Das Extinktionsmaximum muss bei 284 nm liegen:
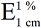 43,6 bei 284 nm in Ethanol
43,6 bei 284 nm in Ethanol
Bei der vorliegenden Verdünnung muss eine Extinktion von 0,84 bis 0,88 erzielt werden.
5.6.2. DL-α-Tocopherol-Standard
5.6.2.1. Herstellen der Gebrauchsstandardlösung
Von der DL-α-Tocopherol-Stammlösung (Nummer 3.11.1) werden 2 ml in einen 50-ml-Messkolben pipettiert und in Methanol (Nummer 3.3) gelöst; es wird mit Methanol zur Marke aufgefüllt. Der Sollgehalt dieser Lösung beträgt 40 μg DL-α-Tocopherol je ml; das entspricht 44,0 μg DL-α-Tocopherol-Acetat je ml. Die Gebrauchsstandardlösung muss vor Gebrauch frisch hergestellt werden.
5.6.2.2. Herstellen der Kalibrierlösungen und Erstellung der Kalibrationskurve
Von der Gebrauchsstandardlösung werden 1,0 ml, 2,0 ml, 4,0 ml bzw. 10,0 ml in jeweils einen 20-ml-Messkolben pipettiert; es wird mit Methanol (Nummer 3.3) zur Marke aufgefüllt und gemischt. Der Sollgehalt dieser Lösungen beträgt 2,0 μg/ml, 4,0 μg/ml, 8,0 μg/ml bzw. 20,0 μg/ml DL-α-Tocopherol, d. h. 2,20 μg/ml, 4,40 μg/ml, 8,79 μg/ml bzw. 22,0 μg/ml DL-α-Tocopherol-Acetat.
Von jeder Kalibrierlösung werden mehrmals 20 μl eingespritzt, und die mittleren Peakhöhen (-flächen) werden gemessen. Anhand der so ermittelten mittleren Peakhöhen (-flächen) wird eine Kalibrationskurve erstellt.
5.6.2.3. UV-Kontrolle der DL-α-Tocopherol-Stammlösung (Nummer 3.11.1)
Von der DL-α-Tocopherol-Stammlösung (Nummer 3.11.1) werden 2,0 ml mit Ethanol auf 25,0 ml aufgefüllt; das UV-Spektrum dieser Lösung wird gegen Ethanol (Nummer 3.1) im Spektralfotometer (Nummer 4.6) zwischen 250 und 320 nm gemessen. Das Extinktionsmaximum muss bei 292 nm liegen:
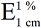 75,8 bei 292 nm in Ethanol
75,8 bei 292 nm in Ethanol
Bei der vorliegenden Verdünnung muss eine Extinktion von 0,6 erzielt werden.
6. Berechnung der Ergebnisse
Aus der mittleren Höhe (Fläche) der Vitamin-E-Peaks der Probenlösung wird anhand der Kalibrationskurve (Nummer 5.6.1.2 oder 5.6.2.2) die Konzentration der Probenlösung in μg/ml (berechnet als DL-α-Tocopherol-Acetat) bestimmt.
Der Vitamin-E-Gehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
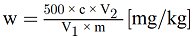
wobei:
| c = | Vitamin-E-Konzentration (als DL-α-Tocopherol-Acetat) der Probenlösung (Nummer 5.4) in μg/ml, |
| V1 = | Volumen der Probenlösung (Nummer 5.4) in ml, |
| V2 = | Volumen des unter 5.4 entnommenen aliquoten Teils in ml, |
| m = | Probeneinwaage in g. |
7. Bemerkungen
7.1. Bei Proben mit niedriger Vitamin-E-Konzentration kann es zweckmäßig sein, die Petroletherextrakte von zwei Verseifungsansätzen (Einwaage 25 g) zu einer Probenlösung für die HPLC-Bestimmung zu vereinigen.
7.2. Die Einwaage für die Analyse darf höchstens 2 g Fett enthalten.
7.3. Bei schlechter Phasentrennung können etwa 10 ml Ethanol (Nummer 3.1) zur Zerstörung der Emulsion zugegeben werden.
7.4. Nach der spektralfotometrischen Vermessung der DL-α-Tocopherol-Acetat- oder der DL-α-Tocopherol-Lösung nach Nummer 5.6.1.3 bzw. 5.6.2.3 empfiehlt es sich, der Lösung (Nummer 3.10.1 bzw. 3.10.2) etwa 10 mg BHT (Nummer 3.12) zuzusetzen und die Lösung im Kühlschrank aufzubewahren (Haltbarkeit höchstens 4 Wochen).
7.5. Statt BHT kann Hydrochinon verwendet werden.
7.6. Bei Verwendung einer Normalphasensäule ist die Trennung von α-, β-, γ- und δ-Tocopherol möglich.
7.7. Statt Natriumascorbat-Lösung können etwa 150 mg Ascorbinsäure verwendet werden.
7.8. Statt Natriumsulfid-Lösung können etwa 50 mg EDTA verwendet werden.
7.9 Vitamin-E-Acetat hydrolysiert unter alkalischen Bedingungen sehr schnell und ist deshalb sehr oxidationsanfällig, insbesondere in Gegenwart von Spurenelementen wie Eisen oder Kupfer. Bei der Bestimmung des Vitamin-E-Gehalts in Vormischungen, bei denen ein Gehalt von 5.000 mg/kg überschritten wird, könnte es zu einem Abbau von Vitamin E kommen. Deshalb wird zur Bestätigung eine HPLC-Methode mit einem enzymatischen Aufschluss der Vitamin-E-Formel ohne einen alkalischen Verseifungsschritt empfohlen.
8. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf 15 % des höheren Werts nicht überschreiten.
9. Ergebnisse eines Ringversuchs 4
| Vormischungen | Fertigfutter-vormischungen | Mineralfutter | Eiweißkonzentrat | Ferkelaufzuchtfutter | |||||||||||||||||
| L | 12 | 12 | 12 | 12 | 12 | ||||||||||||||||
| n | 48 | 48 | 48 | 48 | 48 | ||||||||||||||||
| Mittelwert [mg/kg] | 17.380 | 1.187 | 926 | 315 | 61,3 | ||||||||||||||||
| sr [mg/kg] | 384 | 45,3 | 25,2 | 13,0 | 2,3 | ||||||||||||||||
| r [mg/kg] | 1.075 | 126,8 | 70,6 | 36,4 | 6,4 | ||||||||||||||||
| VKr [%] | 2,2 | 3,8 | 2,7 | 4,1 | 3,8 | ||||||||||||||||
| sR [mg/kg] | 830 | 65,0 | 55,5 | 18,9 | 7,8 | ||||||||||||||||
| R [mg/kg] | 2.324 | 182,0 | 155,4 | 52,9 | 21,8 | ||||||||||||||||
| VKR [%] | 4,8 | 5,5 | 6,0 | 6,0 | 12,7 | ||||||||||||||||
| |||||||||||||||||||||
Abbildung 2:
Extraktionsapparat (4.8)
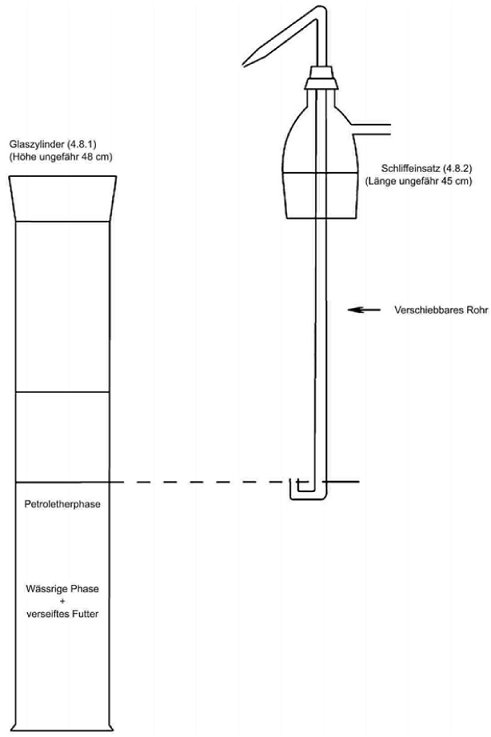
C. Bestimmung des Gehalts an den Spurenelementen Eisen, Kupfer, Mangan und Zink
Der Eisen-, Kupfer-, Mangan- und Zinkgehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Gehalts an den Spurenelementen Eisen, Kupfer, Mangan und Zink in Futtermitteln. 5 Die Bestimmungsgrenzen liegen bei:
2. Prinzip
Die Probe wird nach Zerstörung eventuell vorhandener organischer Substanz in Salzsäure gelöst. Die Elemente Eisen, Kupfer, Mangan und Zink werden nach entsprechender Verdünnung der Analysenlösung mittels Atomabsorptionsspektrometrie bestimmt.
3. Reagenzien
Vorbemerkungen
Das zur Herstellung der Reagenzien und Analysenlösungen verwendete Wasser muss "frei" von den zu bestimmenden Kationen sein, d. h., das Wasser muss entweder in einer Borsilikatglas- oder Quarzapparatur 2-fach destilliert oder durch doppelten Ionenaustausch gereinigt worden sein.
Die zur Analyse verwendeten Reagenzien müssen mindestens von analysenreiner Qualität sein. Die Abwesenheit des zu bestimmenden Elements wird mittels eines Blindversuchs kontrolliert. Falls erforderlich, sind die Reagenzien einer zusätzlichen Reinigung zu unterziehen.
Anstelle der nachfolgend beschriebenen Standardlösungen können auch handelsübliche Standardlösungen verwendet werden, deren Reinheit garantiert und vor der Verwendung kontrolliert wurde.
3.1. Salzsäure (D: 1,19 g/ml).
3.2. Salzsäure (6 mol/l).
3.3. Salzsäure (0,5 mol/l).
3.4. Fluorwasserstoffsäure (Volumenkonzentration = 38 bis 40 %); Eisengehalt: weniger als 1 mg/l; Glührückstand (als Sulfat): weniger als 10 mg/l.
3.5. Schwefelsäure (D: 1,84 g/ml).
3.6. Wasserstoffperoxid, ca. 100 Volumina Sauerstoff (Massenanteil = 30 %).
3.7. Eisen-Standardlösung (1.000 μg Fe/ml), wie folgt zubereitet, oder eine gleichwertige handelsübliche Lösung: 1 g Eisendraht wird in 200 ml 6 mol/l Salzsäure (Nummer 3.2) gelöst. Es werden 16 ml Wasserstoffperoxid (Nummer 3.6) zugegeben; dann wird mit Wasser auf 1 l aufgefüllt:
3.7.1. Eisen-Gebrauchsstandardlösung (100 μg Fe/ml): Die Standardlösung (Nummer 3.7) wird im Verhältnis 1:9 mit Wasser verdünnt.
3.8. Kupfer-Standardlösung (1.000 μg Cu/ml), wie folgt zubereitet, oder eine gleichwertige handelsübliche Lösung:
3.8.1. Kupfer-Gebrauchsstandardlösung (10 μg Cu/ml): Die Standardlösung (Nummer 3.8) wird im Verhältnis 1:9 mit Wasser verdünnt; anschließend wird die so entstandene Lösung wiederum im Verhältnis 1:9 mit Wasser verdünnt.
3.9. Mangan-Standardlösung (1.000 μg Mn/ml), wie folgt zubereitet, oder eine gleichwertige handelsübliche Lösung:
3.9.1. Mangan-Gebrauchsstandardlösung (10 μg Mn/ml): Die Standardlösung (Nummer 3.9) wird im Verhältnis 1:9 mit Wasser verdünnt; anschließend wird die so entstandene Lösung wiederum im Verhältnis 1:9 mit Wasser verdünnt.
3.10. Zink-Standardlösung (1.000 μg Zn/ml), wie folgt zubereitet, oder eine gleichwertige handelsübliche Lösung:
3.10.1. Zink-Gebrauchsstandardlösung (10 μg Zn/ml): Die Standardlösung (Nummer 3.10) wird im Verhältnis 1:9 mit Wasser verdünnt; anschließend wird die so entstandene Lösung wiederum im Verhältnis 1:9 mit Wasser verdünnt.
3.11. Lanthanchloridlösung: In 150 ml Wasser wird 12 g Lanthanoxid gelöst und 100 ml 6 mol/l Salzsäure (Nummer 3.2) zugegeben. Dann wird mit Wasser auf 1 l aufgefüllt.
4. Geräte
4.1. Muffelofen mit Regelvorrichtung und gegebenenfalls mit Temperaturanzeige.
4.2. Glasgeräte müssen aus resistentem Borsilikatglas sein. Es wird empfohlen, Glasgeräte zu benutzen, die ausschließlich der Bestimmung des Gehalts an Spurenelementen vorbehalten bleiben.
4.3. Atomabsorptions-Spektralfotometer; das Gerät muss innerhalb des vorgesehenen Messbereichs hinsichtlich seiner Empfindlichkeit und Genauigkeit den Anforderungen der jeweiligen Methode genügen.
5.1. Proben mit organischen Bestandteilen
5.1.1. Veraschung und Herstellung der Analysenlösung 7
5.1.1.1. Von der Probe werden 5 bis 10 g (auf 0,2 mg genau abgewogen) in eine Quarz- oder Platinschale gegeben (siehe Anmerkung b) und im Trockenschrank bei 105 °C getrocknet; dann wird die Schale in den kalten Muffelofen (Nummer 4.1) verbracht. Der Ofen wird geschlossen (siehe Anmerkung c) und die Temperatur innerhalb von ca. 90 min langsam auf 450 bis 475 °C erhöht. Diese Temperatur wird 4 bis 16 h (z.B. über Nacht) aufrechterhalten, um Kohleteilchen zu entfernen; dann wird der Ofen geöffnet und abkühlen gelassen (siehe Anmerkung d).
Die Asche wird mit Wasser angefeuchtet und in ein 250-ml-Becherglas gegeben. Die Schale wird mit insgesamt etwa 5 ml Salzsäure (Nummer 3.1) ausgespült, die anschließend langsam und vorsichtig (da es aufgrund von CO2-Bildung eventuell zu einer heftigen Reaktion kommen kann) in das Becherglas gegeben wird. Unter Schütteln wird Salzsäure (Nummer 3.1) tropfenweise zugegeben, bis die Schaumbildung aufhört. Die Salzsäure wird unter gelegentlichem Umrühren mit einem Glasstab bis zur Trockne abgedampft.
Dem Rückstand werden 15 ml 6 mol/l Salzsäure (Nummer 3.2) und anschließend etwa 120 ml Wasser zugefügt. Umgerührt wird mit dem Glasstab, der in dem Becherglas zu belassen ist. Letzteres wird mit einem Uhrglas abgedeckt. Die Flüssigkeit wird langsam zum Sieden gebracht und so lange im Sieden gehalten, bis die Asche vollständig gelöst ist. Dann wird durch ein aschefreies Filterpapier filtriert und das Filtrat in einem 250-ml-Messkolben aufgefangen. Das Becherglas und der Filter werden mit 5 ml heißer 6 mol/l Salzsäure (Nummer 3.2) und 2-mal mit kochendem Wasser ausgewaschen. Anschließend wird der Messkolben mit Wasser zur Marke aufgefüllt (HCl-Konzentration etwa 0,5 mol/l).
5.1.1.2. Sollte der Filterrückstand schwarz aussehen (Kohlenstoff), so wird er im Trockenschrank abermals bei 450 bis 475 °C verascht. Diese Veraschung, die nur wenige Stunden erfordert (etwa 3 bis 5 h) ist abgeschlossen, wenn die Asche weiß oder nahezu weiß aussieht. Der Rückstand wird mit etwa 2 ml Salzsäure (Nummer 3.1) aufgenommen, zur Trockne eingedampft und mit 5 ml 6 mol/l Salzsäure (Nummer 3.2) versetzt. Nach dem Erwärmen wird die Lösung in den Messkolben filtriert, und Letzterer mit Wasser zur Marke aufgefüllt (HCl-Konzentration etwa 0,5 mol/l).
Anmerkungen:
5.1.2. Spektralfotometrische Bestimmung
5.1.2.1. Herstellen der Kalibrierlösungen
Aus den Gebrauchsstandardlösungen 3.7.1, 3.8.1, 3.9.1 und 3.10.1 werden für jedes der zu bestimmenden Spurenelemente eine Reihe von Kalibrierlösungen hergestellt. Jede dieser Kalibrierlösungen hat eine HCl-Konzentration von etwa 0,5 mol/l und (im Falle von Eisen, Mangan und Zink) einen Lanthanchlorid-Gehalt, der einer Massenkonzentration von 0,1 % La (w/v) entspricht.
Die gewählten Spurenelementkonzentrationen müssen im Empfindlichkeitsbereich des verwendeten Spektralfotometers liegen. Die nachfolgenden Tabellen zeigen Beispiele für die Zusammensetzung typischer Reihen von Kalibrierlösungen. Je nach Typ und Empfindlichkeit des verwendeten Spektralfotometers kann es jedoch erforderlich sein, für die Kalibrierlösungen eine andere Konzentration zu wählen.
Eisen
| µg Fe/ml | 0 | 0,5 | 1 | 2 | 3 | 4 | 5 |
| ml Gebrauchsstandardlösung (Nummer 3.7.1) (1 ml = 100 μg Fe) | 0 | 0,5 | 1 | 2 | 3 | 4 | 5 |
| ml HCl (Nummer 3.2) | 7 | 7 | 7 | 7 | 7 | 7 | 7 |
| 10 ml Lanthanchloridlösung (Nummer 3.11) zugeben und mit Wasser auf 100 ml auffüllen. | |||||||
Kupfer
| µg Cu/ml | 0 | 0,1 | 0,2 | 0,4 | 0,6 | 0,8 | 1,0 |
| ml Gebrauchsstandardlösung (Nummer 3.8.1) (1 ml = 10 μg Cu) | 0 | 1 | 2 | 4 | 6 | 8 | 10 |
| ml HCl (Nummer 3.2) | 8 | 8 | 8 | 8 | 8 | 8 | 8 |
Mangan
| µg Mn/ml | 0 | 0,1 | 0,2 | 0,4 | 0,6 | 0,8 | 1,0 |
| ml Gebrauchsstandardlösung (Nummer 3.9.1) (1 ml = 10 μg Mn) | 0 | 1 | 2 | 4 | 6 | 8 | 10 |
| ml HCl (Nummer 3.2) | 7 | 7 | 7 | 7 | 7 | 7 | 7 |
| 10 ml Lanthanchloridlösung (Nummer 3.11) zugeben und mit Wasser auf 100 ml auffüllen. | |||||||
Zink
| µg Zn/ml | 0 | 0,05 | 0,1 | 0,2 | 0,4 | 0,6 | 0,8 |
| ml Gebrauchsstandardlösung (Nummer 3.10.1) (1 ml = 10 μg Zn) | 0 | 0,5 | 1 | 2 | 4 | 6 | 8 |
| ml HCl (Nummer 3.2) | 7 | 7 | 7 | 7 | 7 | 7 | 7 |
| 10 ml Lanthanchloridlösung (Nummer 3.11) zugeben und mit Wasser auf 100 ml auffüllen. | |||||||
5.1.2.2. Herstellen der Analysenlösung
Für die Bestimmung des Kupfergehalts kann die nach Nummer 5.1.1 hergestellte Analysenlösung in der Regel direkt verwendet werden. Gegebenenfalls wird ein aliquoter Teil dieser Analysenlösung in einen 100-ml-Messkolben pipettiert und mit 0,5 mol/l Salzsäure (Nummer 3.3) zur Marke aufgefüllt, um ihre Konzentration in den Bereich der Kalibrierlösungen zu bringen.
Für die Bestimmung des Gehalts an Eisen, Mangan und Zink wird ein aliquoter Teil der nach Nummer 5.1.1 hergestellten Lösung in einen 100-ml-Messkolben pipettiert. Es werden 10 ml Lanthanchloridlösung (Nummer 3.11) zugegeben und mit 0,5 mol/l Salzsäure (Nummer 3.3) zur Marke aufgefüllt (siehe Bemerkung 8).
5.1.2.3. Blindversuch
Es wird ein Blindversuch ausgeführt, der alle Verfahrensschritte umfassen muss, nur dass das Probematerial selbst weggelassen wird. Die Kalibrierlösung "0" ersetzt nicht den Blindversuch.
5.1.2.4. Messung der Atomabsorption
Die Atomabsorption der Kalibrierlösungen und der Analysenlösungen ist mit oxydierender Luft-Azetylen-Flamme bei folgenden Wellenlängen zu messen:
| Fe: 248,3 nm |
| Cu: 324,8 nm |
| Mn: 279,5 nm |
| Zn: 213,8 nm |
| Jede Messung ist 4-mal auszuführen. |
5.2. Mineralfutter
Enthält die Probe keine organischen Substanzen, so erübrigt sich eine vorherige Veraschung. In diesem Fall wird dann ab Nummer 5.1.1.1 zweiter Absatz weiter verfahren. Ein Abrauchen mit Fluorwasserstoffsäure kann entfallen.
6. Berechnung der Ergebnisse
Die Spurenelementkonzentration in der Analysenlösung wird mithilfe einer Kalibrationskurve berechnet und das Ergebnis in mg Spurenelement/kg der Probe (ppm) ausgedrückt.
7. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen eines Analytikers bei ein und derselben Probe darf die folgenden Werte nicht überschreiten:
8. Bemerkung
Das Vorhandensein von größeren Phosphatmengen kann die Bestimmung des Gehalts an Eisen, Mangan und Zink beeinträchtigen. Diese Interferenzen sind durch die Zugabe von Lanthanchloridlösung (Nummer 3.11) zu korrigieren. Weist die Probe jedoch das Gewichtsverhältnis Ca + Mg/P > 2 auf, kann auf die Zugabe von Lanthanchloridlösung (Nummer 3.11) zu der Analysenlösung und den Kalibrierlösungen verzichtet werden.
D. Bestimmung des Halofuginongehalts
DL-trans-7-Brom-6-chlor-3-[3-(3-hydroxy-2-piperidyl)acetonyl]-4(3H)-chinazolinon-hydrobromid
Der Halofuginongehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Halofuginongehalts von Futtermitteln. Die Bestimmungsgrenze beträgt 1 mg/kg.
2. Prinzip
Nach der Behandlung mit heißem Wasser wird Halofuginon als freie Base mit Ethylacetat extrahiert und anschließend durch Ausschütteln mit Salzsäure in das Hydrochlorid überführt. Der Extrakt wird durch Ionenaustauschchromatografie gereinigt. Der Halofuginongehalt wird mittels Umkehrphasen-Hochleistungsflüssigkeitschromatografie (HPLC) unter Verwendung eines UV-Detektors bestimmt.
3. Reagenzien
3.1. Acetonitril, HPLC-Qualität.
3.2. Amberlite XAD-2-Harz.
3.3. Ammoniumacetat.
3.4. Ethylacetat.
3.5. Essigsäure (Eisessig).
3.6. Halofuginon-Standardsubstanz: DL-trans-7-Brom-6-chlor-3-[3-(3-hydroxy-2-piperidyl)acetonyl]-4(3H)-chinazolinon-hydrobromid, E 764
3.6.1. Halofuginon-Standard-Stammlösung, 100 mg/ml
Von Halofuginon (Nummer 3.6) werden 50 mg auf 0,1 mg genau in einen 500-ml-Messkolben eingewogen und in Ammoniumacetat-Pufferlösung (Nummer 3.18) gelöst. Es wird mit der Pufferlösung zur Marke aufgefüllt und gemischt. Diese Lösung ist 3 Wochen haltbar, wenn sie im Dunkeln bei 5 °C aufbewahrt wird.
3.6.2. Kalibrierlösungen
Von der Standard-Stammlösung (Nummer 3.6.1) werden 1,0, 2,0, 3,0, 4,0 bzw. 6,0 ml jeweils in einen 100-ml-Messkolben überführt. Es wird mit der mobilen Phase (Nummer 3.21) zur Marke aufgefüllt und durchmischt. Diese Lösungen enthalten Halofuginon in Konzentrationen von 1,0, 2,0, 3,0, 4,0 bzw. 6,0 μg/ml. Die Lösungen müssen vor Gebrauch frisch hergestellt werden.
3.7. Salzsäure (ρ20 = ca. 1,16 g/ml).
3.8. Methanol
3.9. Silbernitrat.
3.10. Natriumascorbat.
3.11. Natriumcarbonat (Soda).
3.12. Natriumchlorid.
3.13. EDTA (Ethylendiamintetraessigsäure, Dinatriumsalz).
3.14. Wasser, HPLC-Qualität.
3.15. Natriumcarbonatlösung, c = 10 g/100 ml.
3.16. Mit Natriumchlorid gesättigte Natriumcarbonatlösung, c = 5 g/100 ml
50 g Natriumcarbonat (Nummer 3.11) werden in Wasser gelöst und auf 1 l verdünnt; dann wird Natriumchlorid (Nummer 3.12) zugegeben, bis die Lösung gesättigt ist.
3.17. Salzsäure, ca. 0,1 mol/l
10 ml Salzsäure (Nummer 3.7) werden mit Wasser auf 1 l verdünnt.
3.18. Ammoniumacetat-Pufferlösung, ca. 0,25 mol/l
19,3 g Ammoniumacetat (Nummer 3.3) und 30 ml Essigsäure (Nummer 3.5) werden in Wasser (Nummer 3.14) gelöst und auf 1 l verdünnt.
3.19. Vorbereitung des Amberlite XAD-2-Harzes
Eine ausreichende Menge Amberlite (Nummer 3.2) wird mit Wasser chloridfrei gewaschen. Die Prüfung der Waschflüssigkeit erfolgt mit Silbernitratlösung (Nummer 3.20). Danach wird das Harz mit 50 ml Methanol (Nummer 3.8) gewaschen. Das Methanol wird verworfen und das Harz in frischem Methanol aufbewahrt.
3.20. Silbernitratlösung, ca. 0,1 mol/l
0,17 g Silbernitrat (Nummer 3.9) werden in 10 ml Wasser gelöst.
3.21. Mobile Phase für die HPLC:
500 ml Acetonitril (Nummer 3.1) werden mit 300 ml Ammoniumacetat-Pufferlösung (Nummer 3.18) und 1.200 ml Wasser (Nummer 3.14) gemischt. Der pH-Wert wird mit Essigsäure (Nummer 3.5) auf 4,3 eingestellt. Die Lösung wird durch einen 0,22-μm-Filter (Nummer 4.8) filtriert und entgast (z.B. durch 10-minütige Ultraschallbehandlung). Diese Lösung ist 1 Monat lang haltbar, wenn sie in einem verschlossenen Gefäß im Dunkeln aufbewahrt wird.
4. Geräte
4.1. Ultraschallbad.
4.2. Rotationsfilmverdampfer.
4.3. Zentrifuge.
4.4. HPLC-Einrichtung mit UV-Detektor mit variabler Wellenlängeneinstellung oder Diodenarray-Detektor
4.4.1. HPLC-Trennsäule, 300 mm × 4 mm, C18, 10 μm Korngröße, oder vergleichbare Säule.
4.5. Glassäule (300 mm × 10 mm) mit gesintertem Glasfilter und Absperrhahn.
4.6. Glasfaserfilter, 150 mm Durchmesser.
4.7. Membranfilter, 0,45 μm Porengröße.
4.8. Membranfilter, 0,22 μm Porengröße.
5. Verfahren
| Anmerkung: | Halofuginon ist als freie Base in Alkali- und Ethylacetat-Lösungen instabil. Es darf höchstens 30 min in Ethylacetat bleiben. |
5.1. Allgemeines
5.1.1. Zur Prüfung, dass weder Halofuginon noch Störsubstanzen vorhanden sind, ist eine Blindprobe zu untersuchen.
5.1.2. Die Wiederfindungsrate wird ermittelt, indem eine Blindprobe untersucht wird, die mit Halofuginon angereichert wurde. Die zugesetzte Menge an Halofuginon sollte der in der Probe vorhandenen Menge entsprechen. Zur Anreicherung auf einen Gehalt von 3 mg/kg werden 300 μl der Standard-Stammlösung (Nummer 3.6.1) zu 10 g der Blindprobe gegeben. Es wird gemischt und 10 min gewartet, bevor mit der Extraktion (Nummer 5.2) fortgefahren wird.
| Anmerkung: | Für den Zweck dieser Methode muss die Blindprobe ähnlich zusammengesetzt sein wie die zu untersuchende Probe, und Halofuginon darf nicht nachweisbar sein. |
5.2. Extraktion
Von der vorbereiteten Probe werden 10 g auf 0,1 g genau in ein 200-ml-Zentrifugenglas eingewogen. Es werden 0,5 g Natriumascorbat (Nummer 3.10), 0,5 g EDTA (Nummer 3.13) und 20 ml Wasser hinzugefügt, und es wird gemischt. Das Zentrifugenglas wird 5 min in ein 80 °C heißes Wasserbad gestellt. Nach dem Abkühlen auf Raumtemperatur werden 20 ml Natriumcarbonatlösung (Nummer 3.15) hinzugefügt, und es wird gemischt. Unmittelbar danach werden 100 ml Ethylacetat (Nummer 3.4) hinzugefügt, und es wird 15 s kräftig von Hand geschüttelt. Danach wird das Zentrifugenglas mit gelockertem Stopfen 3 min in ein Ultraschallbad (Nummer 4.1) gestellt. Es wird 2 min zentrifugiert und die Ethylacetatphase durch einen Glasfaserfilter (Nummer 4.6) in einen 500-ml-Scheidetrichter dekantiert. Die Extraktion der Probe wird mit weiteren 100 ml Ethylacetat wiederholt. Die vereinigten Extrakte werden 1 min lang mit 50 ml der mit Natriumchlorid gesättigten Natriumcarbonatlösung (Nummer 3.16) gewaschen. Die wässrige Phase wird verworfen.
Die organische Phase wird 1 min mit 50 ml Salzsäure (Nummer 3.17) extrahiert. Die untere Säurephase wird in einen 250-ml-Scheidetrichter abgelassen. Die organische Phase wird erneut 1,5 min mit weiteren 50 ml Salzsäure extrahiert. Die beiden Säureextrakte werden vereinigt und durch ca. 10 s langes Schütteln mit 10 ml Ethylacetat (Nummer 3.4) gewaschen.
Die wässrige Phase wird quantitativ in einen 250-ml-Rundkolben überführt und die organische Phase verworfen. Das restliche in der sauren Lösung enthaltene Ethylacetat wird mithilfe des Rotationsverdampfers (Nummer 4.2) entfernt. Die Temperatur des Wasserbads darf 40 °C nicht überschreiten. Bei einem Unterdruck von ca. 25 mbar wird das restliche Ethylacetat bei 38 °C innerhalb von 5 min entfernt.
5.3. Clean-up
5.3.1. Vorbereitung der Amberlitesäule
Für jeden Probenextrakt wird eine XAD-2-Säule vorbereitet. Von dem vorbereiteten Amberlite (Nummer 3.19) werden 10 g mit Methanol (Nummer 3.8) in eine Glassäule (Nummer 4.5) eingefüllt. Auf das obere Ende des Harzbettes wird ein kleiner Glaswattebausch gebracht. Das Methanol wird aus der Säule ablaufen gelassen und das Harz mit 100 ml Wasser gewaschen. Sobald die Flüssigkeit das obere Ende des Harzbettes erreicht hat, wird der Absperrhahn geschlossen. Vor Gebrauch ist die Säule 10 min zu äquilibrieren. Die Säule darf nie trockenlaufen.
5.3.2. Clean-up der Probe
Der Extrakt (Nummer 5.2) wird quantitativ auf die vorbereitete Amberlitesäule (Nummer 5.3.1) aufgebracht und eluiert. Das Eluat wird verworfen. Die Elutionsgeschwindigkeit darf 20 ml/min nicht überschreiten. Der Rundkolben wird mit 20 ml Salzsäure (Nummer 3.17) gespült und die Austauschersäule mit der Spülflüssigkeit gewaschen. Die eventuell auf der Säule verbliebene saure Lösung wird mit einem Luftstrom restlos ausgeblasen. Die Waschlösungen werden verworfen. Es werden 100 ml Methanol (Nummer 3.8) auf die Säule gegeben und ein Eluat von 5 bis 10 ml in einem 250-ml-Rundkolben aufgefangen. Das restliche Methanol wird 10 min lang zur Äquilibrierung auf dem Harz belassen; anschließend wird die Elution mit einer Elutionsgeschwindigkeit von höchstens 20 ml/min fortgesetzt und das Eluat in demselben Rundkolben aufgefangen. Das Methanol wird am Rotationsverdampfer (Nummer 4.2) abgedampft, wobei die Temperatur des Wasserbads 40 °C nicht übersteigen darf. Der Rückstand wird unter Verwendung der mobilen Phase (Nummer 3.21) quantitativ in einen 10-ml-Messkolben überführt. Es wird mit der mobilen Phase zur Marke aufgefüllt und gemischt. Ein aliquoter Teil wird durch einen Membranfilter (Nummer 4.7) filtriert. Diese Lösung wird für die HPLC-Bestimmung (Nummer 5.4) aufbewahrt.
5.4. HPLC-Bestimmung
5.4.1. Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen:
| HPLC-Trennsäule (Nummer 4.4.1), |
| Mobile Phase für die HPLC (Nummer 3.21), |
| Durchflussrate: 1,5 bis 2 ml/min |
| Detektionswellenlänge: 243 nm |
| Einspritzvolumen: 40 bis 100 μl. |
Die Stabilität des chromatografischen Systems wird überprüft, indem die Kalibrierlösung (Nummer 3.6.2), die 3,0 μg/ml enthält, mehrmals eingespritzt wird, bis konstante Peakhöhen (-flächen) und Retentionszeiten erreicht sind.
5.4.2. Erstellung der Kalibrationskurve
Jede Kalibrierlösung (Nummer 3.6.2) wird mehrmals eingespritzt, und die Peakhöhen (-flächen) für die einzelnen Konzentrationen werden gemessen. Es wird eine Kalibrationskurve gezeichnet, indem die mittleren Peakhöhen oder -flächen auf der Ordinate und die dazugehörigen Konzentrationen in μg/ml auf der Abszisse aufgetragen werden.
5.4.3. Bestimmung der Probenlösung
Der Probenextrakt (Nummer 5.3.2) wird mehrmals eingespritzt, wobei dasselbe Volumen wie für die Einspritzung der Kalibrierlösungen verwendet wird, und die mittlere Peakhöhe (-fläche) der Halofuginonpeaks wird ermittelt.
6. Berechnung der Ergebnisse
Aus der mittleren Peakhöhe (-fläche) der Halofuginonpeaks der Probenlösung wird anhand der Kalibrationskurve (Nummer 5.4.2) die Konzentration der Probenlösung in μg/ml bestimmt.
Der Halofuginongehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
w = (c × 10) / m
wobei:
| c =: | Halofuginonkonzentration der Probenlösung in μg/ml, |
| m =: | Probeneinwaage in g. |
7. Überprüfung der Ergebnisse
7.1. Identität
Die Identität des Analyten kann durch Co-Chromatografie oder mithilfe eines Diodenarray-Detektors bestätigt werden, wobei die Spektren der Probenlösung und der Kalibrierlösung (Nummer 3.6.2), die 6,0 μg/ml enthält, verglichen werden.
7.1.1. Co-Chromatografie
Eine Probenlösung wird mit einer geeigneten Menge einer Kalibrierlösung (Nummer 3.6.2) versetzt. Die Menge des zugesetzten Halofuginons muss dem erwarteten Halofuginongehalt der Probenlösung entsprechen.
Unter Berücksichtigung der zugesetzten Menge und der Verdünnung des Extrakts darf nur die Höhe des Halofuginonpeaks vergrößert sein. Die Peakbreite in halber Höhe darf höchstens ± 10 % von der des Peaks der nicht angereicherten Probenlösung abweichen.
7.1.2. Diodenarray-Detektion
Die Ergebnisse werden gemäß den nachstehenden Kriterien beurteilt:
Wird eines dieser Kriterien nicht erfüllt, gilt das Vorhandensein des Analyten als nicht bestätigt.
7.2. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf bei einem Halofuginongehalt von bis zu 3 mg/kg 0,5 mg/kg nicht überschreiten.
7.3. Wiederfindungsrate
Für eine angereicherte Blindprobe muss die Wiederfindung mindestens 80 % betragen.
8. Ergebnisse eines Ringversuchs
Es wurde ein Ringversuch 8 durchgeführt, bei dem 3 Proben von 8 Laboratorien untersucht wurden. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst:
Ergebnisse
| Probe A (Blindprobe) nach Erhalt | Probe B (Mehl) | Probe C (Pellets) | |||||||||||
| Nach Erhalt | Nach 2 Monaten | Nach Erhalt | Nach 2 Monaten | ||||||||||
| Mittelwert [mg/kg] | NN | 2,80 | 2,42 | 2,89 | 2,45 | ||||||||
| SR [mg/kg] | - | 0,45 | 0,43 | 0,40 | 0,42 | ||||||||
| VKR [%] | - | 16 | 18 | 14 | 17 | ||||||||
| Wiederfindung [%] | 86 | 74 | 88 | 75 | |||||||||
| |||||||||||||
E. Bestimmung des Robenidingehalts
1,3-bis[(4-Chlorobenzyliden)amino]-guanidin-hydrochlorid
Der Robenidingehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Robenidingehalts von Futtermitteln. Die Bestimmungsgrenze beträgt 5 mg/kg.
2. Prinzip
Die Probe wird mit angesäuertem Methanol extrahiert. Der Extrakt wird getrocknet und ein aliquoter Teil zum Clean-up auf eine Aluminiumoxidsäule gegeben. Robenidin wird mit Methanol von der Säule eluiert, eingeengt und mit der mobilen Phase auf ein geeignetes Volumen gebracht. Der Robenidingehalt wird mittels Umkehrphasen-Hochleistungsflüssigkeitschromatografie (HPLC) unter Verwendung eines UV-Detektors bestimmt.
3. Reagenzien
3.1. Methanol
3.2. Angesäuertes Methanol
In einen 500-ml-Messkolben werden 4,0 ml Salzsäure (?20 = 1,18 g/ml) überführt. Es wird mit Methanol (Nummer 3.1) zur Marke aufgefüllt und durchmischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.3. Acetonitril, HPLC-Qualität.
3.4. Molekularsieb
Typ 3A, 8 bis 12 Mesh (Korngröße 1,6 bis 2,5 mm, kristallines Aluminiumsilicat, Porendurchmesser 0,3 mm).
3.5. Aluminiumoxid, sauer, Aktivitätsstufe I, für die Säulenchromatografie
100 g Aluminiumoxid werden in ein geeignetes Gefäß gegeben und mit 2,0 ml Wasser versetzt. Das Gefäß wird verschlossen und etwa 20 min geschüttelt. Das Aluminiumoxid ist in einem gut verschlossenen Behälter aufzubewahren.
3.6. Kaliumdihydrogenphosphatlösung, c = 0,025 mol/l
In einem 1.000-ml-Messkolben werden 3,40 g Kaliumdihydrogenphosphat in Wasser (HPLC-Qualität) gelöst. Es wird zur Marke aufgefüllt und durchmischt.
3.7. Dinatriumhydrogenphosphatlösung, c = 0,025 mol/l
In einem 1 l-Messkolben werden 3,55 g wasserfreies Dinatriumhydrogenphosphat (oder 4,45 g Dihydrat oder 8,95 g Dodecahydrat) in Wasser (HPLC-Qualität) gelöst. Es wird zur Marke aufgefüllt und durchmischt.
3.8. Mobile Phase für die HPLC
Folgende Reagenzien werden gemischt:
650 ml Acetonitril (Nummer 3.3),
250 ml Wasser (HPLC-Qualität),
50 ml Kaliumdihydrogenphosphatlösung (Nummer 3.6),
50 ml Dinatriumhydrogenphosphatlösung (Nummer 3.7).
Die Lösung wird durch einen 0,22-μm-Filter (Nummer 4.6) filtriert und entgast (z.B. durch 10-minütige Ultraschallbehandlung).
3.9. Standardsubstanz
Robenidin, 1,3-bis[(4-Chlorbenzyliden)amino]-guanidin-hydrochlorid, rein
3.9.1. Robenidin-Standard-Stammlösung, 300 μg/ml
Von der Robenidin-Standardsubstanz (Nummer 3.9) werden 30 mg auf 0,1 mg genau eingewogen, in einem 100-ml-Messkolben in angesäuertem Methanol (Nummer 3.2) gelöst und mit demselben Lösungsmittel zur Marke aufgefüllt und durchmischt. Der Messkolben wird mit Aluminiumfolie umhüllt und im Dunkeln aufbewahrt.
3.9.2. Robenidin-Standardlösung, 12 μg/ml
Von der Standard-Stammlösung (Nummer 3.9.1) werden 10,0 ml in einen 250-ml-Messkolben überführt. Es wird mit der mobilen Phase (Nummer 3.8) zur Marke aufgefüllt und durchmischt. Der Messkolben wird mit Aluminiumfolie umhüllt und im Dunkeln aufbewahrt.
3.9.3. Kalibrierlösungen
Von der Robenidin-Standardlösung (Nummer 3.9.2) werden 5,0, 10,0, 15,0, 20,0 bzw. 25,0 ml jeweils in einen 50-ml-Messkolben überführt. Es wird mit der mobilen Phase (Nummer 3.8) zur Marke aufgefüllt und durchmischt. Diese Lösungen enthalten Robenidin in Konzentrationen von 1,2, 2,4, 3,6, 4,8 bzw. 6,0 μg/ml. Die Lösungen müssen vor Gebrauch frisch hergestellt werden.
3.10. Wasser, HPLC-Qualität
4. Geräte
4.1. Glassäule
Braunglas mit Absperrhahn und Reservoir mit einem Fassungsvermögen von ca. 150 ml, InnendurchmesS.r.1. bis 15 mm, Länge 250 mm.
4.2. Mechanischer Schüttler oder Magnetrührer.
4.3. Rotationsfilmverdampfer.
4.4. HPLC-Einrichtung mit UV-Detektor mit variabler Wellenlängeneinstellung oder Diodenarray-Detektor mit einem Messbereich von 250 bis 400 nm
4.4.1. HPLC-Trennsäule: 300 mm × 4 mm, C18, 10 μm Korngröße, oder vergleichbare Säule.
4.5. Glasfaser-Filterpapier, z.B. Whatman GF/A oder gleichwertig.
4.6. Membranfilter, 0,22 μm Porengröße.
4.7. Membranfilter, 0,45 μm Porengröße.
5. Verfahren
| Anmerkung: | Robenidin ist lichtempfindlich. Bei allen Verfahrensschritten sind Braunglasgeräte zu verwenden. |
5.1. Allgemeines
5.1.1. Zur Prüfung, dass weder Robenidin noch Störsubstanzen vorhanden sind, ist eine Blindprobe zu untersuchen.
5.1.2. Die Wiederfindungsrate wird ermittelt, indem eine Blindprobe (Nummer 5.1.1) untersucht wird, die mit Robenidin angereichert wurde. Die zugesetzte Menge an Robenidin sollte der in der Probe vorhandenen Menge entsprechen. Zur Anreicherung auf einen Gehalt von 60 mg/kg werden 3,0 ml der Standard-Stammlösung (Nummer 3.9.1) in einen 250-ml-Erlenmeyerkolben gegeben. Die Lösung wird in einem Stickstoffstrom auf ca. 0,5 ml eingeengt. Dann werden 15 g der Blindprobe zugegeben. Es wird gemischt und 10 min stehen gelassen, bevor mit der Extraktion (Nummer 5.2) fortgefahren wird.
| Anmerkung: | Für den Zweck dieser Methode muss die Blindprobe ähnlich zusammengesetzt sein wie die zu untersuchende Probe, und Robenidin darf nicht nachweisbar sein. |
5.2. Extraktion
Von der vorbereiteten Probe werden 15 g auf 0,01 g genau in einen 250-ml-Erlenmeyerkolben eingewogen, mit 100,0 ml angesäuertem Methanol (Nummer 3.2) versetzt und nach Verschließen des Kolbens 1 h auf dem Schüttler (Nummer 4.2) geschüttelt. Die Lösung wird über Glasfaserfilterpapier (Nummer 4.5) filtriert und das gesamte Filtrat in einem 150-ml-Erlenmeyerkolben aufgefangen. Es werden 7,5 g Molekularsieb (Nummer 3.4) zugegeben, und nach Verschließen des Kolbens wird 5 min geschüttelt. Anschließend wird sofort durch ein Glasfaserfilterpapier filtriert. Diese Lösung wird für die Reinigung (Nummer 5.3) aufbewahrt.
5.3. Reinigung
5.3.1. Vorbereitung der Aluminiumoxid-Säule
In das untere Ende der Glassäule (Nummer 4.1) wird ein Glaswattebausch eingebracht, der mit einem Glasstab zusammengedrückt wird. Von dem vorbereiteten Aluminiumoxid (Nummer 3.5) werden 11,0 g auf die Säule aufgebracht. Dabei ist darauf zu achten, dass der Kontakt mit der Luft so gering wie möglich gehalten wird. Durch leichtes Klopfen an das untere Ende der befüllten Säule wird das Aluminiumoxid verdichtet.
5.3.2. Reinigung der Probe
Von dem Probenextrakt (Nummer 5.2) werden 5,0 ml mit einer Pipette auf die Säule gegeben, wobei die Pipettenspitze die Säulenwand berühren soll. Nach Absorption der Lösung durch das Aluminiumoxid wird das Robenidin mit 100 ml Methanol (Nummer 3.1) bei einer Flussrate von 2-3 ml/min von der Säule eluiert und das Eluat in einem 250-ml-Rundkolben aufgefangen. Die Methanollösung wird am Rotationsverdampfer (Nummer 4.3) bei 40 °C und unter vermindertem Druck bis zur Trockne eingeengt. Der Rückstand wird mit 3 bis 4 ml der mobilen Phase (Nummer 3.8) erneut gelöst und quantitativ in einen 10-ml-Messkolben überführt. Der Kolben wird mehrmals mit je 1 bis 2 ml der mobilen Phase gespült, und die Spüllösungen werden in den Messkolben gegeben. Es wird mit der mobilen Phase zur Marke aufgefüllt und gemischt. Ein aliquoter Teil wird durch einen 0,45-μm-Membranfilter (Nummer 4.7) filtriert. Diese Lösung wird für die HPLC-Bestimmung (Nummer 5.4) aufbewahrt.
5.4. HPLC-Bestimmung
5.4.1. Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren
| HPLC-Trennsäule (Nummer 4.4.1), |
| mobile Phase für die HPLC (Nummer 3.8), |
| Durchflussrate: 1,5 bis 2 ml/min, |
| Detektionswellenlänge: 317 nm |
| Einspritzvolumen: 20 bis 50 μl. |
Die Stabilität des chromatografischen Systems wird überprüft, indem die Kalibrierlösung (Nummer 3.9.3), die 3,6 μg/ml enthält, mehrmals eingespritzt wird, bis konstante Peakhöhen (-flächen) und Retentionszeiten erreicht sind.
5.4.2. Erstellung der Kalibrationskurve
Jede Kalibrierlösung (Nummer 3.9.3) wird mehrmals eingespritzt, und die Peakhöhen (-flächen) für die einzelnen Konzentrationen werden gemessen. Es wird eine Kalibrationskurve erstellt, indem die mittleren Peakhöhen (-flächen) der Kalibrierlösungen auf der Ordinate und die dazugehörigen Konzentrationen in μg/ml auf der Abszisse aufgetragen werden.
5.4.3. Bestimmung der Probenlösung
Der Probenextrakt (Nummer 5.3.2) wird mehrmals eingespritzt, wobei dasselbe Volumen wie für die Einspritzung der Kalibrierlösungen verwendet wird, und die mittlere Peakhöhe (-fläche) der Robenidinpeaks wird ermittelt.
6. Berechnung der Ergebnisse
Aus der mittleren Höhe (Fläche) der Robenidinpeaks der Probenlösung wird anhand der Kalibrationskurve (Nummer 5.4.2) die Konzentration der Probenlösung in μg/ml bestimmt.
Der Robenidingehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
w = (c × 200) / m
wobei:
| c = | Robenidinkonzentration der Probenlösung in μg/ml, |
| m = | Probeneinwaage in g. |
7. Überprüfung der Ergebnisse
7.1. Identität
Die Identität des Analyten kann durch Co-Chromatografie oder mithilfe eines Diodenarray-Detektors bestätigt werden, wobei die Spektren der Probenlösung und der Kalibrierlösung (Nummer 3.9.3), die 6 μg/ml enthält, verglichen werden.
7.1.1. Co-Chromatografie
Eine Probenlösung wird mit einer geeigneten Menge Kalibrierlösung (Nummer 3.9.3) versetzt. Die Menge des zugesetzten Robenidins muss dem erwarteten Robenidingehalt der Probenlösung entsprechen.
Unter Berücksichtigung der zugesetzten Menge und der Verdünnung des Extrakts darf nur die Höhe des Robenidinpeaks vergrößert sein. Die Peakbreite in halber Höhe darf höchstens ± 10 % von der des Peaks der nicht angereicherten Probenlösung abweichen.
7.1.2. Diodenarray-Detektion
Die Ergebnisse werden gemäß den nachstehenden Kriterien beurteilt:
Wird eines dieser Kriterien nicht erfüllt, gilt das Vorhandensein des Analyten als nicht bestätigt.
7.2. Wiederholbarkeit
Bei einem Robenidingehalt von mehr als 15 mg/kg darf die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe 10 % des höheren Werts nicht überschreiten.
7.3. Wiederfindungsrate
Für eine angereicherte Blindprobe muss die Wiederfindungsrate mindestens 85 % betragen.
8. Ergebnisse eines Ringversuchs
Bei einem EU-Ringversuch wurden 4 Proben von Geflügel- und Kaninchenfutter in Form von Mehl oder Pellets von 12 Laboratorien analysiert. Jede Probe wurde doppelt analysiert. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst.
| Geflügelfutter | Kaninchenfutter | |||||||||||
| Mehl | Pellets | Mehl | Pellets | |||||||||
| Mittelwert [mg/kg] | 27,00 | 27,99 | 43,6 | 40,1 | ||||||||
| sr [mg/kg] | 1,46 | 1,26 | 1,44 | 1,66 | ||||||||
| VKr [%] | 5,4 | 4,5 | 3,3 | 4,1 | ||||||||
| SR [mg/kg] | 4,36 | 3,36 | 4,61 | 3,91 | ||||||||
| VKR [%] | 16,1 | 12,0 | 10,6 | 9,7 | ||||||||
| Wiederfindung [%] | 90,0 | 93,3 | 87,2 | 80,2 | ||||||||
| ||||||||||||
F. Bestimmung des Diclazurilgehalts
(±)-4-Chlorphenyl[2,6 dichlor-4-(2,3,4,5-tetrahydro-3,5-dioxo-1,2,4-triazin-2-yl)phenyl]acetonitrile.
Der Diclazurilgehalt ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Diclazurilgehalts von Futtermitteln und Vormischungen. 9 Die Nachweisgrenze beträgt 0,1 mg/kg, die Bestimmungsgrenze 0,5 mg/kg. Niedrigere Bestimmungsgrenzen können zwar erreicht werden, aber dies ist vom Nutzer zu validieren.
2. Prinzip
Nach Hinzufügen eines internen Standards wird die Probe mit angesäuertem Methanol extrahiert. Bei Futtermitteln wird ein aliquoter Teil des Extrakts mit einer C18-Festphasen-Extraktionskartusche gereinigt. Diclazuril wird aus der Kartusche mit einem Gemisch aus angesäuertem Methanol und Wasser eluiert. Nach dem Einengen wird der Rückstand in DMF/Wasser gelöst. Bei Vormischungen wird der Extrakt eingeengt und der Rückstand in DMF/Wasser gelöst. Der Diclazurilgehalt wird mittels ternärer Gradienten-Hochleistungsflüssigkeitschromatografie (HPLC) über eine Umkehrphase unter Verwendung eines UV-Detektors bestimmt.
3. Reagenzien
3.1. Wasser, HPLC-Qualität.
3.2. Ammoniumacetat.
3.3. Tetrabutylammoniumhydrogensulfat (TBHS).
3.4. Acetonitril, HPLC-Qualität.
3.5. Methanol, HPLC-Qualität.
3.6. N,N-Dimethylformamid (DMF).
3.7. Salzsäure, ρ20 = 1,19 g/ml.
3.8. Standardsubstanz: Diclazuril: 2,6-Dichlor-alpha-(4-chlorophenyl)-4-(4,5-dihydro-3,5-dioxo-1,2,4-triazin-2-(3H)-yl)benzacetonitril, rein.
3.8.1. Diclazuril-Standard-Stammlösung, 500 μg/ml
Von der Diclazuril-Standardsubstanz (Nummer 3.8) werden 25 mg auf 0,1 mg genau in einen 50-ml-Messkolben eingewogen und in DMF (Nummer 3.6) gelöst; es wird mit DMF (Nummer 3.6) zur Marke aufgefüllt und gemischt. Der Messkolben wird mit Aluminiumfolie umhüllt (oder ein Messkolben aus braunem Glas verwendet) und im Kühlschrank aufbewahrt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar. 10
3.8.2. Diclazuril-Standardlösung, 50 μg/ml
Von der Standard-Stammlösung (Nummer 3.8.1) werden 5,00 ml in einen 50-ml-Messkolben überführt; es wird mit DMF (Nummer 3.6) zur Marke aufgefüllt und gemischt. Der Messkolben wird mit Aluminiumfolie umhüllt (oder ein Messkolben aus braunem Glas verwendet) und im Kühlschrank aufbewahrt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.9. Interne Standardsubstanz: 2,6 Dichloro-α-(4-chlorophenyl)-4-(4,5-dihydro-3,5-dioxo-1,2,4-triazin-2-(3H)-yl)-α-methylbenzacetonitril (Methyldiclazuril)
3.9.1. Interne Standardlösung, 500 μg/ml
Von der internen Standardsubstanz (Nummer 3.9) werden 25 mg auf 0,1 mg genau in einen 50-ml-Messkolben eingewogen und in DMF (Nummer 3.6) gelöst; es wird mit DMF (Nummer 3.6) zur Marke aufgefüllt und gemischt. Der Messkolben wird mit Aluminiumfolie umhüllt (oder ein Messkolben aus braunem Glas verwendet) und im Kühlschrank aufbewahrt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.9.2. Interne Standardlösung, 50 μg/ml
Von der internen Standardlösung (Nummer 3.9.1) werden 5,00 ml in einen 50-ml-Messkolben überführt; es wird mit DMF (Nummer 3.6) zur Marke aufgefüllt und gemischt. Der Messkolben wird mit Aluminiumfolie umhüllt (oder ein Messkolben aus braunem Glas verwendet) und im Kühlschrank aufbewahrt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.9.3. Interne Standardlösung für Vormischungen, p/1.000 mg/ml (p = Diclazuril-Sollgehalt in der Vormischung in mg/kg)
Von der internen Standardsubstanz werden p/10 mg auf 0,1 mg genau in einen 100-ml-Messkolben eingewogen und mittels Ultraschallbad (Nummer 4.7) in DMF (Nummer 3.6) gelöst; es wird mit DMF (Nummer 3.6) zur Marke aufgefüllt und gemischt. Der Messkolben wird mit Aluminiumfolie umhüllt (oder ein Messkolben aus braunem Glas verwendet) und im Kühlschrank aufbewahrt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.10. Kalibrierlösungen
3.10.1. Kalibrierlösung, 1 μg/ml
In einen 50-ml-Messkolben werden 1,00 ml Diclazuril-Standardlösung (Nummer 3.8.2) und 2,00 ml interne Standardlösung (Nummer 3.9.2) pipettiert. Es werden 17 ml DMF (Nummer 3.6) hinzugefügt; anschließend wird mit Wasser (Nummer 3.1) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.2. Kalibrierlösung, 2 μg/ml
In einen 50-ml-Messkolben werden 2,00 ml Diclazuril-Standardlösung (Nummer 3.8.2) und 2,00 ml interne Standardlösung (Nummer 3.9.2) pipettiert. Es werden 16 ml DMF (Nummer 3.6) hinzugefügt; anschließend wird mit Wasser (Nummer 3.1) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.3. Kalibrierlösung, 3 μg/ml (Diclazuril)
In einen 50-ml-Messkolben werden 3,00 ml Diclazuril-Standardlösung (Nummer 3.8.2) und 2,00 ml interne Standardlösung (Nummer 3.9.2) pipettiert. Es werden 15 ml DMF (Nummer 3.6) hinzugefügt; anschließend wird mit Wasser (Nummer 3.1) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.4. Kalibrierlösung, 4 μg/ml (Diclazuril)
In einen 50-ml-Messkolben werden 4,00 ml Diclazuril-Standardlösung (Nummer 3.8.2) und 2,00 ml interne Standardlösung (Nummer 3.9.2) pipettiert. Es werden 14 ml DMF (Nummer 3.6) hinzugefügt; anschließend wird mit Wasser (Nummer 3.1) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.5. Kalibrierlösung, 5 μg/ml (Diclazuril)
In einen 50-ml-Messkolben werden 5,00 ml Diclazuril-Standardlösung (Nummer 3.8.2) und 2,00 ml interne Standardlösung (Nummer 3.9.2) pipettiert. Es werden 13 ml DMF (Nummer 3.6) hinzugefügt; anschließend wird mit Wasser (Nummer 3.1) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
| Anmerkung: | Die Kalibrierlösungen (Nummer 3.10.1, 3.10.2, 3.10.3, 3.10.4 und 3.10.5) decken Diclazurilkonzentrationen von 0,5 mg/kg bis 2,5 mg/kg in Futtermitteln ab, sofern das aktuelle Protokoll verwendet wird. |
3.11. C18-Festphasen-Extraktionskartusche, z.B. Mega Bond Elut, Größe: 20 cc, Sorptionsmenge: 5.000 mg (Vorkonditionierung gemäß Lieferantenleitlinien).
3.12. Extraktionslösung: angesäuertes Methanol
5,0 ml Salzsäure (Nummer 3.7) werden in 1.000 ml Methanol (Nummer 3.5) pipettiert und gemischt.
3.13. Mobile Phase für die HPLC:
3.13.1. Elutionsmittel A: Ammoniumacetat-Tetrabutylammoniumhydrogensulfat-Lösung,
5 g Ammoniumacetat (Nummer 3.2) und 3,4 g TBHS (Nummer 3.3) werden in 1.000 ml Wasser (Nummer 3.1) gelöst und gemischt.
3.13.2. Elutionsmittel B: Acetonitril (Nummer 3.4).
3.13.3. Elutionsmittel C: Methanol (Nummer 3.5).
4. Geräte
4.1. Mechanischer Schüttler.
4.2. HPLC-Einrichtung für ternären Gradienten
4.2.1. HPLC-Trennsäule, 3 μm Korngröße, 100 mm × 4,6 mm, z.B. Hypersil ODS, oder vergleichbare Säule.
4.2.2. UV-Detektor mit variabler Wellenlängeneinstellung oder Diodenarray-Detektor.
4.3. Rotationsfilmverdampfer.
4.4. Membranfilter (z.B. aus chemisch resistentem Nylon), 0,45 μm
4.5. Einwegspritze, 5 ml
4.6. Vakuumeinrichtung.
4.7. Ultraschallbad.
5. Verfahren
5.1. Allgemeines
5.1.1. Blindprobe
Zur Prüfung, dass weder Diclazuril noch Störsubstanzen vorhanden sind, ist eine Blindprobe zu untersuchen. Die Blindprobe muss ähnlich zusammengesetzt sein wie die zu untersuchende Probe, und Diclazuril oder Störsubstanzen dürfen nicht nachweisbar sein.
5.1.2. Wiederfindungstest
Die Wiederfindungsrate wird ermittelt, indem eine Blindprobe untersucht wird, die mit Diclazuril angereichert wurde. Die zugesetzte Menge sollte der in der Probe vorhandenen Menge entsprechen. Zur Anreicherung auf einen Gehalt von 1 mg/kg werden 0,1 ml der Standard-Stammlösung (Nummer 3.8.1) zu 50 g der Blindprobe gegeben. Es wird gründlich gemischt, 10 min stehen gelassen und nochmals mehrfach gemischt, bevor mit der Extraktion (Nummer 5.2) fortgefahren wird.
Ist eine der zu untersuchenden Probe ähnliche Blindprobe nicht verfügbar (siehe 5.1.1), so kann ein Wiederfindungstest mithilfe des Standard-Additionsverfahrens durchgeführt werden. In diesem Fall wird die zu untersuchende Probe mit einer Diclazurilmenge angereichert, die der bereits in der Probe vorhandenen Menge entspricht. Diese Probe wird zusammen mit der nicht angereicherten Probe untersucht, und die Wiederfindungsrate kann durch Subtraktion ermittelt werden.
5.2. Extraktion
5.2.1. Mischfuttermittel
Von der Probe werden 50 g auf 0,01 g genau eingewogen und in einen 500-ml-Erlenmeyerkolben überführt. Es werden 1,00 ml der internen Standardlösung (Nummer 3.9.2) und 200 ml Extraktionslösung (Nummer 3.12) hinzugefügt. Anschließend wird der Kolben verschlossen. Die Mischung wird über Nacht auf dem Schüttler (Nummer 4.1) geschüttelt und anschließend 10 min stehen gelassen. Ein aliquoter Teil von 20 ml der überstehenden Lösung wird in einen geeigneten Glasbehälter überführt und mit 20 ml Wasser (Nummer 3.1) verdünnt. Diese Lösung wird auf eine Extraktionskartusche (Nummer 3.11) gegeben und mittels Vakuum (Nummer 4.6) hindurch gesaugt. Die Kartusche wird mit 25 ml einer Mischung aus Extraktionslösung (Nummer 3.12) und Wasser (Nummer 3.1), 65 + 35 (V+V), ausgewaschen. Die gesammelten Fraktionen werden verworfen, und der Wirkstoff und der interne Standard werden mit 25 ml einer Mischung aus Extraktionslösung (Nummer 3.12) und Wasser, 80 + 20 (V+V), eluiert. Diese Fraktion wird mithilfe eines Rotationsverdampfers (Nummer 4.3) bei 60 °C zur Trockne eingeengt. Der Rückstand wird in 1,0 ml DMF (Nummer 3.6) gelöst; es werden 1,5 ml Wasser (Nummer 3.1) hinzugefügt, gemischt, durch einen Membranfilter (Nummer 4.4) filtriert und auf eine Einwegspritze (Nummer 4.5) gezogen. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.2.2. Vormischungen
Von der Probe wird 1 g auf 0,001 g genau eingewogen und in einen 500-ml-Erlenmeyerkolben überführt. Es werden 1,00 ml interne Standardlösung (Nummer 3.9.3) und 200 ml Extraktionslösung (Nummer 3.12) hinzugefügt, und der Kolben wird verschlossen. Die Mischung wird über Nacht auf dem Schüttler (Nummer 4.1) geschüttelt und anschließend 10 min stehen gelassen. Ein 10.000/p-ml-Aliquot (p = Diclazuril-Sollgehalt in der Vormischung in mg/kg) der überstehenden Lösung wird in einen Rundkolben geeigneter Größe überführt. Es wird mithilfe eines Rotationsverdampfers (Nummer 4.3) bei vermindertem Druck und 60 °C zur Trockne eingeengt. Der Rückstand wird in 10,0 ml DMF (Nummer 3.6) gelöst; es werden 15,0 ml Wasser (Nummer 3.1) hinzugefügt und gemischt. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.3. HPLC-Bestimmung
5.3.1. Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren oder besseren Ergebnissen führen.
Die Stabilität des chromatografischen Systems wird überprüft, indem die Kalibrierlösung (Nummer 3.10.2), die 2 μg/ml Diclazuril und interner Standard enthält, mehrmals eingespritzt wird, bis konstante Peakhöhen (-flächen) und Retentionszeiten erreicht sind.
5.3.2. Chromatografische Analyse der Kalibrierlösungen
Es werden zweimal je 20 μl der Kalibrierlösungen (Nummer 3.10.1, 3.10.2, 3.10.3, 3.10.4 und 3.10.5) eingespritzt, für Diclazuril und den internem Standard werden die Peakhöhen ermittelt und integriert, dann wird die Kalibrierkurve anhand des Verhältnisses der mittleren Peakhöhe oder -fläche von Diclazuril zur mittleren Peakhöhe oder -fläche des internen Standards gegenüber der Diclazurilkonzentration in den Kalibrierlösungen (μg/ml) aufgezeichnet.
5.3.3. Chromatografische Analyse der Probenlösungen
Von der Probenlösung (Nummer 5.2.1 oder 5.2.2) werden zweimal 20 μl eingespritzt, und für Diclazuril und den internen Standard wird die mittlere Peakhöhe (-fläche) bestimmt.
6. Berechnung der Ergebnisse
6.1. Mischfuttermittel
Der Diclazurilgehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
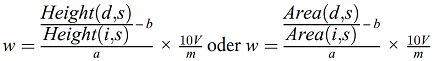
wobei:
6.2. Vormischungen
Der Diclazurilgehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
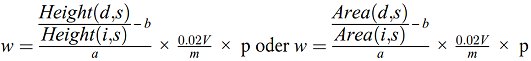
wobei:
7. Überprüfung der Ergebnisse
7.1. Identität
Die Identität des Analyten kann durch Co-Chromatografie oder mithilfe eines Diodenarray-Detektors bestätigt werden, wobei die Spektren der Probenlösung (Nummer 5.2.1 oder 5.2.2) und der Kalibrierlösung (Nummer 3.10.2) verglichen werden.
7.1.1. Co-Chromatografie
Eine nach Nummer 5.2.1 oder 5.2.2 hergestellte Probenlösung wird mit einer geeigneten Menge Kalibrierlösung (Nummer 3.10.2) angereichert. Die Menge des zugesetzten Diclazurils muss dem erwarteten Diclazurilgehalt der Probenlösung entsprechen.
Unter Berücksichtigung der zugesetzten Menge und der Verdünnung des Extrakts darf nur die Höhe des Diclazurilpeaks und des Peaks des internen Standards vergrößert sein. Die Peakbreite in halber Höhe darf höchstens ± 10 % von der des ursprünglichen Diclazurilpeaks oder Standardpeaks des nicht angereicherten Probenextrakts abweichen.
7.1.2. Diodenarray-Detektion
Die Ergebnisse werden gemäß den nachstehenden Kriterien beurteilt:
Wird eines dieser Kriterien nicht erfüllt, gilt das Vorhandensein des Analyten als nicht bestätigt.
7.2. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier unabhängiger Messungen an zwei Teilproben darf die folgenden Werte nicht überschreiten:
7.3. Wiederfindungsrate
Bei einer angereicherten (Blind-)Probe muss die Wiederfindungsrate mindestens 80 % betragen.
8. Ergebnisse eines Ringversuchs
Es wurden zwei Ringversuche durchgeführt. Im ersten, 1994 von einer anderen Gruppe von Laboratorien durchgeführten Ringversuch handelte es sich bei den untersuchten Proben um zwei Vormischungen (O 100, A 100) und drei Proben von Ergänzungsfuttermitteln für Geflügel (L1, Z1, K1). Eine der Proben aus Vormischungen war mit einer organischen Matrix (O 100) und die andere mit einer anorganischen Matrix (A 100) gemischt. Der theoretische Diclazurilgehalt liegt bei 100 mg/kg. Die Laboratorien wurden beauftragt, jede der Proben 1- oder 2-mal zu untersuchen. (Nähere Informationen zu diesem ersten Ringversuch sind dem Journal of AOAC International, Band 77, Nr. 6, 1994, S. 1359-1361, zu entnehmen).
Im zweiten Ringversuch wurden drei Mischfuttermittel für Geflügel, eines mit Diclazuril in einer Konzentration von 0,9 mg/kg (MAT 1), eines mit 1,5 mg/kg (MAT 2) und eine Blindprobe (MAT 3), analysiert. (Nähere Informationen zu diesem zweiten Ringversuch sind dem Technischen Bericht der JRC (2016) und dem Journal of AOAC International, Band 102, Nr. 2, 2019, S. 646-652, zu entnehmen.) Die Ergebnisse der beiden Ringstudien sind der nachstehenden Tabelle zu entnehmen:
| Probe 1A 100 | Probe 2O 100 | Probe 3 L1 | Probe 4 Z1 | Probe 5 K1 | Probe 6 MAT 1 | Probe 7 MAT 2 | Probe 8 MAT 3 | |||||||||||||||||
| L | 11 | 11 | 11 | 11 | 6 | 10 | 9 | 10 | ||||||||||||||||
| n | 19 | 18 | 19 | 19 | 12 | 20 | 18 | 10 | ||||||||||||||||
| Mittelwert (mg/kg) | 100,8 | 103,5 | 0,89 | 1,15 | 0,89 | 1,0 | 1,5 | < LOQ | ||||||||||||||||
| Sr (mg/kg) | 5,88 | 7,64 | 0,15 | 0,02 | 0,03 | 0,11 | 0,07 | - | ||||||||||||||||
| VKr (%) | 5,83 | 7,38 | 17,32 | 1,92 | 3,34 | 11,2 | 4,5 | - | ||||||||||||||||
| SR (mg/kg) | 7,59 | 7,64 | 0,17 | 0,11 | 0,12 | 0,18 | 0,21 | - | ||||||||||||||||
| VKR (%) | 7,53 | 7,38 | 18,61 | 9,67 | 13,65 | 18,1 | 14,3 | - | ||||||||||||||||
| Sollgehalt (mg/kg) | 100 | 100 | 1,0 | 1,0 | 1,0 | 0,9 | 1,5 | - | ||||||||||||||||
| Referenz * | Erste Studie aus dem Jahr 1.994 | Erste Studie aus dem Jahr 1.994 | Erste Studie aus dem Jahr 1.994 | Erste Studie aus dem Jahr 1.994 | Erste Studie aus dem Jahr 1.994 | Zweite Studie aus dem Jahr 2.015 | Zweite Studie aus dem Jahr 2.015 | Zweite Studie aus dem Jahr 2.015 | ||||||||||||||||
| ||||||||||||||||||||||||
9. Allgemeine Anmerkungen
Es muss vorab erwiesen sein, dass das Diclazurilsignal im linearen Konzentrationsbereich liegt.
Zumindest bei der Analyse von Diclazuril in Mischfuttermitteln mit hohem Fettgehalt (zu diesem Zweck mehr als 12 % Fett) kann die Analysemethode durch andere HPLC-basierte Methoden ersetzt werden, etwa durch eine Methode auf der Basis von Hochleistungsflüssigchromatografie mit Massenspektrometrie (HPLC-MS), sofern die alternative Methode gleichwertige Leistungsmerkmale (Wiederfindungsrate, Präzision unter Wiederholbarkeits- und Vergleichbarkeitsbedingungen) aufweist.
G. Bestimmung des Gehalts an Lasalocid-Natrium
Monocarboxylsäure-Polyether-Natriumsalz, gebildet durch Streptomyces lasaliensis
Der Gehalt an Lasalocid-Natrium ist mit folgenden Verfahren zu bestimmen:
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Gehalts an Lasalocid-Natrium in Futtermitteln und Vormischungen. Die Nachweisgrenze beträgt 5 mg/kg, die Bestimmungsgrenze 10 mg/kg.
2. Prinzip
Lasalocid-Natrium wird aus der Probe mit angesäuertem Methanol extrahiert und mittels Umkehrphasen-Hochleistungsflüssigchromatografie (RP-HPLC) unter Verwendung eines spektrofluorometrischen (Fluoreszenz-)Detektors bestimmt.
3. Reagenzien
3.1. Kaliumdihydrogenphosphat (KH2PO4)
3.2. Orthophosphorsäure, w (Massenanteil) = 85 %
3.3. Orthophosphorsäurelösung, c = 20 %
23,5 ml Orthophosphorsäure (Nummer 3.2) werden mit Wasser auf 100 ml aufgefüllt.
3.4. 6-Methyl-2-Heptylamin (1,5-Dimethylhexylamin), w (Massenanteil) = 99 %.
3.5. Methanol, HPLC-Qualität.
3.6. Salzsäure, Dichte = 1,19 g/ml.
3.7. Phosphatpufferlösung, c = 0,01 mol/l
In 500 ml Wasser (Nummer 3.11) werden 1,36 g KH2PO4 (Nummer 3.1) gelöst, und es werden 3,5 ml Orthophosphorsäure (Nummer 3.2) sowie 10,0 ml 6-Methyl-2-Heptylamin (Nummer 3.4) hinzugefügt. Den pH-Wert mit Orthophosphorsäurelösung (Nummer 3.3) auf pH 4,0 einstellen und mit Wasser (Nummer 3.11) auf 1.000 ml auffüllen.
3.8. Angesäuertes Methanol
In einen 1.000-ml-Messkolben werden 5,0 ml Salzsäure (Nummer 3.6) gegeben, und es wird mit Methanol (Nummer 3.5) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.9. Mobile Phase für die HPLC: Phosphatpuffer-Methanollösung 5 + 95 (V+V)
Von der Phosphatpufferlösung (Nummer 3.7) werden 5 ml mit 95 ml Methanol (Nummer 3.5) vermischt.
3.10. Lasalocid-Natrium-Standardsubstanz, garantiert rein, C34H53O8Na (Monocarboxylsäure-Polyether-Natriumsalz, gebildet durch Streptomyces lasaliensis), E 763
3.10.1. Lasalocid-Natrium-Standard-Stammlösung, 500 μg/ml
Von Lasalocid-Natrium (Nummer 3.10) werden 50 mg auf 0,1 mg genau in einen 100-ml-Messkolben eingewogen und in angesäuertem Methanol (Nummer 3.8) gelöst. Es wird mit demselben Lösungsmittel zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.2. Lasalocid-Natrium-Standardlösung, 50 μg/ml
Von der Standard-Stammlösung (Nummer 3.10.1) werden 10,0 ml in einen 100-ml-Messkolben pipettiert; es wird mit angesäuertem Methanol (Nummer 3.8) zur Marke aufgefüllt und gemischt. Diese Lösung muss vor Gebrauch frisch hergestellt werden.
3.10.3. Kalibrierlösungen
Von der Lasalocid-Natrium-Standardlösung (Nummer 3.10.2) werden 1,0, 2,0, 4,0, 5,0 bzw. 10,0 ml in jeweils einen 50-ml-Messkolben überführt. Es wird mit angesäuertem Methanol (Nummer 3.8) zur Marke aufgefüllt und durchmischt. Diese Kalibrierlösungen enthalten jeweils 1,0, 2,0, 4,0, 5,0 bzw. 10,0 μg Lasalocid-Natrium je ml. Die Lösungen müssen vor Gebrauch frisch hergestellt werden.
3.11. Wasser, HPLC-Qualität.
4. Geräte
4.1. Ultraschallbad (oder Schüttel-Wasserbad) mit Temperatursteuerung.
4.2. Membranfilter, 0,45 μm Porengröße.
4.3. HPLC-Einrichtung mit Injektionssystem für Einspritzvolumina von 20 μl
4.3.1. HPLC-Trennsäule, 125 mm × 4 mm, mit Umkehrphase C18, 5 μm Korngröße, oder vergleichbare Säule.
4.3.2. Spektrofluorometer mit variabler Einstellung für Anregungs- und Emissionswellenlängen.
5. Verfahren
5.1. Allgemeines
5.1.1. Blindprobe
Für die Durchführung des Wiederfindungstests (Nummer 5.1.2) ist zur Prüfung, dass weder Lasalocid-Natrium noch Störsubstanzen vorhanden sind, eine Blindprobe zu untersuchen. Die Blindprobe muss ähnlich zusammengesetzt sein wie die zu untersuchende Probe, und Lasalocid-Natrium oder Störsubstanzen dürfen nicht nachweisbar sein.
5.1.2. Wiederfindungstest
Die Wiederfindungsrate wird ermittelt, indem eine Blindprobe untersucht wird, die mit Lasalocid-Natrium angereichert wurde. Die zugesetzte Menge sollte in etwa der in der Probe vorhandenen Menge entsprechen. Zur Anreicherung auf einen Gehalt von 100 mg/kg werden 10,0 ml der Standard-Stammlösung (Nummer 3.10.1) in einen 250-ml-Erlenmeyerkolben überführt. Die Lösung wird auf ca. 0,5 ml eingeengt. Dann werden 50 g der Blindprobe zugegeben. Es wird gründlich gemischt, 10 min stehen gelassen und erneut mehrmals gemischt, bevor mit der Extraktion (Nummer 5.2) fortgefahren wird.
Ist eine der zu untersuchenden Probe ähnliche Blindprobe nicht verfügbar (siehe 5.1.1), so kann ein Wiederfindungstest mithilfe des Standard-Additionsverfahrens durchgeführt werden. In diesem Fall wird die zu untersuchende Probe mit einer Lasalocid-Natrium-Menge angereichert, die in etwa der bereits in der Probe vorhandenen Menge entspricht. Diese Probe wird zusammen mit der nicht angereicherten Probe untersucht und die Wiederfindungsrate kann durch Subtraktion ermittelt werden.
5.2. Extraktion
5.2.1. Futtermittel
Von der Probe werden 5 bis 10 g auf 0,01 g genau in einen 250-ml-Erlenmeyerkolben mit Stopfen eingewogen und 100,0 ml angesäuertes Methanol (Nummer 3.8) mit einer Pipette hinzugefügt. Der Stopfen wird lose aufgesetzt und der Inhalt zum Dispergieren geschwenkt. Der Kolben wird 20 min in ein Ultraschallbad (Nummer 4.1) mit einer Temperatur von ca. 40 °C gestellt, dann entnommen und auf Raumtemperatur abkühlen gelassen. Der Kolben wird etwa 1 h stehen gelassen, bis die Schwebstoffe sich abgesetzt haben. Dann wird ein aliquoter Teil über einen 0,45-μm-Membranfilter (Nummer 4.2) in ein geeignetes Gefäß filtriert. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.2.2. Vormischungen
Rund 2 g der nicht gemahlenen Vormischung werden auf 0,001 g genau in einen 250-ml-Messkolben gegeben. Es werden 100,0 ml angesäuertes Methanol (Nummer 3.8) hinzugefügt; der Inhalt wird zum Dispergieren geschwenkt. Der Kolben wird mit Inhalt 20 min lang in ein Ultraschallbad (Nummer 4.1) mit einer Temperatur von ca. 40 °C gestellt, dann entnommen und auf Raumtemperatur abkühlen gelassen. Es wird mit angesäuertem Methanol (Nummer 3.8) zur Marke aufgefüllt und sorgfältig gemischt. Der Kolben wird etwa 1 h stehen gelassen, bis die Schwebstoffe sich abgesetzt haben. Dann wird ein aliquoter Teil durch einen 0,45-μm-Membranfilter (Nummer 4.2) filtriert. Ein aliquoter Teil des klaren Filtrats wird mit angesäuertem Methanol (Nummer 3.8) verdünnt, um eine Lösung mit einer Konzentration von etwa 4 μg/ml Lasalocid-Natrium zu erhalten. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.3. HPLC-Bestimmung
5.3.1. Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen:
| HPLC-Trennsäule (Nummer 4.3.1): | 125 mm × 4 mm, Umkehrphase C18, 5 μm Korngröße, oder vergleichbare Säule |
| Mobile Phase (Nummer 3.9): | Mischung aus Phosphatpufferlösung (Nummer 3.7) und Methanol (Nummer 3.5), 5 + 95 (V + V). |
| Durchflussrate: | 1,2 ml/min |
| Detektionswellenlänge: | Anregung: 310 nm |
| Emission: 419 nm | |
| Einspritzvolumen: | 20 μl |
Die Stabilität des chromatografischen Systems wird überprüft, indem die Kalibrierlösung (Nummer 3.10.3), die 4,0 μg/ml enthält, mehrmals eingespritzt wird, bis konstante Peakhöhen (-flächen) und Retentionszeiten erreicht sind.
5.3.2. Erstellung der Kalibrationskurve
Jede Kalibrierlösung (Nummer 3.10.3) wird mehrmals eingespritzt, und die mittleren Peakhöhen (-flächen) werden für die einzelnen Konzentrationen gemessen. Es wird eine Kalibrationskurve erstellt, indem die mittleren Peakhöhen (-flächen) auf der Ordinate und die dazugehörigen Konzentrationen in μg/ml auf der Abszisse aufgetragen werden.
5.3.3. Bestimmung der Probenlösung
Die nach Nummer 5.2.1 bzw. 5.2.2 gewonnenen Probenextrakte werden mehrmals eingespritzt, wobei dasselbe Volumen wie für die Einspritzung der Kalibrierlösungen verwendet wird. Die mittlere Peakhöhe (-fläche) der Lasalocid-Natrium-Peaks wird ermittelt.
6. Berechnung der Ergebnisse
Aus der mittleren Peakhöhe (-fläche) der Probenlösung (Nummer 5.3.3) wird anhand der Kalibrationskurve die Konzentration an Lasalocid-Natrium (μg/ml) bestimmt.
6.1. Futtermittel
Der Gehalt an Lasalocid-Natrium w (in mg/kg) der Probe wird nach folgender Formel berechnet:
w = (c × V1) / m [mg/kg]
wobei:
| c = | c = Lasalocid-Natrium-Konzentration der Probenlösung (Nummer 5.2.1) in μg/ml, |
| V1 = | Volumen des Probenextrakts gemäß Nummer 5.2.1 (d. h. 100 ml), |
| m = | Probeneinwaage in g. |
6.2. Vormischungen
Der Gehalt an Lasalocid-Natrium w (in mg/kg) der Probe wird nach folgender Formel berechnet:
w = (c × V2 × f) / m [mg/kg]
wobei:
| c = | c = Lasalocid-Natrium-Konzentration der Probenlösung (Nummer 5.2.2) in μg/ml, |
| V2 = | Volumen des Probenextrakts gemäß Nummer 5.2.2 in ml (d. h. 250 ml), |
| f = | Verdünnungsfaktor gemäß Nummer 5.2.2, |
| m = | Probeneinwaage in g. |
7. Überprüfung der Ergebnisse
7.1. Identität
Nachweis- und Bestimmungsverfahren, denen die Fluoreszenzdetektion zugrunde liegt, sind im Vergleich zur UV-Detektion weniger interferenzanfällig. Die Identität des Analyten kann durch Co-Chromatografie bestätigt werden.
7.1.1. Co-Chromatografie
Ein Probenextrakt (Nummer 5.2.1 oder 5.2.2) wird mit einer entsprechenden Menge Kalibrierlösung (Nummer 3.10.3) angereichert. Die zugesetzte Lasalocid-Natrium-Menge muss in etwa dem Lasalocid-Natrium-Gehalt des Probenextrakts entsprechen. Unter Berücksichtigung der zugesetzten Lasalocid-Natrium-Menge und der Verdünnung des Extrakts darf nur die Höhe des Lasalocid-Natrium-Peaks vergrößert sein. Die Peakbreite in halber Höhe darf höchstens ± 10 % von der ursprünglichen Peakbreite abweichen, die sich bei dem nicht angereicherten Probenextrakt ergibt.
7.2. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf die folgenden Werte nicht überschreiten:
7.3. Wiederfindungsrate
Bei einer angereicherten (Blind-)Probe muss die Wiederfindungsrate bei Futtermitteln mindestens 80 % betragen. Bei angereicherten Vormischungsproben muss die Wiederfindungsrate mindestens 90 % betragen.
8. Ergebnisse eines Ringversuchs
In einem Ringversuch * wurden 2 Vormischungen (Proben 1 und 2) und 5 Futtermittel (Proben 3 bis 7) in 12 Laboratorien untersucht. Jede Probe wurde doppelt analysiert. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst.
| Probe 1 Vormischung Hühnerfutter | Probe 2 Vormischung Truthahnfutter | Probe 3 Truthahnpellets | Probe 4 Hühnerkrümelfutter | Probe 5 Truthahnfutter | Probe 6 Geflügelfutter A | Probe 7 Geflügelfutter B | |||||||||||||||||||
| L | 12 | 12 | 12 | 12 | 12 | 12 | 12 | ||||||||||||||||||
| n | 23 | 23 | 23 | 23 | 23 | 23 | 23 | ||||||||||||||||||
| Mittelwert [mg/kg] | 5.050 | 16.200 | 76,5 | 78,4 | 92,9 | 48,3 | 32,6 | ||||||||||||||||||
| sr [mg/kg] | 107 | 408 | 1,71 | 2,23 | 2,27 | 1,93 | 1,75 | ||||||||||||||||||
| VKr [%] | 2,12 | 2,52 | 2,24 | 2,84 | 2,44 | 4,00 | 5,37 | ||||||||||||||||||
| sR [mg/kg] | 286 | 883 | 3,85 | 7,32 | 5,29 | 3,47 | 3,49 | ||||||||||||||||||
| VKR [%] | 5,66 | 5,45 | 5,03 | 9,34 | 5,69 | 7,18 | 10,70 | ||||||||||||||||||
| Sollgehalt [mg/kg] | 5.000 ** | 16.000 ** | 80 ** | 105 ** | 120 ** | 50 + | 35 + | ||||||||||||||||||
| |||||||||||||||||||||||||
H. Bestimmung des Gehalts an Amprolium-Hydrochlorid
1-[(4-Amino-2-propyl-5-pyrimidinyl)methyl]-2-methyl-pyridiniumchlorid-monohydrochlorid
1. Zweck und Anwendungsbereich
Die Methode erlaubt die Bestimmung des Amproliumgehalts von Futtermitteln. Die Nachweisgrenze beträgt 1 mg/kg, die Bestimmungsgrenze 5 mg/kg.
2. Prinzip
Die Probe wird mit einem Methanol-Wasser-Gemisch extrahiert. Nach Verdünnung mit der mobilen Phase und Membranfiltration wird der Amproliumgehalt mittels Hochleistungsflüssigkeitschromatografie (HPLC) über ein Kationenaustauschermaterial unter Verwendung eines UV-Detektors bestimmt.
3. Reagenzien
3.1. Methanol
3.2. Acetonitril, HPLC-Qualität.
3.3. Wasser, HPLC-Qualität.
3.4. Natriumdihydrogenphosphatlösung, c = 0,1 mol/l
Von dem Natriumdihydrogenphosphatmonohydrat werden 13,80 g in einem 1.000-ml-Messkolben in Wasser (Nummer 3.3) gelöst. Es wird mit Wasser (Nummer 3.3) zur Marke aufgefüllt und gemischt.
3.5. Natriumperchloratlösung, c = 1,6 mol/l
Von dem Natriumperchloratmonohydrat werden 224,74 g in einem 1.000-ml-Messkolben in Wasser (Nummer 3.3) gelöst. Es wird mit Wasser (Nummer 3.3) zur Marke aufgefüllt und gemischt.
3.6. Mobile Phase für die HPLC (siehe Bemerkung 9.1)
Mischung aus Acetonitril (Nummer 3.2), Natriumdihydrogenphosphat-Lösung (Nummer 3.4) und Natriumperchlorat-Lösung (Nummer 3.5), 450 + 450 + 100 (v+v+v). Vor der Verwendung wird die Lösung durch einen 0,22-μm-Membranfilter (Nummer 4.3) filtriert und entgast (z.B. mindestens 15 min im Ultraschallbad (Nummer 4.4)).
3.7. Standardsubstanz: Amprolium, rein, 1-[(4-Amino-2-propyl-5-pyrimidinyl)methyl]-2-methyl-pyridiniumchlorid, E 750 (siehe 9.2)
3.7.1. Amprolium-Standard-Stammlösung, 500 μg/ml
Von Amprolium (Nummer 3.7) werden 50 mg auf 0,1 mg genau in einen 100-ml-Messkolben eingewogen, in 80 ml Methanol (Nummer 3.1) gelöst und 10 min in ein Ultraschallbad (Nummer 4.4) gestellt. Nach der Ultraschallbehandlung wird die Lösung auf Raumtemperatur gebracht; es wird mit Wasser zur Marke aufgefüllt und gemischt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.7.2. Amprolium-Standard-Zwischenlösung, 50 μg/ml
Von der Standard-Stammlösung (Nummer 3.7.1) werden 5,0 ml in einen 50-ml-Messkolben pipettiert; es wird mit der Extraktionslösung (Nummer 3.8) zur Marke aufgefüllt und gemischt. Bei einer Temperatur von ≤ 4 °C ist diese Lösung 1 Monat lang haltbar.
3.7.3. Kalibrierlösungen
Von der Amprolium-Standardlösung (Nummer 3.7.2) werden 0,5, 1,0 bzw. 2,0 ml jeweils in einen 50-ml-Messkolben überführt. Mit der mobilen Phase (Nummer 3.6) wird zur Marke aufgefüllt und durchmischt. Diese Lösungen enthalten jeweils 0,5, 1,0 bzw. 2,0 μg Amprolium je ml. Die Lösungen müssen vor Gebrauch frisch hergestellt werden.
3.8. Extraktionslösung
Methanol (Nummer 3.1)-Wasser-Mischung 2 + 1 (V+V).
4. Geräte
4.1. HPLC-Einrichtung mit Injektionssystem für Einspritzvolumina von 100 μl
4.1.1. HPLC-Trennsäule für die Kationenaustauschchromatografie, 125 × 4 mm, z.B. Nucleosil 10 SA, 5 oder 10 μm Korngröße, oder vergleichbare Säule.
4.1.2. UV-Detektor mit variabler Wellenlängeneinstellung oder Diodenarray-Detektor.
4.2. Membranfilter, PTFE-Material, 0,45 μm Porengröße.
4.3. Membranfilter, 0,22 μm Porengröße.
4.4. Ultraschallbad.
4.5. Mechanischer Schüttler oder Magnetrührer.
5. Verfahren
5.1. Allgemeines
5.1.1. Blindprobe
Für die Durchführung des Wiederfindungstests (Nummer 5.1.2) muss zur Prüfung, dass weder Amprolium noch Störsubstanzen vorhanden sind, eine Blindprobe untersucht werden. Die Blindprobe muss ähnlich zusammengesetzt sein wie die zu untersuchende Probe, und Amprolium oder Störsubstanzen dürfen nicht nachweisbar sein.
5.1.2. Wiederfindungstest
Die Wiederfindungsrate wird ermittelt, indem eine Blindprobe untersucht wird, die mit Amprolium angereichert wurde. Die zugesetzte Menge an Amprolium sollte der in der Probe vorhandenen Menge entsprechen. Zur Anreicherung auf einen Gehalt von 100 mg/kg werden 10,0 ml der Standard-Stammlösung (Nummer 3.7.1) in einen 250-ml-Erlenmeyerkolben überführt und auf ca. 0,5 ml eingeengt. Dann werden 50 g der Blindprobe zugegeben. Es wird gründlich gemischt, 10 min stehen gelassen und nochmals mehrfach gemischt, bevor mit der Extraktion (Nummer 5.2) fortgefahren wird.
Ist eine der zu untersuchenden Probe ähnliche Blindprobe nicht verfügbar (siehe 5.1.1), so kann ein Wiederfindungstest mithilfe des Standard-Additionsverfahrens durchgeführt werden. In diesem Fall wird die zu untersuchende Probe mit einer Amproliummenge angereichert, die der bereits in der Probe vorhandenen Menge entspricht. Diese Probe wird zusammen mit der nicht angereicherten Probe untersucht, und die Wiederfindungsrate kann durch Subtraktion ermittelt werden.
5.2. Extraktion
5.2.1. Vormischungen (Amproliumgehalt < 1 %) und Futtermittel
Je nach Amproliumgehalt werden 5 bis 40 g der Probe auf 0,01 g genau in einen 500-ml-Erlenmeyerkolben eingewogen und mit 200 ml Extraktionslösung (Nummer 3.8) versetzt. Der Kolben wird für 15 min in ein Ultraschallbad (Nummer 4.4) gestellt und anschließend 1 h auf dem Schüttelgerät geschüttelt oder auf dem Magnetrührer gerührt (Nummer 4.5). Ein aliquoter Teil des Extrakts wird mit der mobilen Phase (Nummer 3.6) auf einen Amproliumgehalt von 0,5 bis 2 μg/ml verdünnt und gemischt (siehe Bemerkung 9.3). Von dieser verdünnten Lösung werden 5 bis 10 ml durch einen Membranfilter (Nummer 4.2) filtriert. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.2.2. Vormischungen (Amproliumgehalt ≥ 1 %)
Je nach Amproliumgehalt werden 1 bis 4 g der Vormischung auf 0,001 g genau in einen 500-ml-Erlenmeyerkolben eingewogen und mit 200 ml Extraktionslösung (Nummer 3.8) versetzt. Der Kolben wird für 15 min in ein Ultraschallbad (Nummer 4.4) gestellt und anschließend 1 h auf dem Schüttelgerät geschüttelt oder auf dem Magnetrührer gerührt (Nummer 4.5). Ein aliquoter Teil des Extrakts wird mit der mobilen Phase (Nummer 3.6) auf einen Amproliumgehalt von 0,5 bis 2 μg/ml verdünnt und gemischt. Von dieser verdünnten Lösung werden 5 bis 10 ml durch einen Membranfilter (Nummer 4.2) filtriert. Anschließend wird die HPLC-Bestimmung (Nummer 5.3) durchgeführt.
5.3. HPLC-Bestimmung
5.3.1. Parameter
Die folgenden Angaben sind Richtwerte; andere Parameter können verwendet werden, sofern sie zu vergleichbaren Ergebnissen führen:
| HPLC-Trennsäule (Nummer 4.1.1): | 125 mm × 4 mm, Kationenaustausch Nucleosil 10 SA, 5 oder 10 μm Korngröße, oder vergleichbare Säule |
| Mobile Phase (Nummer 3.6): | Mischung aus Acetonitril (Nummer 3.2), Natriumdihydrogenphosphat-Lösung (Nummer 3.4) und Natriumperchloratlösung (Nummer 3.5) 450 + 450 + 100 (v + v + v). |
| Durchflussrate: | 0,7 bis 1 ml/min |
| Detektionswellenlänge: | 264 nm |
| Einspritzvolumen: | 100 μl |
Die Stabilität des chromatografischen Systems wird überprüft, indem die Kalibrierlösung (Nummer 3.7.3), die 1,0 μg/ml enthält, mehrmals eingespritzt wird, bis konstante Peakhöhen (-flächen) und Retentionszeiten erreicht sind.
5.3.2. Erstellung der Kalibrationskurve
Jede Kalibrierlösung (Nummer 3.7.3) wird mehrmals eingespritzt, und die mittleren Peakhöhen (-flächen) werden für die einzelnen Konzentrationen gemessen. Es wird eine Kalibrierkurve erstellt, indem die mittleren Peakhöhen (-flächen) auf der Ordinate und die dazugehörigen Konzentrationen in μg/ml auf der Abszisse aufgetragen werden.
5.3.3. Bestimmung der Probenlösung
Der Probenextrakt (Nummer 5.2) wird mehrmals eingespritzt, wobei dasselbe Volumen wie für die Einspritzung der Kalibrierlösungen verwendet wird. Die mittlere Peakhöhe (-fläche) der Amproliumpeaks wird ermittelt.
6. Berechnung der Ergebnisse
Aus der mittleren Höhe (Fläche) der Amproliumpeaks der Probenlösung wird anhand der Kalibrationskurve (Nummer 5.3.2) die Konzentration der Probenlösung in μg/ml bestimmt.
Der Amproliumgehalt w (in mg/kg) der Probe wird nach folgender Formel berechnet:
w = (V × c × f ) / m [mg/kg]
wobei:
| V = | Volumen der Extraktionslösung (Nummer 3.8) in ml gemäß Nummer 5.2 (d. h. 200 ml), |
| c = | Amproliumkonzentration der Probenlösung (Nummer 5.2) in μg/ml, |
| f = | Verdünnungsfaktor gemäß Nummer 5.2, |
| m = | Probeneinwaage in g. |
7. Überprüfung der Ergebnisse
7.1. Identität
Die Identität des Analyten kann durch Co-Chromatografie oder mithilfe eines Diodenarray-Detektors bestätigt werden, wobei die Spektren der Probenlösung (Nummer 5.2) und der Kalibrierlösung (Nummer 3.7.3), die 2,0 μg/ml enthält, verglichen werden.
7.1.1. Co-Chromatografie
Eine Probenlösung (Nummer 5.2) wird mit einer geeigneten Menge Kalibrierlösung (Nummer 3.7.3) angereichert. Die zugesetzte Amproliummenge muss dem Amproliumgehalt des Probenextrakts entsprechen.
Unter Berücksichtigung der zugesetzten Menge und der Verdünnung des Extrakts darf nur die Höhe des Amproliumpeaks vergrößert sein. Die Peakbreite in halber Höhe darf höchstens ± 10 % von der des Peaks der nicht angereicherten Probenlösung abweichen.
7.1.2. Diodenarray-Detektion
Die Ergebnisse werden gemäß den nachstehenden Kriterien beurteilt:
Wird eines dieser Kriterien nicht erfüllt, so gilt das Vorhandensein des Analyten als nicht bestätigt.
7.2. Wiederholbarkeit
Die Differenz zwischen den Ergebnissen zweier paralleler Bestimmungen an ein und derselben Probe darf die folgenden Werte nicht überschreiten:
7.3. Wiederfindungsrate
Bei einer angereicherten (Blind-)Probe muss die Wiederfindungsrate mindestens 90 % betragen.
8. Ergebnisse eines Ringversuchs
Bei einem Ringversuch wurden 3 Geflügelfuttermittel (Proben 1 bis 3), 1 Mineralfuttermittel (Probe 4) und 1 Vormischung (Probe 5) untersucht. Die Ergebnisse sind in der nachstehenden Tabelle zusammengefasst.
| Probe 1 (Blindprobe) | Probe 2 | Probe 3 | Probe 4 | Probe 5 | |||||||||||||
| L | 14 | 14 | 14 | 14 | 15 | ||||||||||||
| n | 56 | 56 | 56 | 56 | 60 | ||||||||||||
| Mittelwert [mg/kg] | - | 45,5 | 188 | 5.129 | 25.140 | ||||||||||||
| sr [mg/kg] | - | 2,26 | 3,57 | 178 | 550 | ||||||||||||
| VKr [%] | - | 4,95 | 1,90 | 3,46 | 2,20 | ||||||||||||
| sR [mg/kg] | - | 2,95 | 11,8 | 266 | 760 | ||||||||||||
| VKR [%] | - | 6,47 | 6,27 | 5,19 | 3,00 | ||||||||||||
| Sollgehalt [mg/kg] | - | 50 | 200 | 5.000 | 25.000 | ||||||||||||
| |||||||||||||||||
9. Bemerkungen
9.1. Enthält die Probe Thiamin, so erscheint der Thiaminpeak in der Chromatografie kurz vor dem Amproliumpeak. Bei Anwendung dieser Methode müssen Amprolium und Thiamin getrennt werden. Sind Amprolium und Thiamin nicht durch die bei dieser Methode verwendete Säule (Nummer 4.1.1) getrennt, sollten bis zu 50 % des Acetonitrilanteils der mobilen Phase (Nummer 3.6) durch Methanol ersetzt werden.
9.2. Gemäß dem britischen Arzneibuch zeigt das Spektrum einer Amproliumlösung (c = 0,02 mol/l) in Salzsäure (c = 0,1 mol/l) Maxima bei 246 nm und 262 nm. Die Absorption beträgt 0,84 bei 246 nm bzw. 0,80 bei 262 nm.
9.3. Der Extrakt muss immer mit der mobilen Phase verdünnt werden, da sich sonst die Retentionszeit des Amproliumpeaks durch Veränderungen der Ionenstärke beträchtlich verschieben kann.
I. Bestimmung des Narasingehalts
Der Narasingehalt ist mit folgenden Verfahren zu bestimmen:
J. Bestimmung des Nicarbazingehalts
Der Nicarbazingehalt ist mit folgenden Verfahren zu bestimmen:
K. Bestimmung des Decoquinatgehalts
Der Decoquinatgehalt ist mit folgenden Verfahren zu bestimmen:
L. Bestimmung des Monensingehalts
Der Monensingehalt ist mit folgenden Verfahren zu bestimmen:
M. Bestimmung des Salinomycingehalts
Der Salinomycingehalt ist mit folgenden Verfahren zu bestimmen:
N. Bestimmung des Semduramycingehalts
Der Semduramycingehalt ist mit folgenden Verfahren zu bestimmen:
O. Europäische Normen (EN)
Für die Anwendung von Artikel 34 Absatz 2 Buchstabe a der Verordnung (EU) 2017/625 sind die folgenden europäischen Normen maßgeblich:
| EN ISO 30024 "Futtermittel - Bestimmung der Phytaseaktivität" |
| EN 17050 "Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Iod in Futtermitteln mittels ICP-MS" |
| EN 17550 "Futtermittel - Bestimmung von Carotinoiden in Mischfuttermitteln und Vormischungen für Tiere mittels Hochleistungs-Flüssigchromatographie mit UV-Detektion (HPLC-UV)" |
| EN 15784 "Futtermittel - Probenahme- und Untersuchungsverfahren - Nachweis und Zählung von Bacillus spp. als Futtermittelzusatzstoff" |
| EN 15785 "Futtermittel - Probenahme- und Untersuchungsverfahren - Keimzählung von Bifidobacterium spp" |
| EN 15786 "Futtermittel - Probenahme- und Untersuchungsverfahren - Nachweis und Zählung von Pediococcus spp. als Futtermittelzusatzstoff" |
| EN 15787 "Futtermittel - Probenahme- und Untersuchungsverfahren - Nachweis und Zählung von Lactobacillus spp. als Futtermittelzusatzstoff" |
| EN 15788 "Futtermittel - Probenahme- und Untersuchungsverfahren - Nachweis und Zählung von Enterococcus spp. ( E. faecium) als Futtermittelzusatzstoff" |
| EN 15789 "Futtermittel - Probenahme- und Untersuchungsverfahren - Nachweis und Zählung von Saccharomyces cerevisiae als Futtermittelzusatzstoff" |
| EN 15510 "Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Calcium, Natrium, Phosphor, Magnesium, Kalium, Eisen, Zink, Kupfer, Mangan, Cobalt, Molybdän und Blei mittels ICP-AES" (zur Analyse der Futtermittelzusatzstoffe Cobalt oder Molybdän) |
| EN 15621 "Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Calcium, Natrium, Phosphor, Magnesium, Kalium, Schwefel, Eisen, Zink, Kupfer, Mangan und Cobalt nach Druckaufschluss mittels ICP-AES" (zur Analyse des Futtermittelzusatzstoffs Cobalt) |
| EN 16159 "Futtermittel - Bestimmung von Selen mit Atomabsorptionsspektrometrie-Hydridtechnik (HD-AAS) nach Mikrowellen-Druckaufschluss (Aufschluss mit 65 % Salpetersäure und 30 % Wasserstoffperoxid)" (zur Analyse des Futtermittelzusatzstoffs Selen) |
| EN 17053 "Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Spurenelementen, Schwermetallen und anderen Elementen in Futtermitteln mittels ICP-MS (Multimethode)" (zur Analyse der Futtermittelzusatzstoffe Cobalt, Molybdän und Selen) |
"
2) Durchgeführt von der Fachgruppe Futtermittel des Verbands deutscher landwirtschaftlicher Untersuchungs- und Forschungsanstalten (VDLUFA).
3) Die Analysemethode gemäß EN 17547 wird als Alternativmethode bei amtlichen Kontrollen zur Bestimmung der Vitamine A und E anstelle der in Teil A dieses Anhangs beschriebenen Methode zur Bestimmung von Vitamin A und der in Teil B dieses Anhangs beschriebenen Methode zur Bestimmung von Vitamin E angegeben.
4) Durchgeführt von der Fachgruppe Futtermittel des Verbands deutscher landwirtschaftlicher Untersuchungs- und Forschungsanstalten (VDLUFA).
5) Diese Methode wurde im Rahmen eines Ringversuchs für verschiedene Futtermittelmatrizen validiert. Weitere Informationen sind hier abrufbar: https://ec.europa.eu/jrc/en/eurl/feed-additives/authorisation.
6) Andere Aufschlussmethoden können verwendet werden, sofern erwiesen ist, dass sie zu vergleichbaren Ergebnissen führen (z.B. Mikrowellen-Druckaufschluss).
7) Grünfutter (frisch oder getrocknet) kann größere Mengen pflanzlicher Kieselsäure enthalten, welche Spurenelemente binden kann und daher entfernt werden muss. Bei Proben dieser Futtermittel muss also nach folgendem geänderten Verfahren vorgegangen werden: Das Verfahren 5.1.1.1 wird bis zur Filtration durchgeführt. Das den unlöslichen Rückstand enthaltende Filterpapier wird 2-mal mit kochendem Wasser ausgewaschen, in eine Quarz- oder Platinschale gegeben
und im Muffelofen (Nummer 4.1) bei weniger als 550 °C bis zur vollständigen Elimination aller Kohlepartikel verascht. Nach dem Abkühlen werden einige Tropfen Wasser und danach 10-15 ml Fluorwasserstoffsäure (Nummer 3.4) zugegeben und bei ca. 150 °C zur Trockne eingedampft. Verbleibt im Rückstand noch Kieselsäure, so wird diese erneut in einigen ml Fluorwasserstoffsäure (Nummer 3.4) gelöst und anschließend zur Trockne eingedampft. Dann werden 5 Tropfen Schwefelsäure (Nummer 3.5) zugesetzt und so lange erhitzt, bis keine weißen Dämpfe mehr auftreten. Nach Zugabe von 5 ml 6 mol/l Salzsäure (Nummer 3.2) und etwa 30 ml Wasser wird erhitzt und die Lösung in den 250-ml-Messkolben filtriert. Letzterer wird mit Wasser zur Marke aufgefüllt (HCl-Konzentration etwa 0,5 mol/l). Anschließend wird wie ab 5.1.2 beschrieben weiterverfahren.
8) The Analyst 108, 1983, S. 1252-1256.
9) Das Verfahren kann auch für die Bestimmung des Diclazurilgehalts in Einzelfuttermitteln angewendet werden.
10) Eine längere Haltbarkeit (von bis zu einem Jahr) kann möglich sein, muss jedoch von dem einzelnen Labor bestätigt werden.
| Anhang V |
"Anhang V
Analysemethoden zur Untersuchung von Futtermitteln auf unerwünschte Stoffe
A. Bestimmung des Gehalts an Dioxinen (PCDD/PCDF) und PCB
Kapitel I
Probenahmeverfahren und Auswertung von Analyseergebnissen
1. Zweck und Anwendungsbereich
Die Proben für die amtliche Untersuchung des Gehalts an polychlorierten Dibenzo-p-dioxinen (PCDD), polychlorierten Dibenzofuranen (PCDF) sowie dioxinähnlichen polychlorierten Biphenylen (PCB) 1 und nicht dioxinähnlichen PCB in Futtermitteln werden nach den in Anhang I beschriebenen Verfahren genommen. Hinsichtlich der Untersuchung auf Stoffe oder Erzeugnisse, die in Futtermitteln gleichmäßig verteilt sind, gelten die quantitativen Anforderungen gemäß Anhang I Nummer 5.1. Die mit diesem Verfahren gewonnenen Sammelproben sind als repräsentativ für die betreffenden Partien oder Teilpartien anzusehen. Anhand der bei den Laborproben bestimmten Gehalte wird festgestellt, ob die in der Richtlinie 2002/32/EG festgesetzten Höchstgehalte eingehalten wurden.
Für die Zwecke dieses Teils gelten die Begriffsbestimmungen in Anhang I der Durchführungsverordnung (EU) 2021/808 der Kommission 2.
Darüber hinaus gelten für die Zwecke dieses Teils folgende Begriffsbestimmungen:
| "Screening-Verfahren" sind Verfahren, die zur Auswahl derjenigen Proben genutzt werden, deren Gehalt an PCDD/F und dioxinähnlichen PCB die Höchstgehalte oder die Aktionsgrenzwerte überschreitet. Sie müssen auf kostengünstige Weise einen hohen Probendurchsatz erlauben, was die Chancen erhöht, neue Vorfälle mit hoher Exposition und Gesundheitsgefahren für die Verbraucher aufzudecken. Screening-Verfahren beruhen auf bioanalytischen oder GC-MS-Verfahren. Ergebnisse von Proben, in denen der Cut-off-Wert für die Überprüfung der Konformität mit dem Höchstgehalt überschritten wird, sind durch eine erneute vollständige Analyse der ursprünglichen Probe mittels eines Bestätigungsverfahrens zu überprüfen. |
| "Bestätigungsverfahren" sind Verfahren, die vollständige oder ergänzende Daten liefern, mit denen die PCDD/F und dioxinähnlichen PCB am Höchstgehalt oder erforderlichenfalls am Aktionsgrenzwert eindeutig identifiziert und quantifiziert werden können. Bei diesen Verfahren kommen Gaschromatografie/hochauflösende Massenspektrometrie (GC-HRMS) oder Gaschromatografie/Tandem-Massenspektrometrie (GC-MS/MS) zum Einsatz. |
2. Übereinstimmung der Partie bzw. Teilpartie mit den Anforderungen in Bezug auf die Höchstgehalte
2.1. Nicht dioxinähnliche PCB
Die Partie oder Teilpartie entspricht den Anforderungen in Bezug auf den Höchstgehalt, wenn das Ergebnis der Untersuchung für die Summe von PCB 28, PCB 52, PCB 101, PCB 138, PCB 153 und PCB 180 (im Folgenden "nicht dioxinähnliche PCB") den in der Richtlinie 2002/32/EG festgelegten Höchstgehalt unter Berücksichtigung der erweiterten Messunsicherheit nicht überschreitet 3 . Die Partie oder Teilpartie entspricht nicht den Anforderungen in Bezug auf den Höchstgehalt gemäß der Richtlinie 2002/32/EG, wenn das Mittel der durch Zweitanalyse 4 ermittelten Obergrenzen ("upper-bound") 5 zweier Untersuchungsergebnisse unter Berücksichtigung der erweiterten Messunsicherheit den Höchstgehalt zweifelsfrei überschreitet, d. h. zur Beurteilung, ob die Höchstgehalte eingehalten werden, wird die gemessene Konzentration nach Abzug der erweiterten Messungenauigkeit herangezogen.
Die erweiterte Messunsicherheit wird mithilfe eines Erweiterungsfaktors von 2 berechnet, der zu einem Grad des Vertrauens von ca. 95 % führt. Eine Partie oder Teilpartie entspricht nicht den Vorgaben, wenn das Mittel der gemessenen Werte abzüglich der erweiterten Messunsicherheit des Mittels über dem Höchstgehalt liegt.
Die in den vorstehenden Absätzen unter dieser Nummer genannten Bestimmungen gelten für das Untersuchungsergebnis der für die amtliche Kontrolle entnommenen Probe. Im Falle einer Analyse für die Zwecke eines zweiten Sachverständigengutachtens oder für Referenzwecke gelten die einzelstaatlichen Bestimmungen.
2.2. Für PCDD/F und dioxinähnliche PCB
Die Partie oder Teilpartie entspricht den Anforderungen in Bezug auf die Höchstgehalte, wenn das Ergebnis einer einzelnen Untersuchung,
Für Screening-Assays ist ein Cut-off-Wert festzulegen, anhand dessen entschieden wird, ob eine Probe den jeweiligen Höchstgehalten für PCDD/F bzw. die Summe von PCDD/F und dioxinähnlichen PCB entspricht.
Die Partie oder Teilpartie entspricht nicht den Anforderungen in Bezug auf den Höchstgehalt gemäß der Richtlinie 2002/32/EG, wenn das Mittel der durch Zweitanalyse 6 mit einem Bestätigungsverfahren ermittelten Obergrenzen ("upper-bound") 7 zweier Untersuchungsergebnisse unter Berücksichtigung der erweiterten Messunsicherheit den Höchstgehalt zweifelsfrei überschreitet, d. h., zur Beurteilung, ob die Höchstgehalte eingehalten werden, wird die gemessene Konzentration nach Abzug der erweiterten Messungenauigkeit herangezogen.
Die erweiterte Messunsicherheit wird mithilfe eines Erweiterungsfaktors von 2 berechnet, der zu einem Grad des Vertrauens von ca. 95 % führt. Eine Partie oder Teilpartie entspricht nicht den Vorgaben, wenn das Mittel der gemessenen Werte abzüglich der erweiterten Messunsicherheit des Mittels über dem Höchstgehalt liegt.
Die Summe der geschätzten erweiterten Messunsicherheiten der getrennten Analyseergebnisse der PCDD/F und dioxinähnlichen PCB ist für die Summe der PCDD/F und dioxinähnlichen PCB zu verwenden.
Die in den vorstehenden Absätzen unter dieser Nummer genannten Bestimmungen gelten für das Untersuchungsergebnis der für die amtliche Kontrolle entnommenen Probe. Im Falle einer Analyse für Rechtfertigungs- oder Referenzwecke gelten die einzelstaatlichen Bestimmungen.
3. Ergebnisse, die die Aktionsgrenzwerte gemäß Anhang II der Richtlinie 2002/32/EG überschreiten
Aktionsgrenzwerte dienen als Instrument zur Auswahl der Proben in Fällen, in denen eine Kontaminationsquelle gefunden wird und Maßnahmen zu deren Eindämmung oder Beseitigung getroffen werden müssen. Durch Screening-Verfahren sind die geeigneten Cut-off-Werte für die Auswahl dieser Proben festzulegen. Wenn die Bestimmung einer Kontaminationsquelle und deren Eindämmung oder Beseitigung erhebliche Anstrengungen erfordert, ist es angezeigt, die Überschreitung der Aktionsgrenzwerte durch eine Zweitanalyse im Bestätigungsverfahren und unter Berücksichtigung der erweiterten Messunsicherheit zu bestätigen 8.
Kapitel II
Probenvorbereitung und Anforderungen an Untersuchungsverfahren zur amtlichen Kontrolle des Gehalts an Dioxinen (PCDD/F) und dioxinähnlichen PCB in Futtermitteln
1. Anwendungsbereich
Die in diesem Kapitel beschriebenen Anforderungen gelten, wenn Futtermittel zur amtlichen Kontrolle des Gehalts an 2,3,7,8-substituierten PCDD/F und dioxinähnlichen PCB sowie für die Probenvorbereitung und Untersuchungsanforderungen zu anderen regulatorischen Zwecken, darunter die Kontrollen der Futtermittelunternehmer zur Gewährleistung der Vorschriftsmäßigkeit gemäß der Verordnung (EG) Nr. 183/2005 des Europäischen Parlaments und des Rates 9, untersucht werden.
Die Überwachung von Futtermitteln auf Vorhandensein von PCDD/F und dioxinähnlichen PCB kann mit zwei unterschiedlichen Verfahrensarten erfolgen:
a) Screening-Verfahren
Ziel der Screening-Verfahren ist die Auswahl derjenigen Proben, deren Gehalt an PCCD/F und dioxinähnlichen PCB die Höchstgehalte oder die Aktionsgrenzwerte überschreitet. Screening-Verfahren sollen auf kostengünstige Weise einen hohen Probendurchsatz erlauben, was die Chancen erhöht, neue Vorfälle mit hoher Exposition und Gesundheitsgefahren für die Verbraucher aufzudecken. Ihre Anwendung hat insbesondere die Vermeidung falsch-negativer Ergebnisse zum Ziel. Sie können bioanalytische und GC-MS-Verfahren umfassen.
Bei Screening-Verfahren wird das Analyseergebnis mit einem Cut-off-Wert verglichen und angegeben, ob der Höchstgehalt oder Aktionsgrenzwert möglicherweise überschritten wird oder nicht. Die Konzentration von PCDD/F und der Summe von PCDD/F und dioxinähnlichen PCB in Proben, in denen eine Überschreitung des Höchstgehalts vermutet wird, muss durch ein Bestätigungsverfahren ermittelt oder bestätigt werden.
Darüber hinaus können Screening-Verfahren Hinweise auf den in der Probe vorhandenen Gehalt an PCDD/F und dioxinähnlichen PCB liefern. Bei bioanalytischen Screening-Verfahren wird das Ergebnis in bioanalytischen Äquivalenten (BEQ) und bei physikalisch-chemischen GC-MS-Verfahren in Toxizitätsäquivalenten (TEQ) ausgedrückt. Die in Zahlen ausgedrückten Ergebnisse von Screening-Verfahren sind geeignet, die Konformität bzw. die vermutete Nichtkonformität oder das Überschreiten von Aktionsgrenzwerten anzuzeigen und weisen außerdem für den Fall einer Weiterverfolgung mittels Bestätigungsverfahren auf die Gehaltsbereiche hin. Sie sind nicht für Zwecke wie die Bewertung von Hintergrundkonzentrationen, die Schätzung der Aufnahme, die Verfolgung der zeitlichen Entwicklung von Gehalten oder die Neubewertung von Aktionsgrenzwerten und Höchstgehalten geeignet.
b) Bestätigungsverfahren
Bestätigungsverfahren ermöglichen die eindeutige Identifizierung und Quantifizierung von in einer Probe vorhandenen PCDD/F und dioxinähnlichen PCB und liefern vollständige Informationen über den Gehalt der einzelnen Kongenere. Sie erlauben somit die Kontrolle von Höchstgehalten und Aktionsgrenzwerten, einschließlich der Bestätigung von mittels Screening-Verfahren erzielten Ergebnissen. Außerdem können die Ergebnisse für weitere Zwecke genutzt werden, wie die Bestimmung der Belastung im niedrigen Hintergrundbereich bei der Futtermittelüberwachung, die Verfolgung der zeitlichen Entwicklung, die Expositionsbewertung und für den Aufbau einer Datenbank im Hinblick auf eine mögliche Neubewertung der Aktionsgrenzwerte und Höchstgehalte. Sie sind außerdem bei der Feststellung von Kongeneren-Mustern zur Bestimmung der Quelle einer möglichen Kontamination von Bedeutung. Solche Verfahren verwenden GC-HRMS. Zur Bestätigung der Konformität oder Nichtkonformität mit dem Höchstgehalt kann auch die GC-MS/MS angewendet werden.
2. Hintergrund
Zur Berechnung der TEQ-Konzentrationen werden die Konzentrationen der einzelnen Stoffe in einer bestimmten Probe mit den jeweiligen Toxizitätsäquivalenzfaktoren (TEF) (siehe Fußnote 1 in Kapitel I) multipliziert und dann addiert, woraus sich die Gesamtkonzentration an dioxinähnlichen Verbindungen, ausgedrückt in TEQ, ergibt.
Für die Zwecke dieses Teils A entspricht die akzeptierte spezifische Bestimmungsgrenze eines einzelnen Kongeners dem niedrigsten Analytgehalt, der sich mit angemessener statistischer Zuverlässigkeit quantifizieren lässt und die Identifizierungskriterien erfüllt, wie sie in international anerkannten Normen, z.B. in der Norm EN 16215:2012 (Futtermittel - Bestimmung von Dioxinen und dioxin-ähnlichen PCBs mittels GC/HRMS und von Indikator-PCBs mittels GC/HRMS) und/oder in den überarbeiteten EPA-Methoden 1613 und 1668, beschrieben sind.
Die Bestimmungsgrenze eines einzelnen Kongeners lässt sich bestimmen als
Mit bioanalytischen Methoden erhält man kein Ergebnis auf Ebene der Kongeneren, sondern lediglich einen Hinweis 10 auf den TEQ-Gehalt, der in BEQ ausgedrückt wird, wodurch der Tatsache Rechnung getragen wird, dass möglicherweise nicht alle in einem Probenextrakt vorliegenden Verbindungen, die ein Signal erzeugen, allen Voraussetzungen des TEQ-Prinzips genügen.
Screening- und Bestätigungsverfahren können nur dann zur Kontrolle einer bestimmten Matrix angewendet werden, wenn sie empfindlich genug sind, Gehalte im Bereich der Aktionsgrenzwerte oder Höchstgehalte zuverlässig zu bestimmen.
3. Anforderungen an die Qualitätssicherung
3.1. Auf jeder Stufe des Probenahme- und Analyseverfahrens sind Maßnahmen zur Vermeidung von Kreuzkontamination zu treffen.
3.2. Die Proben sind in hierfür geeigneten Glas-, Aluminium-, Polypropylen- oder Polyethylen-Behältnissen zu lagern und zu transportieren, sodass der Gehalt der Proben an PCDD/F und dioxinähnlichen PCB nicht verfälscht wird. Spuren von Papierstaub sind vom Probenbehälter zu entfernen.
3.3. Lagerung und Transport der Proben haben so zu erfolgen, dass die Futtermittelprobe unversehrt erhalten bleibt.
3.4. Sofern zutreffend, sind die einzelnen Laborproben mithilfe eines Verfahrens, mit dem nachweislich eine vollständige Homogenisierung erreicht wird, fein zu mahlen und gründlich zu mischen (z.B. so fein gemahlen, dass die Probe durch ein Sieb mit einer Maschenweite von 1 mm passt). Falls die Proben einen zu hohen Feuchtigkeitsgehalt aufweisen, sind sie vor dem Zermahlen zu trocknen.
3.5. Die Reagenzien, Glasgeräte und die weitere Ausrüstung sind auf Faktoren, die möglicherweise die TEQ- und BEQ-basierten Ergebnisse verfälschen könnten, zu kontrollieren.
3.6. Es ist eine Methodenleerwert-Untersuchung durchzuführen, bei der das gesamte Analyseverfahren durchgeführt und nur die Probe weggelassen wird.
3.7. Bei Anwendung bioanalytischer Methoden ist zu überprüfen, dass sämtliche Glasgeräte und Lösungsmittel, die bei der Analyse verwendet werden, frei von Verbindungen sind, die die Erkennung der Zielverbindungen im Arbeitsbereich beeinträchtigen könnten. Glasgeräte sind mit Lösungsmitteln zu spülen oder auf Temperaturen zu erhitzen, die geeignet sind, alle Spuren von PCDD/F, dioxinähnlichen Verbindungen und interferierenden Verbindungen von der Oberfläche der Geräte zu entfernen.
3.8. Die Menge der für die Extraktion verwendeten Probe muss ausreichend groß sein, um die Anforderungen hinsichtlich eines ausreichend niedrigen Arbeitsbereichs, der den Konzentrationsbereich der Höchstgehalte oder Aktionsgrenzwerte beinhaltet, zu erfüllen.
3.9. Zur spezifischen Vorbereitung der Proben der zu untersuchenden Erzeugnisse sind Verfahren gemäß international anerkannten Leitlinien, d. h. EN ISO 6498, anzuwenden.
4. Anforderungen an Laboratorien
4.1. Gemäß den Bestimmungen der Verordnung (EU) 2017/625 müssen die Laboratorien von einer anerkannten Stelle akkreditiert sein, die nach ISO/IEC Guide 58 arbeitet, damit sichergestellt ist, dass die Laboratorien bei der Untersuchung Qualitätssicherungsverfahren anwenden. Die Laboratorien müssen gemäß der Norm EN ISO/IEC 17025 akkreditiert sein. Es sind die in den technischen Leitlinien für die Schätzung der Messunsicherheit und der Bestimmungsgrenzen für die Untersuchung auf PCDD/F und PCB beschriebenen Grundsätze zu befolgen 11.
4.2. Die Laborleistung ist durch die kontinuierliche erfolgreiche Teilnahme an Laborvergleichsuntersuchungen zur Ermittlung des Gehalts an PCDD/F und dioxinähnlichen PCB in den entsprechenden Futtermittelmatrices und Konzentrationsbereichen unter Beweis zu stellen.
4.3. Laboratorien, die zur Routinekontrolle von Proben Screening-Verfahren anwenden, müssen eng mit Laboratorien zusammenarbeiten, die Bestätigungsverfahren anwenden, sowohl zur Qualitätssicherung als auch zur Bestätigung der Ergebnisse verdächtiger Proben.
5. Grundlegende Anforderungen an Verfahren zur Untersuchung auf Dioxine (PCDD/F) und dioxinähnliche PCB
5.1. Niedriger Arbeitsbereich und niedrige Bestimmungsgrenzen
Bei PCDD/F müssen die nachweisbaren Mengen wegen der extrem hohen Toxizität einiger dieser Verbindungen im oberen Femtogramm-Bereich (10-15g) liegen. Bei den meisten PCB-Kongeneren ist eine Bestimmungsgrenze im Bereich Nanogramm (10-9g) bereits ausreichend. Zur Messung der toxischeren dioxinähnlichen PCB-Kongenere (insbesondere der non-orthosubstituierten Kongenere) muss das untere Ende des Arbeitsbereichs bis in den unteren Pikogramm-Bereich (10-12g) reichen. Bei allen anderen PCB-Kongeneren ist eine Bestimmungsgrenze im Nanogramm-Bereich (10-9g) ausreichend.
5.2. Hohe Selektivität (Spezifizität)
5.2.1. PCDD/F und dioxinähnliche PCB müssen von einer Vielzahl anderer, gemeinsam extrahierter und möglicherweise interferierender Verbindungen unterschieden werden, die in Konzentrationen von bis zu mehreren Größenordnungen höher als diejenigen der interessierenden Analyten vorhanden sind. Bei GC-MS-Verfahren ist eine Unterscheidung zwischen verschiedenen Kongeneren erforderlich, beispielsweise zwischen toxischen (z.B. die siebzehn 2,3,7,8-substituierten PCDD/F sowie die zwölf dioxinähnlichen PCB) und anderen Kongeneren.
5.2.2. Bioanalytische Methoden müssen einen Nachweis der Zielverbindungen als Summe der PCDD/F und/oder dioxinähnlichen PCB ermöglichen. Ziel der Probenaufreinigung muss es sein, Verbindungen, die falsch-positive Ergebnisse verursachen könnten, oder Verbindungen, die das Signal schwächen und dadurch falsch-negative Ergebnisse verursachen könnten, zu entfernen.
5.3. Hohe Genauigkeit (Richtigkeit und Präzision, beobachtete Bioassay-Wiederfindung)
5.3.1. Bei Anwendung von GC-MS-Verfahren muss die Bestimmung eine valide Schätzung der tatsächlichen Konzentration in einer Probe ermöglichen. Hohe Genauigkeit ist notwendig, damit die Zurückweisung eines Ergebnisses einer Probenuntersuchung aufgrund der geringen Zuverlässigkeit des bestimmten TEQ-Gehalts vermieden wird. Die Genauigkeit des Analyseverfahrens wird angegeben durch die Richtigkeit (Differenz zwischen dem gemessenen Mittelwert eines Analyten in einem zertifizierten Material und seinem zertifizierten Wert, ausgedrückt als Prozentsatz dieses Wertes) und die Präzision (RSDR; relative Standardabweichung, berechnet aus unter Vergleichbarkeitsbedingungen ermittelten Ergebnissen).
5.3.2. Für bioanalytische Methoden ist die beobachtete Bioassay-Wiederfindung zu bestimmen. Die beobachtete Bioassay-Wiederfindung ist der BEQ-Gehalt, berechnet anhand einer TCDD-Kalibrierkurve oder einer PCB-126-Kalibrierkurve nach Korrektur um den Blindwert, geteilt durch den mittels Bestätigungsverfahren bestimmten TEQ-Wert. Dadurch sollen Faktoren wie der Verlust von PCDD/F und dioxinähnlichen Verbindungen während der einzelnen Extraktions- bzw. Reinigungsschritte, die Verstärkung oder Abschwächung des Signals durch mitextrahierte Verbindungen (agonistische bzw. antagonistische Wirkung), die Qualität der Kurvenanpassung oder Unterschiede zwischen TEF- und REP-(Relative-Potency-)Werten korrigiert werden. Die beobachtete Bioassay-Wiederfindung wird anhand geeigneter Referenzproben berechnet, die im Bereich der interessierenden Konzentration liegen und repräsentative Kongeneren-Muster aufweisen.
5.4. Validierung im Bereich des Höchstgehalts und allgemeine Qualitätssicherungsmaßnahmen
5.4.1. Die Laboratorien haben im Rahmen der Validierung und während der Routineanalytik den Nachweis der Leistungsfähigkeit eines Verfahrens im Bereich des Höchstgehalts, z.B. 0,5x, 1x und 2x Höchstgehalt mit einem akzeptablen Variationskoeffizienten für wiederholte Untersuchung, zu führen.
5.4.2. Als interne Qualitätssicherungsmaßnahmen müssen regelmäßige Methodenleerwert-Kontrollen und Experimente mit dotierten Proben oder Analysen von Kontrollproben (sofern erhältlich, vorzugsweise zertifiziertes Referenzmaterial) durchgeführt werden. Für Methodenleerwert-Kontrollen, Experimente mit dotierten Proben und Analysen von Kontrollproben sind Qualitätskontroll-Charts anzufertigen und zu prüfen, damit sichergestellt ist, dass die Analyseleistungsfähigkeit den Anforderungen genügt.
5.5. Bestimmungsgrenze
5.5.1. Bei einem bioanalytischen Screening-Verfahren ist eine Ermittlung der Bestimmungsgrenze (LOQ) nicht unbedingt erforderlich; es muss jedoch nachgewiesen sein, dass mit dem Verfahren eine Unterscheidung zwischen dem Methodenleerwert und dem Cut-off-Wert möglich ist. Wird ein BEQ-Gehalt angegeben, ist eine Konzentration festzulegen, ab der Ergebnisse mitgeteilt werden (Meldewert), um Proben, die ein Ergebnis unterhalb davon aufweisen, entsprechend einstufen zu können. Der Meldewert muss sich mindestens um den Faktor 3 von Methodenleerwert-Proben mit einem Signal unterhalb des Arbeitsbereichs unterscheiden. Er ist daher auf der Grundlage von Proben zu berechnen, die ungefähr den erforderlichen Mindestgehalt an Zielverbindungen enthalten, und nicht aus dem Signal/Rausch-Verhältnis oder einem Assay-Leerwert.
5.5.2. Die LOQ liegt beim Bestätigungsverfahren bei etwa einem Fünftel des Höchstgehalts.
5.6. Analysekriterien
Damit die Ergebnisse der Bestätigungs- oder Screening-Verfahren zuverlässig sind, müssen folgende Kriterien im Bereich des Höchstgehalts für den TEQ-Wert bzw. den BEQ-Wert erfüllt sein, entweder bestimmt als Gesamt-TEQ bzw. Gesamt-BEQ (Summe der PCDD/F und dioxinähnlichen PCB) oder separat für PCDD/F und dioxinähnliche PCB.
| Screening mit bioanalytischen oder physikalisch-chemischen Verfahren | Bestätigungsverfahren | |
| Falsch-negativ-Rate * | < 5 % | |
| Richtigkeit | -20 % bis +20 % | |
| Wiederholbarkeit (RSDr) | < 20 % | |
| Laborpräzision (RSDR) | < 25 % | < 15 % |
| *) Bezogen auf die Höchstgehalte. | ||
5.7. Besondere Anforderungen an Screening-Verfahren
5.7.1. Sowohl GC-MS-Verfahren als auch bioanalytische Methoden dürfen zum Screening angewendet werden. Bei GC-MS-Verfahren sind die unter Nummer 6 festgelegten Anforderungen zu erfüllen. Für zellbasierte bioanalytische Methoden sind unter Nummer 7 spezifische Anforderungen festgelegt.
5.7.2. Laboratorien, die zur Routinekontrolle von Proben Screening-Verfahren verwenden, müssen eng mit Laboratorien zusammenarbeiten, die das Bestätigungsverfahren anwenden.
5.7.3. Der Nachweis der Leistungsfähigkeit des Screening-Verfahrens ist während der Routineanalyse durch Qualitätssicherung und permanente Methodenvalidierung zu erbringen. Es muss ein kontinuierliches Programm zur Kontrolle der als konform beurteilten Analysenergebnisse geben.
5.7.4. Prüfung auf eine mögliche Unterdrückung der Zellantwort und auf Zytotoxizität:
20 % der Probenextrakte sind während des Routine-Screenings sowohl ohne als auch mit Zusatz einer dem Höchstgehalt oder dem Aktionsgrenzwert entsprechenden Menge von 2,3,7,8-TCDD zu analysieren, damit überprüft werden kann, ob das Signal möglicherweise durch interferierende Stoffe im Probenextrakt unterdrückt wird. Die gemessene Konzentration der dotierten Probe ist mit der Summe aus der Konzentration der nicht dotierten Probe und der Konzentration der Dotierung zu vergleichen. Liegt die gemessene Konzentration mehr als 25 % unter der berechneten (Summen-)Konzentration, ist dies ein Hinweis auf eine mögliche Signalunterdrückung und die entsprechende Probe ist einem GC-HRMS-Bestätigungsverfahren zu unterziehen. Die Ergebnisse sind anhand von Qualitätskontroll-Charts zu überwachen.
5.7.5. Qualitätssicherung bei als konform beurteilten Proben:
Etwa 2-10 % der konformen Proben sind, je nach Probenmatrix und Laborerfahrung, mittels GC-HRMS zu bestätigen.
5.7.6. Bestimmung der Falsch-negativ-Raten auf Grundlage der Qualitätssicherungsdaten:
Die Rate falsch-negativer Ergebnisse beim Screening von Proben unter- und oberhalb der Höchstgehalte oder Aktionsgrenzwerte ist zu bestimmen. Der tatsächliche Anteil der falsch-negativen Ergebnisse muss unter 5 % liegen. Wenn im Rahmen der Qualitätssicherung je Matrix/Matrixgruppe mindestens 20 Proben bestätigt wurden, ist aus dieser Datenbasis die Falsch-negativ-Rate zu ermitteln. Die zur Ermittlung der Falsch-negativ-Rate mindestens erforderlichen 20 Ergebnisse können auch die Ergebnisse von in Ringversuchen oder im Rahmen eines Kontaminationsereignisses untersuchten Proben mit einschließen, die einen Konzentrationsbereich von beispielsweise bis zum doppelten Höchstgehalt abdecken. Die Proben müssen die häufigsten Kongeneren-Muster abdecken, die verschiedene Kontaminationsquellen repräsentieren.
Obwohl Screening-Verfahren hauptsächlich auf die Ermittlung derjenigen Proben abzielen, in denen der Aktionsgrenzwert überschritten wird, ist das ausschlaggebende Kriterium zur Bestimmung der Falsch-negativ-Rate der Höchstgehalt, unter Berücksichtigung der erweiterten Messunsicherheit des Bestätigungsverfahrens.
5.7.7. Alle Proben, die im Screening-Verfahren als möglicherweise nicht konform beurteilt werden, müssen durch eine erneute vollständige Untersuchung der ursprünglichen Probe im Rahmen eines Bestätigungsverfahrens überprüft werden. Diese Proben dürfen auch zur Bewertung der Rate der falsch-positiven Ergebnisse herangezogen werden. Im Rahmen von Screening-Verfahren entspricht die Falsch-Positiv-Rate dem Anteil derjenigen Ergebnisse, von denen sich im Bestätigungsverfahren herausstellt, dass sie konform sind, nachdem sie zunächst als möglicherweise nicht konform eingestuft worden waren. Die Vorteile des Screening-Verfahrens sind auf Grundlage eines Vergleichs zwischen der Zahl der falsch-positiven Proben und der Gesamtzahl der untersuchten Proben zu bewerten. Dabei muss der Anteil der falsch-positiven Proben so gering sein, dass ein Screening vorteilhaft ist.
5.7.8. Unter Validierungsbedingungen müssen bioanalytische Methoden einen stichhaltigen Hinweis auf den TEQ-Gehalt ergeben, berechnet und ausgedrückt als BEQ.
Bei unter wiederholten Bedingungen angewandten bioanalytischen Methoden wäre in der Regel die laborinterne Wiederholbarkeit RSDr geringer als die unter Vergleichbarkeitsbedingungen (RSDR).
6. Besondere Anforderungen an GC-MS-Verfahren für Screening- oder Bestätigungszwecke
6.1. Annehmbare Differenzen zwischen Obergrenze ("upper-bound") und Untergrenze ("lower-bound") (WHO-TEQ-Ergebnisse)
Zur Bestätigung der Überschreitung von Höchstgehalten oder erforderlichenfalls von Aktionsgrenzwerten darf die Differenz zwischen Ober- und Untergrenze nicht mehr als 20 % betragen.
6.2. Kontrolle der Wiederfindungsrate
6.2.1. Die Zugabe von 13C-markierten 2,3,7,8-chlorsubstituierten internen PCDD/F-Standards und 13C-markierten internen dioxinähnlichen PCB-Standards ist ganz zu Anfang des Analyseverfahrens, z.B. vor der Extraktion, durchzuführen, damit das Analyseverfahren validiert werden kann. Bei jeder der tetra- bis octachlorierten homologen Gruppen von PCDD/F und bei jeder der homologen Gruppen von dioxinähnlichen PCB muss mindestens ein Kongener zugegeben werden (alternativ dazu mindestens ein Kongener je massenspektrometrisch ausgewählter Ionenaufzeichnungsfunktion zur Überwachung von PCDD/F und dioxinähnlichen PCB). Im Fall der Bestätigungsverfahren sind alle 17 13C-markierten 2,3,7,8-substituierten internen PCDD/F-Standards und alle 12 13C-markierten internen dioxinähnlichen PCB-Standards zu verwenden.
6.2.2. Die relativen Responsefaktoren sind mittels geeigneter Kalibrierlösungen auch für diejenigen Kongenere zu bestimmen, bei denen kein 13C-markiertes Analogon zugegeben ist.
6.2.3. Bei Futtermitteln pflanzlichen Ursprungs und Futtermitteln tierischen Ursprungs, die weniger als 10 % Fett enthalten, ist die Zugabe der internen Standards vor der Extraktion obligatorisch. Bei Futtermitteln tierischen Ursprungs, die mehr als 10 % Fett enthalten, sind die internen Standards entweder vor oder nach der Fettextraktion zuzugeben. Die Extraktionseffizienz ist auf geeignete Weise zu validieren, abhängig davon, auf welcher Stufe die internen Standards zugegeben werden.
6.2.4. Vor der GC-MS-Analyse sind 1 oder 2 Wiederfindungs-(Surrogat-)Standard(s) zuzugeben.
6.2.5. Es ist eine Kontrolle der Wiederfindungsrate erforderlich. Bei Bestätigungsverfahren müssen die Wiederfindungsraten der einzelnen internen Standards zwischen 60 und 120 % liegen. Geringere oder höhere Wiederfindungsraten für einzelne Kongenere, insbesondere für einige hepta- und octachlorierte Dibenzo-p-dioxine und Dibenzofurane, werden unter der Bedingung akzeptiert, dass ihr Beitrag zum TEQ-Wert 10 % des gesamten TEQ-Werts (basierend auf der Summe von PCDD/F und dioxinähnlichen PCB) nicht übersteigt. Bei GC-MS-Screening-Verfahren müssen die Wiederfindungen zwischen 30 und 140 % liegen.
6.3. Entfernung interferierender Stoffe
6.4. Kalibrierung mittels Standardkurve
Die Kalibrierkurve muss alle jeweils relevanten Bereiche der Höchstgehalte oder Aktionsgrenzwerte abdecken.
6.5. Besondere Kriterien für Bestätigungsverfahren
Bei der HRMS muss die Auflösung für den gesamten Massenbereich bei 10 % Tal in der Regel gleich oder größer als 10.000 sein.
Erfüllung weiterer Identifizierungs- und Bestätigungskriterien, wie sie in international anerkannten Normen, z.B. in der Norm EN 16215:2012 (Futtermittel - Bestimmung von Dioxinen und dioxin-ähnlichen PCBs mittels GC/HRMS und von Indikator-PCBs mittels GC/HRMS) und/oder in den überarbeiteten EPA-Methoden 1613 und 1668, beschrieben sind.
Messung von mindestens 2 spezifischen Vorläufer-Ionen, jeweils mit einem spezifischen zugehörigen Übergangsprodukt-Ion für alle markierten und nicht markierten Analyten im Untersuchungsbereich.
Zulässige Höchsttoleranz für relative Ionenintensitäten von ± 15 % für ausgewählte Übergangs-Produkt-Ionen im Vergleich zu berechneten oder gemessenen Werten (Mittelwert aus Kalibrierstandards) unter Anwendung identischer MS/MS-Bedingungen, insbesondere Kollisionsenergie und Kollisionsgasdruck, für jeden Übergang eines Analyts.
Festlegung der Auflösung für jeden Quadrupol gleichwertig oder besser als die Einheitsmassenauflösung (Einheitsmassenauflösung: ausreichende Auflösung zur Auftrennung zweier Peaks, die sich um eine Masseneinheit unterscheiden), um mögliche Auswirkungen von Interferenzen auf die interessierenden Analyten zu minimieren.
Erfüllung der weiteren Kriterien, wie sie in international anerkannten Normen, z.B. in der Norm EN 16215:2012 (Futtermittel - Bestimmung von Dioxinen und dioxin-ähnlichen PCBs mittels GC/HRMS und von Indikator-PCBs mittels GC/HRMS) und/oder in den überarbeiteten EPA-Methoden 1613 und 1668, beschrieben sind, die Pflicht zur Verwendung von GC-HRMS ausgenommen.
7. Besondere Anforderungen an bioanalytische Methoden
Bioanalytische Methoden sind Verfahren, die auf der Anwendung biologischer Grundsätze beruhen, beispielsweise zellbasierte Assays, Rezeptor-Assays oder Immunoassays. Unter dieser Nummer werden allgemeine Anforderungen an bioanalytische Methoden festgelegt.
Mit einem Screening-Verfahren wird eine Probe prinzipiell entweder als konform oder als vermutlich nicht konform eingestuft. Dazu wird der berechnete BEQ-Wert mit dem Cut-off-Wert verglichen (siehe Nummer 7.3). Proben, die unter dem Cut-off-Wert liegen, gelten als konform, Proben, die dem Cut-off-Wert entsprechen oder diesen überschreiten, gelten als vermutlich nicht konform und müssen mit einem Bestätigungsverfahren untersucht werden. In der Praxis kann ein BEQ-Gehalt, der zwei Drittel des Höchstgehalts entspricht, als Cut-off-Wert dienen, sofern eine Falsch-negativ-Rate von unter 5 % sowie eine annehmbare Rate von falsch-positiven Ergebnissen gewährleistet wird. Da für PCDD/F und für die Summe von PCDD/F und dioxinähnliche PCB unterschiedliche Höchstgehalte gelten, ist zur Prüfung der Konformität der Proben ohne Fraktionierung ein geeigneter Bioassay-Cut-off-Wert für PCDD/F erforderlich. Zur Überprüfung von Proben, in denen die Aktionsgrenzwerte überschritten werden, eignet sich ein entsprechender Prozentsatz des jeweiligen Aktionsgrenzwerts als Cut-off-Wert.
Wird ein ungefährer Gehalt in BEQ ausgedrückt, müssen die Probenergebnisse angegeben werden, die im Arbeitsbereich liegen und den Meldewert überschreiten (siehe Nummern 7.1.1 und 7.1.6).
7.1. Signalauswertung
7.1.1. Allgemeine Anforderungen
7.1.2. Kalibrierung
7.1.2.1. Kalibrierung mittels Standardkurve
7.1.2.2. Kalibrierung anhand von Referenzproben
Alternativ kann eine Kalibrierkurve auf Grundlage von mindestens vier Referenzproben verwendet werden (siehe Nummer 7.2.4): eine Matrixleerwert-Probe sowie 3 Referenzproben, die jeweils 0,5x, 1x und 2x den Höchstgehalt oder den Aktionsgrenzwert enthalten, wodurch keine Notwendigkeit zur Korrektur um Blindwerte und Wiederfindung besteht, wenn sich die Matrixeigenschaften bei Referenzproben und unbekannten Proben decken. In diesem Fall kann das Signal, das zwei Drittel des Höchstgehalts entspricht (siehe Nummer 7.3), direkt auf Grundlage dieser Proben berechnet und als Cut-off-Wert verwendet werden. Zur Überprüfung von Proben, in denen die Aktionsgrenzwerte überschritten werden, eignet sich ein entsprechender Prozentsatz dieser Aktionsgrenzwerte als Cut-off-Wert.
7.1.3. Separate Bestimmung von PCDD/F und dioxinähnlichen PCB
Extrakte können in Fraktionen, welche PCDD/F und dioxinähnliche PCB enthalten, aufgetrennt werden, sodass PCDD/F-TEQ und TEQ der dioxinähnlichen PCB-Verbindungen (jeweils als BEQ) getrennt angegeben werden können. Zur Bewertung der Ergebnisse für die Fraktion, die dioxinähnliche PCB enthält, ist vorzugsweise eine PCB-126-Standardkalibrierkurve zu verwenden.
7.1.4. Beobachtete Bioassay-Wiederfindung
Die "beobachtete Bioassay-Wiederfindung" ist auf Grundlage geeigneter Referenzproben mit repräsentativen Kongeneren-Mustern im Bereich des Höchstgehalts oder des Aktionsgrenzwert zu berechnen und wird als Prozentsatz des BEQ-Gehalts im Vergleich zum TEQ-Gehalt ausgedrückt. Je nachdem, welche Art von Assay oder TEF 12 verwendet wird, können die Unterschiede zwischen TEF- und REP-Faktoren in dioxinähnlichen PCB zu niedrigeren Wiederfindungswerten für dioxinähnliche PCB im Vergleich zu PCDD/F führen. Daher muss die beobachtete Bioassay-Wiederfindung bei einer getrennten Bestimmung von PCDD/F und dioxinähnlichen PCB für dioxinähnliche PCB 20 bis 60 % und für PCDD/F 50 bis 130 % betragen (bei Verwendung einer TCDD-Kalibrierkurve). Der Beitrag der dioxinähnlichen PCB zur Summe der PCDD/F und dioxinähnlichen PCB kann je nach Matrices und Proben unterschiedlich sein; dies spiegelt sich in den Bereichen der beobachteten Bioassay-Wiederfindung für die Summe der PCDD/F und dioxinähnlichen PCB wider, die zwischen 30 und 130 % liegen müssen. Jeder Niederschlag wesentlicher Änderungen der TEF-Werte auf die Rechtsvorschriften der Union über PCDD/F und dioxinähnliche PCB erfordert eine Überarbeitung dieser Bereiche.
7.1.5. Kontrolle der Wiederfindung nach Reinigung der Probenextrakte
Der Verlust von Verbindungen während der Reinigung ist im Rahmen der Validierung zu überprüfen. Eine Matrixleerprobe, dotiert mit einem Gemisch verschiedener Kongenere, ist dem Reinigungsverfahren zu unterziehen (mindestens n = 3), und Wiederfindung und Streuung sind mittels eines Bestätigungsverfahrens zu untersuchen. Die Wiederfindung muss zwischen 60 und 120 % betragen, insbesondere für Kongenere, die in verschiedenen Gemischen jeweils mehr als 10 % des TEQ-Gehalts ausmachen.
7.1.6. Meldegrenze
Werden BEQ-Gehalte angegeben, ist auf der Grundlage relevanter Matrix-Proben, die typische Kongeneren-Muster aufweisen, eine Meldegrenze zu ermitteln; dabei ist die Kalibrierkurve der Standards aufgrund ihrer geringen Präzision im unteren Bereich nicht heranzuziehen. Die Einflüsse aus Extraktion und Reinigung müssen berücksichtigt werden. Die Meldegrenze muss mindestens um den Faktor 3 über den Methodenleerwerten liegen.
7.2. Verwendung von Referenzproben
7.2.1. Referenzproben müssen repräsentativ für Probenmatrix, Kongeneren-Muster und Konzentrationen für PCDD/F und dioxinähnliche PCB im Bereich des Höchstgehalts oder des Aktionsgrenzwerts sein.
7.2.2. Bei jeder Test-Reihe ist eine Matrixleerprobe, oder, sofern dies nicht möglich ist, eine Methodenleerwert-Probe, sowie eine Referenzprobe im Bereich des Höchstgehalts oder des Aktionsgrenzwerts einzubeziehen. Diese Proben müssen zur gleichen Zeit und unter identischen Bedingungen extrahiert und analysiert werden. Die Referenzprobe muss im Vergleich zu der Matrixleerprobe ein deutlich höheres Signal aufweisen, wodurch die Eignung des Analyseverfahrens gewährleistet ist. Solche Proben können zur Korrektur um Leerwert und Wiederfindung verwendet werden.
7.2.3. Referenzproben, die zur Korrektur um die Wiederfindung herangezogen werden, müssen repräsentativ für die Analysenproben sein, d. h., die Kongeneren-Muster dürfen nicht zu einer Unterschätzung der Gehalte führen.
7.2.4. Zusätzliche Referenzproben, deren Konzentration z.B. das 0,5- und 2-Fache des Höchstgehalts oder des Aktionsgrenzwerts beträgt, können einbezogen werden, damit die ordnungsgemäße Durchführung der Untersuchungen in dem für die Kontrolle des Höchstgehalts oder des Aktionsgrenzwerts relevanten Bereich nachgewiesen werden kann. In Kombination können diese Proben zur Berechnung der BEQ-Gehalte in den untersuchten Proben verwendet werden (siehe Nummer 7.1.2.2).
7.3. Bestimmung der Cut-off-Werte
Die Beziehung zwischen den in BEQ ausgedrückten Ergebnissen der bioanalytischen Methode und den in TEQ ausgedrückten Ergebnissen von Bestätigungsverfahren ist zu ermitteln, z.B. durch matrixbezogene Kalibrierexperimente unter Verwendung von Referenzproben, die mit 0, 0,5x, 1x und 2x Höchstgehalt dotiert sind und auf jeder Konzentrationsstufe jeweils 6 Mal untersucht werden (n = 24). Korrekturfaktoren (Leerwert und Wiederfindung) können auf der Grundlage dieses Verhältnisses geschätzt werden, sind jedoch gemäß Nummer 7.2.2 zu überprüfen.
Für die Entscheidung, ob eine Probe den Höchstgehalten entspricht, oder gegebenenfalls zur Überprüfung der Aktionsgrenzwerte sind Cut-off-Werte zu ermitteln, wobei die jeweiligen Höchstgehalte bzw. Aktionsgrenzwerte entweder einzeln für PCDD/F und dioxinähnliche PCB oder aber für die Summe von PCDD/F und dioxinähnlichen PCB festgelegt sein können. Sie stellen den unteren Endpunkt der Verteilung bioanalytischer Ergebnisse (korrigiert um Leerwert und Wiederfindung) von Proben dar, die Gehalte an der Entscheidungsgrenze des Bestätigungsverfahrens aufweisen, berechnet auf Grundlage eines Vertrauensniveaus von 95 %, was eine Falsch-negativ-Rate von < 5 % impliziert, und auf Basis einer RSDR unter 25 %. Die Entscheidungsgrenze des Bestätigungsverfahrens entspricht dem Höchstgehalt zuzüglich der erweiterten Messunsicherheit.
Der Cut-off-Wert (in BEQ) kann gemäß einem der unter den Nummern 7.3.1, 7.3.2 oder 7.3.3 beschriebenen Ansätze berechnet werden (siehe Abbildung 1).
7.3.1. Verwendung des unteren Bands des Prognoseintervalls von 95 % an der Entscheidungsgrenze des Bestätigungsverfahrens
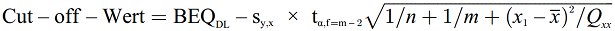
Dabei ist
| BEQDL | der BEQ-Wert, der der Entscheidungsgrenze des Bestätigungsverfahrens entspricht, die wiederum dem Höchstgehalt unter Berücksichtigung der erweiterten Messunsicherheit entspricht. |
| sy,x | die Reststandardabweichung |
| tα,f = m-2 | der Student-Faktor (α = 5 %, f = Freiheitsgrade, einseitig) |
| m | die Gesamtzahl der Kalibrierpunkte (Laufzahl j) |
| n | die Anzahl der Wiederholungen auf jeder Ebene |
| xi | die Probenkonzentration (in TEQ) des Kalibrierpunkts i, durch ein Bestätigungsverfahren ermittelt |
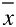 | der Mittelwert der Konzentrationen (in TEQ) aller Kalibrierproben |
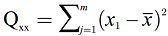 | Quadratsummenparameter, i = Laufzahl des Kalibrierpunkts i |
7.3.2. Berechnung aus bioanalytischen Ergebnissen (korrigiert um Leerwert und Wiederfindung) aus der Mehrfachuntersuchung (n ≥ 6) von Proben, die Gehalte an der Entscheidungsgrenze des Bestätigungsverfahrens aufweisen, als unterer Endpunkt der Datenverteilung am entsprechenden BEQ-Mittelwert:
Cut - off - Wert =BEQDL - 1,64 × SDR
Dabei ist
| SDR | die Standardabweichung der Bioassay-Ergebnisse am BEQDL, gemessen unter laborinternen Vergleichbarkeitsbedingungen. |
7.3.3. Berechnung als Mittelwert der bioanalytischen Ergebnisse (in BEQ, korrigiert um Leerwert und Wiederfindung) auf der Grundlage mehrfacher Untersuchungen (n ≥ 6) von Proben, die mit zwei Dritteln des Höchstgehalts oder des Aktionsgrenzwerts kontaminiert sind, auf Grundlage der Beobachtung, dass dieser Wert in der Nähe des gemäß Nummer 7.3.1 oder 7.3.2 bestimmten Cut-off-Wertes liegt.
Berechnung der Cut-off-Werte auf der Grundlage eines Vertrauensniveaus von 95 %, was eine Falsch-negativ-Rate von < 5 % impliziert, und auf Basis einer RSDR < 25 %:
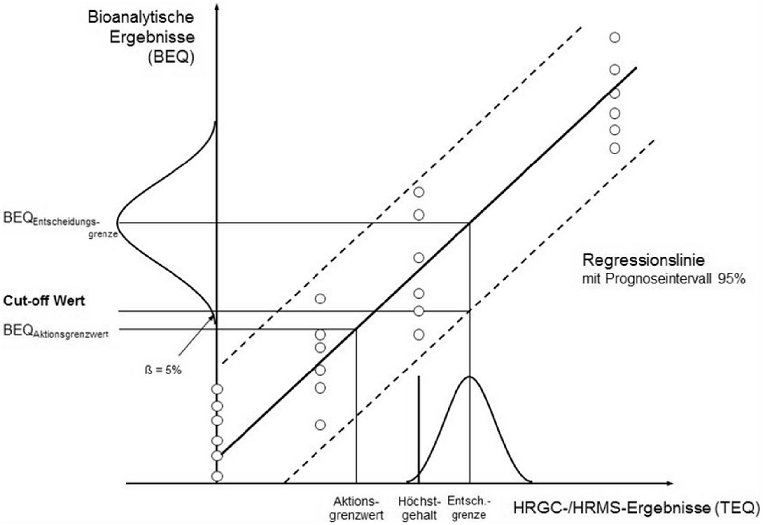
7.3.4. Beschränkungen der Cut-off-Werte:
Auf BEQ basierende Cut-off-Werte, die anhand der im Rahmen der Validierung und unter Verwendung einer begrenzten Anzahl von Proben mit unterschiedlichen Matrix-/Kongeneren-Mustern erzielten RSDR berechnet wurden, können höher sein als die auf TEQ basierenden Höchstgehalte oder Aktionsgrenzwerte, da hier die Präzision höher ist, als es in einer Routine möglich ist, in der ein unbekanntes Spektrum möglicher Kongeneren-Muster überprüft werden muss. In solchen Fällen ist der Berechnung der Cut-off-Werte eine RSDR = 25 % zugrunde zu legen, oder aber es sind zwei Drittel des Höchstgehalts oder des Aktionsgrenzwerts als Cut-off-Wert zu verwenden.
7.4. Leistungsmerkmale
7.4.1. Da bei bioanalytischen Methoden keine internen Standards verwendet werden können, sind Tests zur Wiederholbarkeit bioanalytischer Methoden durchzuführen, um Informationen über die Standardabweichung innerhalb einer Testreihe bzw. zwischen Testreihen zu erhalten. Die Wiederholbarkeit muss unter 20 % liegen, die laborinterne Vergleichbarkeit unter 25 %. Grundlage dafür müssen die nach Korrektur um Blindwert und Wiederfindung als BEQ berechneten Konzentrationen sein.
7.4.2. Während der Validierung muss nachgewiesen werden, dass mit dem Testverfahren zwischen einer Leerprobe und einem Gehalt in Höhe des Cut-off-Werts unterschieden werden kann, sodass Proben, deren Gehalt über dem entsprechenden Cut-off-Wert liegt, identifiziert werden können (siehe Nummer 7.1.2).
7.4.3. Die zu bestimmenden Verbindungen, mögliche auftretende Störungen und der maximal akzeptable Leerwert müssen festgelegt werden.
7.4.4. Die Standardabweichung in Prozent, mit der die Signalwerte oder die aus den Signalwerten berechneten Konzentrationen (nur möglich im Arbeitsbereich) behaftet sind, darf bei einer dreifachen Bestimmung eines Probenextrakts nicht mehr als 15 % betragen.
7.4.5. Zur Bewertung der Leistungsfähigkeit einer bioanalytischen Methode über einen konstanten Zeitraum hinweg sind die unkorrigierten Ergebnisse der Referenzprobe(n), ausgedrückt in BEQ (Leerwert und Höchstgehalt oder Aktionsgrenzwert), heranzuziehen.
7.4.6. Für Leerwert-Proben und für jede Art von Referenzproben sind Qualitätskontroll-Charts anzufertigen und zu prüfen, damit sichergestellt ist, dass die analytische Leistungsfähigkeit den Anforderungen genügt, insbesondere bei Methodenleerwert-Proben im Hinblick auf den erforderlichen Mindestabstand zum unteren Ende des Arbeitsbereichs und für Referenzproben hinsichtlich der laborinternen Vergleichbarkeit. Methodenleerwert-Proben sind so zu prüfen, dass falsch-negative Ergebnisse bei Abzug der Werte vermieden werden.
7.4.7. Die Ergebnisse der in Bezug auf verdächtige Proben durchgeführten Bestätigungsverfahren und von 2 bis 10 % der konformen Proben (mindestens 20 Proben je Matrix) sind zu sammeln und zur Bewertung der Leistungsfähigkeit des Screening-Verfahrens und der Beziehung zwischen BEQ und TEQ zu verwenden. Diese Datenbank kann zur Neubewertung der Cut-off-Werte für Routineproben der validierten Matrices genutzt werden.
7.4.8. Die Leistungsfähigkeit eines Verfahrens kann auch durch Teilnahme an Ringversuchen nachgewiesen werden. Die Ergebnisse von in Ringversuchen analysierten Proben, die einen Konzentrationsbereich bis zum doppelten Höchstgehalt abdecken, können zur Bewertung der Falsch-negativ-Rate herangezogen werden, wenn ein Laboratorium seine Leistungsfähigkeit unter Beweis gestellt hat. Die Proben müssen die häufigsten Kongeneren-Muster abdecken, die verschiedene Kontaminationsquellen repräsentieren.
7.4.9. Bei Kontaminationsfällen können die Cut-off-Werte neu ermittelt werden, um den Besonderheiten von Matrix und Kongeneren-Muster des jeweiligen Zwischenfalls Rechnung zu tragen.
8. Bericht über die Ergebnisse
8.1. Bestätigungsverfahren
8.1.1. Die Untersuchungsergebnisse müssen die Werte der einzelnen Kongenere von PCDD/F und dioxinähnlichen PCB enthalten, und die TEQ-Werte müssen als Untergrenze ("lower-bound"), Obergrenze ("upper-bound") und Mittelwert ("medium-bound") gemeldet werden, damit möglichst viele Informationen in den Untersuchungsberichten enthalten sind und die Ergebnisse somit entsprechend den speziellen Anforderungen interpretiert werden können.
8.1.2. In dem Bericht muss das zur Extraktion der PCDD/F und dioxinähnlichen PCB angewendete Verfahren genannt werden.
8.1.3. Die Wiederfindungsraten der einzelnen internen Standards sind zur Verfügung zu stellen, falls die Wiederfindungen außerhalb des unter Nummer 6.2.5 genannten Bereichs liegen, falls die Gehalte in den Proben den Höchstgehalt überschreiten (in diesem Fall die Wiederfindungen aus einer der beiden Untersuchungen) sowie in anderen Fällen auf Anfrage.
8.1.4. Da bei der Entscheidung über die Konformität einer Probe die erweiterte Messunsicherheit zu berücksichtigen ist, ist dieser Parameter vorzulegen. Das Analyseergebnis ist als x ± U anzugeben, wobei x das Analyseergebnis darstellt und U die erweiterte Messunsicherheit unter Verwendung eines Erweiterungsfaktors von 2, was einem Vertrauensniveau von ca. 95 % entspricht. Bei einer getrennten Bestimmung des Gehalts an PCDD/F und dioxinähnlichen PCB ist die Summe der geschätzten erweiterten Messunsicherheit der getrennten Analyseergebnisse der PCDD/F und der dioxinähnlichen PCB für die Berechnung der Summe der PCDD/F und dioxinähnlichen PCB zu verwenden.
8.1.5. Die Ergebnisse sind in denselben Einheiten und mit mindestens derselben Anzahl signifikanter Stellen anzugeben wie die in der Richtlinie 2002/32/EG festgelegten Höchstgehalte.
8.2. Bioanalytische Screening-Verfahren
8.2.1. Das Ergebnis des Screenings ist anzugeben als "konform" oder "vermutlich nicht konform" ("verdächtig").
8.2.2. Außerdem können annähernde Ergebniswerte für PCDD/F und/oder dioxinähnliche PCB in BEQ, nicht in TEQ, angegeben werden.
8.2.3. Proben, deren Gehalt unterhalb der Meldegrenze liegt, sind als solche zu bezeichnen. Proben, deren Gehalt "oberhalb des Arbeitsbereichs" liegt, sind mit dieser Angabe zu melden, und der der Obergrenze des Arbeitsbereichs entsprechende Gehalt ist in BEQ anzugeben.
8.2.4. In dem Bericht muss für jede Art von Probenmatrix der Höchstgehalt oder der Aktionsgrenzwert genannt werden, auf dem die Bewertung beruht.
8.2.5. Aus dem Bericht müssen die Art des verwendeten Tests, die grundlegenden Testprinzipien und die Art der Kalibrierung hervorgehen.
8.2.6. In dem Bericht muss das zur Extraktion der PCDD/F und dioxinähnlichen PCB angewendete Verfahren genannt werden.
8.2.7. Für Proben, die vermutlich nicht konform sind, muss der Bericht einen Hinweis auf die zu ergreifenden Maßnahmen enthalten. Die Konzentration von PCDD/F und der Summe von PCDD/F und dioxinähnlichen PCB in diesen Proben mit erhöhten Gehalten muss durch ein Bestätigungsverfahren ermittelt/bestätigt werden.
8.2.8. Nicht konforme Ergebnisse werden nur gemeldet, wenn sie in einem Bestätigungsverfahren ermittelt wurden.
8.3. Physikalisch-chemische Screening-Verfahren
8.3.1. Das Ergebnis des Screenings ist anzugeben als "konform" oder "vermutlich nicht konform" ("verdächtig").
8.3.2. In dem Bericht muss für jede Art von Probenmatrix der Höchstgehalt oder der Aktionsgrenzwert genannt werden, auf dem die Bewertung beruht.
8.3.3. Zudem können Werte der einzelnen Kongenere von PCDD/F und dioxinähnlichen PCB sowie als Untergrenze, Obergrenze und Mittelwert gemeldete TEQ-Werte angegeben werden. Die Ergebnisse sind in denselben Einheiten und mit mindestens derselben Anzahl signifikanter Stellen anzugeben wie die in der Richtlinie 2002/32/EG festgelegten Höchstgehalte.
8.3.4. Die Wiederfindungsraten der einzelnen internen Standards sind zur Verfügung zu stellen, falls die Wiederfindungen außerhalb des unter Nummer 6.2.5 genannten Bereichs liegen, falls die Gehalte in den Proben den Höchstgehalt überschreiten (in diesem Fall die Wiederfindungen aus einer der beiden Untersuchungen) sowie in anderen Fällen auf Anfrage.
8.3.5. Aus dem Bericht muss hervorgehen, welches GC-MS-Verfahren angewendet wurde.
8.3.6. In dem Bericht muss das zur Extraktion der PCDD/F und dioxinähnlichen PCB angewendete Verfahren genannt werden.
8.3.7. Für Proben, die vermutlich nicht konform sind, muss der Bericht einen Hinweis auf die zu ergreifenden Maßnahmen enthalten. Die Konzentration von PCDD/F und der Summe von PCDD/F und dioxinähnlichen PCB in diesen Proben mit erhöhten Gehalten muss durch ein Bestätigungsverfahren ermittelt/bestätigt werden.
8.3.8. Ob ein Wert nicht konform ist, kann nur in einem Bestätigungsverfahren entschieden werden.
Kapitel III
Probenvorbereitung und Anforderungen an Untersuchungsverfahren zur amtlichen Kontrolle des Gehalts an nicht dioxinähnlichen PCB in Futtermitteln
1. Anwendungsbereich
Die in diesem Kapitel beschriebenen Anforderungen gelten, wenn Futtermittel zur amtlichen Kontrolle des Gehalts an nicht dioxinähnlichen PCB sowie für die Probenvorbereitung und Untersuchungsanforderungen zu anderen regulatorischen Zwecken, darunter die Kontrollen der Futtermittelunternehmer zur Gewährleistung der Vorschriftsmäßigkeit gemäß der Verordnung (EG) Nr. 183/2005, untersucht werden.
2. Anzuwendende Nachweisverfahren
Gaschromatografie/Elektroneneinfangdetektor (GC-ECD), GC-LRMS, GC-MS/MS, GC-HRMS oder gleichwertige Verfahren.
3. Bestimmung und Bestätigung der interessierenden Analyten
3.1. Relative Retentionszeit im Verhältnis zu internen Standards oder Referenzstandards (akzeptable Abweichung ± 0,25 %).
3.2. Gaschromatografische Trennung der nicht dioxinähnlichen PCB von interferierenden Stoffen, insbesondere von koeluierenden PCB und insbesondere dann, wenn die Gehalte der Proben an der gesetzlichen Grenze liegen und bestätigt werden muss, dass sie nicht konform sind 13.
3.3. Anforderungen an GC-MS-Techniken
Messung von mindestens der folgenden Anzahl an Molekül-Ionen oder charakteristischen Ionen des Molekül-Clusters:
Zulässige Höchsttoleranzen für das Isotopenhäufigkeitsverhältnis für ausgewählte Massenfragmente:
Relative Abweichung des Isotopenhäufigkeitsverhältnisses ausgewählter Massenfragmente von der theoretischen Häufigkeit oder dem Kalibrierstandard für das Ziel-Ion (das am häufigsten vorkommende Ion) und das/die Qualifizier-Ion(en): ± 15 %.
3.4. Anforderungen an GC-ECD-Techniken
Ergebnisse, die den Höchstgehalt überschreiten, sind anhand von zwei GC-Säulen mit stationären Phasen unterschiedlicher Polarität zu bestätigen.
4. Nachweis der Leistungsfähigkeit des Verfahrens
Die Leistungsfähigkeit der Methode im Bereich des Höchstgehalts (0,5- bis 2facher Höchstgehalt) mit einem akzeptablen Variationskoeffizienten für wiederholte Untersuchung (siehe Anforderungen an die Laborpräzision unter Nummer 9) ist zu validieren.
5. Bestimmungsgrenze
Die Summe der Bestimmungsgrenzen (LOQ) 14 nicht dioxinähnlicher PCB darf ein Drittel des Höchstgehalts nicht übersteigen 15.
6. Qualitätssicherung
Regelmäßige Blindkontrollen, Analysen dotierter Proben, Qualitätssicherungsproben, Teilnahme an Laborvergleichsuntersuchungen zu relevanten Matrices.
7. Kontrolle der Wiederfindungsrate
7.1. Es sind geeignete interne Standards mit physikalisch-chemikalischen Eigenschaften, die denen der interessierenden Analyten vergleichbar sind, zu verwenden.
7.2. Zugabe interner Standards:
Zugabe zu Erzeugnissen (vor Extraktion und Clean-up).
7.3. Anforderungen an Verfahren, bei denen alle sechs isotopenmarkierten nicht dioxinähnlichen PCB-Kongenere verwendet werden:
7.4. Anforderungen an Verfahren, bei denen nicht alle sechs isotopenmarkierten internen Standards oder andere interne Standards verwendet werden:
7.5. Die Wiederfindungen nicht markierter Kongenere sind mittels dotierter Proben oder Qualitätskontrollproben mit Konzentrationen im Bereich des Höchstgehalts zu prüfen. Für diese Kongenere sind Wiederfindungsraten zwischen 60 und 120 % akzeptabel.
8. Anforderungen an Laboratorien
Gemäß den Bestimmungen der Verordnung (EU) 2017/625 müssen die Laboratorien von einer anerkannten Stelle akkreditiert sein, die nach ISO/IEC Guide 58 arbeitet, damit sichergestellt ist, dass die Laboratorien bei der Untersuchung Qualitätssicherungsverfahren anwenden. Die Laboratorien müssen gemäß der Norm EN ISO/IEC 17025 akkreditiert sein. Zudem sind die in den technischen Leitlinien für die Schätzung der Messunsicherheit und der Bestimmungsgrenzen für die Untersuchung auf PCB beschriebenen Grundsätze zu befolgen 16.
9. Leistungsmerkmale: Kriterien für die Summe der nicht dioxinähnlichen PCB im Bereich des Höchstgehalts
| Isotopenverdünnungs-Massenspektrometrie * | Andere Techniken | |
| Richtigkeit | -20 bis + 20 % | -30 bis + 30 % |
| Laborpräzision (RSD %) | ≤ 15 % | ≤ 20 % |
| Differenz zwischen berechneter Obergrenze ("upper-bound") und Untergrenze ("lower-bound") | ≤ 20 % | ≤ 20 % |
| *) Alle sechs 13C-markierten Analoga müssen als interne Standards verwendet werden. | ||
10. Bericht über die Ergebnisse
10.1. Die Untersuchungsergebnisse müssen die Werte der einzelnen nicht dioxinähnlichen PCB und der Summe solcher PCB-Kongenere enthalten, angegeben als Untergrenze ("lower-bound"), Obergrenze ("upper-bound") und Mittelwert ("medium-bound"), damit möglichst viele Informationen in den Untersuchungsberichten enthalten sind und die Ergebnisse somit entsprechend den speziellen Anforderungen interpretiert werden können.
10.2. In dem Bericht muss das zur Extraktion der PCB angewendete Verfahren genannt werden.
10.3. Die Wiederfindungsraten der einzelnen internen Standards sind zur Verfügung zu stellen, falls die Wiederfindungen außerhalb des unter Nummer 7 genannten Bereichs liegen, falls die Gehalte in den Proben den Höchstgehalt überschreiten sowie in anderen Fällen auf Anfrage.
10.4. Da bei der Entscheidung über die Konformität einer Probe die erweiterte Messunsicherheit zu berücksichtigen ist, ist dieser Parameter ebenfalls vorzulegen. Das Analyseergebnis ist als x ± U anzugeben, wobei x das Analyseergebnis darstellt und U die erweiterte Messunsicherheit unter Verwendung eines Erweiterungsfaktors von 2, was einem Vertrauensniveau von ca. 95 % entspricht.
10.5. Die Ergebnisse sind in denselben Einheiten und mit mindestens derselben Anzahl signifikanter Stellen anzugeben wie die in der Richtlinie 2002/32/EG festgelegten Höchstgehalte.
B. Europäische Normen (EN)
Für die Anwendung von Artikel 34 Absatz 2 Buchstabe a der Verordnung (EU) 2017/625 sind die folgenden europäischen Normen maßgeblich:
| EN 17194: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Deoxynivalenol, Aflatoxin B1, Fumonisin B1 und B2, T-2- und HT-2-Toxine, Zearalenon und Ochratoxin A in Einzelfuttermitteln und Mischfuttermitteln mittels LC-MS/MS |
| EN 17270: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Theobromin in Einzel- und Mischfuttermitteln, einschließlich aus Kakao gewonnenen Bestandteilen, mittels Flüssigchromatographie |
| EN 17504: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Gossypol in Baumwollsamen und Futtermitteln mittels LC-MS/MS |
| EN 17362: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Pentachlorphenol (PCP) in Futtermittel und Mischfuttermittel mittels LC-MS/MS |
| EN 16279: Futtermittel - Bestimmung des Fluoridgehaltes nach Salzsäure-Behandlung mit ionensensitiver Elektrode (ISE) |
| EN 17053: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Spurenelementen, Schwermetallen und anderen Elementen in Futtermitteln mittels ICP-MS (Multimethode) |
| EN 15550: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von Cadmium und Blei mittels Graphitrohrofen-Atomabsorptionsspektrometrie (GF-AAS) nach Druckaufschluss |
| EN 16206: Futtermittel - Bestimmung von Arsen mit Atomabsorptionsspektrometrie-Hydridtechnik (HD-AAS) nach Mikrowellen-Druckaufschluss (Aufschluss mit 65 % Salpetersäure und 30 % Wasserstoffperoxid) |
| EN 16277: Futtermittel - Bestimmung von Quecksilber mit Kaltdampf-Atomabsorptionsspektrometrie (KD-AAS) nach Mikrowellen-Druckaufschluss (Extraktion mit 65 % Salpetersäure und 30 % Wasserstoffperoxid) |
| EN 16278: Futtermittel - Bestimmung von anorganischem Arsen mit Atomabsorptionsspektrometrie-Hydridtechnik (HD-AAS) nach Mikrowellen-Extraktion und Trennung durch Festphasenextraktion (SPE) |
| EN 17374: Futtermittel - Probenahme- und Untersuchungsverfahren - Bestimmung von anorganischem Arsen in Futtermittel mittels Anionenaustausch HPLC-ICP-MS |
"
| Kongener | TEF-Wert | Kongener | TEF-Wert |
| Dibenzo-p-dioxine (PCDD) und Dibenzo-p-furane (PCDF) | "Dioxinähnliche PCB" Non-ortho-PCB + Mono-ortho-PCB | ||
| 2,3,7,8-TCDD | 1 | ||
| 1,2,3,7,8-PeCDD | 1 | Non-ortho PCB | |
| 1,2,3,4,7,8-HxCDD | 0,1 | PCB 77 | 0,0001 |
| 1,2,3,6,7,8-HxCDD | 0,1 | PCB 81 | 0,0003 |
| 1,2,3,7,8,9-HxCDD | 0,1 | PCB 126 | 0,1 |
| 1,2,3,4,6,7,8-HpCDD | 0,01 | PCB 169 | 0,03 |
| OCDD | 0,0003 | Mono-ortho PCB | |
| 2,3,7,8-TCDF | 0,1 | PCB 105 | 0,00003 |
| 1,2,3,7,8-PeCDF | 0,03 | PCB 114 | 0,00003 |
| 2,3,4,7,8-PeCDF | 0,3 | PCB 118 | 0,00003 |
| 1,2,3,4,7,8-HxCDF | 0,1 | PCB 123 | 0,00003 |
| 1,2,3,6,7,8-HxCDF | 0,1 | PCB 156 | 0,00003 |
| 1,2,3,7,8,9-HxCDF | 0,1 | PCB 157 | 0,00003 |
| 2,3,4,6,7,8-HxCDF | 0,1 | PCB 167 | 0,00003 |
| 1,2,3,4,6,7,8-HpCDF | 0,01 | PCB 189 | 0,00003 |
| 1,2,3,4,7,8,9-HpCDF | 0,01 | ||
| OCDF | 0,0003 | ||
Abkürzungen: "T" = tetra; "Pe" = penta; "Hx" = hexa; "Hp" = hepta; "O" = octa; "CDD" = Chlordibenzodioxin; "CDF" = Chlordibenzofuran; "CB" = Chlorbiphenyl.
2) Durchführungsverordnung (EU) 2021/808 der Kommission vom 22. März 2021 über Leistungskriterien für Analysemethoden für Rückstände pharmakologisch wirksamer Stoffe in zur Lebensmittelerzeugung genutzten Tieren und über die Auswertung von Ergebnissen sowie über die für Probenahmen anzuwendenden Methoden und zur Aufhebung der Entscheidungen 2002/657/EG und 98/179/EG (ABl. L 180 vom 21.05.2021 S. 84).
3) Falls zutreffend, sind die im "Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry" (https://food.ec.europa.eu/system/files/2017-05/animal-feed-guidance_document_pcdd-f_pcb_en.pdf) beschriebenen Grundsätze zu befolgen.
4) "Zweitanalyse": getrennte Untersuchung der interessierenden Analyten anhand eines zweiten Aliquots derselben homogenisierten Probe. Grundsätzlich gelten für Zweitanalysen die Anforderungen gemäß Anhang II Kapitel C Nummer 3. Bei Verfahren, bei denen 13C-markierte interne Standards für die relevanten Analyten verwendet werden, ist die Zweitanalyse jedoch nur erforderlich, wenn das Ergebnis der ersten Bestimmung nicht konform ist. Die Zweitanalyse ist erforderlich, um eine interne Kreuzkontamination oder eine versehentliche Vertauschung der Proben auszuschließen. Bei einer Untersuchung im Verlauf eines Kontaminationsfalls kann auf die Bestätigung durch Zweitanalyse verzichtet werden, wenn sich die untersuchten Proben auf den Kontaminationsfall zurückverfolgen lassen und der gemessene Wert deutlich über dem Höchstgehalt liegt.
5) Nach dem Konzept der "Obergrenze" ("upper-bound") wird der Beitrag jedes nicht quantifizierten Kongeners der Bestimmungsgrenze gleichgesetzt. Beim Konzept der "Untergrenze" ("lower-bound") wird der Beitrag jedes nicht quantifizierten Kongeners gleich null gesetzt. Beim Konzept des "Mittelwerts" ("medium-bound") wird der Beitrag jedes nicht quantifizierten Kongeners der Hälfte der Bestimmungsgrenze gleichgesetzt.
6) Grundsätzlich gelten für Zweitanalysen die Anforderungen gemäß Anhang II Kapitel C Nummer 3. Bei Bestätigungsverfahren, bei denen 13C-markierte interne Standards für die relevanten Analyten verwendet werden, ist die Zweitanalyse jedoch nur erforderlich, wenn das Ergebnis der ersten Bestimmung nicht konform ist. Die Zweitanalyse ist erforderlich, um eine interne Kreuzkontamination oder eine versehentliche Vertauschung der Proben auszuschließen. Bei einer Untersuchung im Verlauf eines Kontaminationsfalls kann auf die Bestätigung durch Zweitanalyse verzichtet werden, wenn sich die untersuchten Proben auf den Kontaminationsfall zurückverfolgen lassen und der gemessene Wert deutlich über dem Höchstgehalt liegt.
7) Nach dem Konzept der "Obergrenze" ("upper-bound") wird der Beitrag jedes nicht quantifizierten Kongeners zum TEQ der Bestimmungsgrenze gleichgesetzt. Beim Konzept der "Untergrenze" ("lower-bound") wird der Beitrag jedes nicht quantifizierten Kongeners zum TEQ gleich null gesetzt. Beim Konzept des "Mittelwerts" ("medium-bound") wird der Beitrag jedes nicht quantifizierten Kongeners zum TEQ der Hälfte der Bestimmungsgrenze gleichgesetzt.
8) Für Zweitanalysen zur Kontrolle der Aktionsgrenzwerte gelten die gleichen Erklärungen und Anforderungen wie die für Höchstgehalte in Fußnote 33 genannten.
9) Verordnung (EG) Nr. 183/2005 des Europäischen Parlaments und des Rates vom 12. Januar 2005 mit Vorschriften für die Futtermittelhygiene (ABl. L 35 vom 08.02.2005 S. 1).
10) Bioanalytische Methoden sind nicht spezifisch für diejenigen Kongenere, die in das TEF-Schema fallen. Im Probenextrakt können auch andere, strukturverwandte AhR-aktive Verbindungen vorliegen, die zur Gesamt-Zellantwort beitragen. Daher erlauben bioanalytische Ergebnisse keine Schätzung des TEQ-Gehalts, sondern stellen eher einen Hinweis auf den TEQ-Gehalt in einer Probe dar.
11) "Guidance Document on Measurement Uncertainty for Laboratories performing PCDD/F and PCB Analysis using Isotope Dilution Mass Spectrometry" [https://food.ec.europa.eu/system/files/2017-05/animal-feed-guidance_document_pcdd-f_pcb_en.pdf], "Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food" [https://food.ec.europa.eu/system/files/2016-10/cs_contaminants_sampling_analysis-report_2004_en.pdf].
12) Die derzeitigen Anforderungen basieren auf den in M. Van den Berg et al, Toxicol Sci 93 (2), 223-241 (2006) veröffentlichten TEF.
13) Kongenere, die oft koeluieren, sind beispielsweise PCB 28/31, PCB 52/69 und PCB 138/163/164. Bei GC-MS-Verfahren muss auch die Möglichkeit von Störungen durch Fragmente höher chlorierter Kongenere berücksichtigt werden.
14) Falls zutreffend, sind die im "Guidance Document on the Estimation of LOD and LOQ for Measurements in the Field of Contaminants in Feed and Food' (https://data.europa.eu/doi/10.2787/8931) beschriebenen Grundsätze zu befolgen.
15) Ein geringerer Beitrag der Reagenzienleerwerte zum Kontaminationsgehalt der Probe ist äußerst empfehlenswert. Das Labor ist dafür zuständig, die Variation der Leerwerte zu überwachen, insbesondere, wenn die Leerwerte abgezogen werden.
16) Siehe Fußnote 37.
| Anhang VI |
"Anhang VII
Methode zur Berechnung des Energiegehalts von Futtermitteln für Geflügel
1. Berechnungsmethode und Formel des Energiegehalts
Der Energiegehalt von Mischfuttermitteln für Geflügel muss anhand der prozentualen Anteile bestimmter analytischer Bestandteile der Futtermittel nach nachstehender Formel berechnet werden. Dieser Wert wird in Megajoules (MJ) umsetzbarer, N-korrigierter Energie (ME) je kg Mischfuttermittel ausgedrückt und nach folgender Formel berechnet:
MJ ME/kg = 0,1551 × % Rohprotein + 0,3431 × % Rohfett + 0,1669 × % Stärke + 0,1301 × % Gesamtzucker (ausgedrückt als Saccharose).
2. Toleranzen auf die angegebenen Gehalte
Ergibt sich bei den amtlichen Untersuchungen eine energieerhöhende oder energievermindernde Abweichung zwischen dem Kontrollergebnis und dem angegebenen Energiegehalt, so gilt eine Toleranz von 0,4 MJ ME/kg.
3. Angabe der Ergebnisse
Das nach vorstehender Formel errechnete Ergebnis ist mit nur einer Dezimalstelle anzugeben.
4. Probenahmeverfahren und Analysemethoden
Die Probenahme beim Mischfuttermittel und die Bestimmung des Gehalts an der Berechnungsmethode zugrunde liegenden analytischen Bestandteilen erfolgt in Übereinstimmung mit den Probenahmeverfahren bzw. Analysemethoden der Union für die amtliche Untersuchung von Futtermitteln.
Anzuwenden sind:
Methode zur Berechnung des Energiegehalts von Futtermittel-Ausgangserzeugnissen und Mischfuttermitteln für Katzen und Hunde
Der Energiegehalt von Futtermittel-Ausgangserzeugnissen und Mischfuttermitteln für Katzen und Hunde ist gemäß folgender Norm zu berechnen: EN 16967: Futtermittel - Probenahme- und Untersuchungsverfahren - Schätzgleichungen für umsetzbare Energie in Futtermittel-Ausgangserzeugnissen und Mischfuttermitteln (Heimtierfutter) für Katzen und Hunde, einschließlich Diätfuttermittel."
 | ENDE |